

2022年12月,由中华医学会心血管病学分会心血管病影像学组、动脉粥样硬化与冠心病学组、冠状动脉腔内影像及生理学学组及基础研究学组和中华心血管病杂志编辑委员会相关专家制定了《缺血伴非阻塞性冠状动脉疾病诊断及管理中国专家共识》并发表于《中华心血管病杂志》,旨在结合我国国情及临床实践,进一步明确INOCA诊疗规范,为临床提供指导。西安交通大学第一附属医院袁祖贻教授作为通信作者,在武汉亚心年会上对该共识进行解读。

据悉,该共识经过线下、线上专家反复研讨,具有临床实践意义。2021年12月18日厦门召开共识启动会,2022年5月15日线上召开共识审稿会,2022年6月26日线上召开共识审稿会。

心绞痛与冠心病息息相关,非阻塞性冠状动脉病变占70%。心绞痛是冠心病最常见的症状,据调查,在中国慢性稳定性冠心病患者中,82.9%的患者出现劳力性心绞痛。然而,高达70%的心绞痛患者在冠状动脉造影(CAG)后未检出阻塞性冠状动脉病变。非阻塞性冠状动脉疾病发病率高。我国数据表明,在因心绞痛入院接受造影的患者中,约20%为非阻塞性冠状动脉疾病;因疑似心绞痛和/或负荷试验阳性而接受 CAG的患者中,39%的为非阻塞性冠状动脉疾病。临床误诊和治疗不足常见。近20年研究表明,冠状动脉微血管功能障碍和血管痉挛是导致心肌缺血的重要机制。但由于目前无法直观评估冠状动脉微血管,使得这些患者的症状被误认为是非心源性原因所致,从而导致误诊和治疗不足。
国内对非阻塞性冠状动脉疾病认识不充分,亟需相关专家共识。尽管我国分别于2015年和2017年推出了《冠状动脉痉挛综合征诊断与治疗中国专家共识》及《冠状动脉微血管疾病诊断和治疗的中国专家共识》,但目前临床对于此类疾病认识尚不充分。
据推测,我国缺血伴非阻塞性冠状动脉疾病的疾病负担较重,为了更好的规范诊断和管理,临床专家制定了本共识,以期进一步明确INOCA诊疗规范,为临床提供指导。经过专家共识会议和文献回顾,本共识总结了非阻塞性冠脉疾病发生的机制和分型、临床表现和预后,并给出了诊断和治疗的推荐方案。多方法及时诊断,推荐个体化治疗。
共识框架分为六个部分:INOCA的定义和流行病学、INOCA发病机制及分型、INOCA的临床表现、INOCA预后、INOCA诊断、INOCA治疗及管理(见于Part 3部分)。
一、INOCA的定义和流行病学
2022中国共识针对INOCA给出了具体的定义。缺血伴非阻塞性冠状动脉疾病(INOCA)是指一类具有缺血性胸痛症状和心肌缺血客观证据,但冠状动脉造影(CAG)或冠状动脉计算机断层扫描血管成像(CCTA)未发现阻塞性冠状动脉病变的临床综合征。一项历时19年的研究显示,对1439例INOCA患者进行侵入性评估发现,2/3的患者有微血管功能障碍。国内研究报道,存在静息胸痛且CAG提示心外膜血管狭窄<50%的人群中,75%患者药物激发试验阳性。
二、INOCA发病机制及分型
1.INOCA的发病机制与CMD(冠状动脉微血管功能障碍)和/或CAS(冠状动脉痉挛)导致的心肌缺血相关。INOCA 主要由 CMD和/或冠状动脉痉挛导致心肌需氧与血供之间出现不匹配,从而出现缺血相关表现。

2.INOCA可分为微血管性心绞痛(MVA)和血管痉挛性心绞痛(VSA)。微血管性心绞痛主要由冠状动脉微血管结构重塑和/或功能障碍导致。血管痉挛性心绞痛是由于冠状动脉痉挛引起,不同于劳力性心绞痛,通常表现为夜间及静息时发生,伴心电图相应导联ST段缺血性改变。
3.了解冠状动脉微血管结构和调节机制,警惕微血管性心绞痛。正常生理条件下,当心肌耗氧量增加时,代谢产物增加促进小型微小动脉血管扩张,导致中型微小动脉的管腔压力降低,从而使得血管扩张,进一步增加近端大型微小动脉及前小动脉血流量,使其心外膜动脉扩张,增加心肌总体灌注量。

4.微血管结构重塑和微血管功能障碍是导致INOCA的病理原因。微血管结构重塑存在肥胖、吸烟、糖尿病等危险因素及动脉粥样硬化等疾病的患者中,冠脉微血管可出现向心性重塑。表现为管壁增厚、管腔缩小和/或心肌毛细血管密度降低。微血管功能障碍一方面表现为一氧化氮的合成减少,血管扩张能力降低,微循环阻力升高。另一方面,平滑肌细胞反应性升高,出现反常的血管收缩。
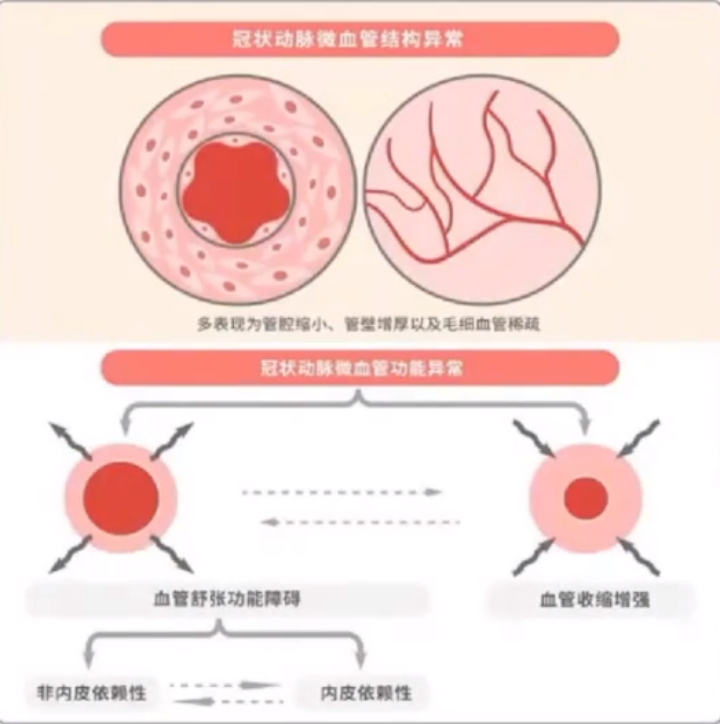
5.血管痉挛性心绞痛不可小觑,多种因素导致其发生。短暂的血管痉挛可能无症状、或出现心绞痛和心电图变化,但痉挛持续不缓解,则可诱发急性心肌梗死、心律失常及猝死。血管痉挛发生的相关因素包括:血管内皮细胞功能紊乱、平滑肌细胞收缩反应性增高、自主神经功能障碍、氧化应激、动脉粥样硬化、慢性炎症。
三、INOCA的临床表现
INOCA患者的临床表现差异较大,警惕误诊。
1.微血管性心绞痛,可表现为劳力性心绞痛,也可以出现气促、肩胛骨区疼痛、消化不良、恶心、乏力、虚弱、呕叶以及睡眠障碍等不典型表现。在中青年女性中不典型症状更为多见。
2.血管痉挛性心绞痛,更多见于男性,以静息性胸痛为主要表现,多在寒冷刺激、大量吸烟、过量饮酒、情绪波动等条件下诱发。
由于INOCA患者临床表现差异较大,在认识不足的情况下可能出现误诊。对于非典型症状的患者,特别是女性、长期吸烟或合并糖尿病的患者,应仔细鉴别并评估,决定是否进一步检查。
四、INOCA预后
INOCA患者的预后情况不容乐观。INOCA患者如果没有得到明确的诊断和及时治疗,可能导致生活质量下降、残疾风险、医疗费用支出及不良事件发生风险升高。特别是有确切心肌缺血证据的CMD患者,预后更差。
女性缺血综合征评价(WISE)研究,纳入189名疑似缺血女性并进行冠脉血流储备(CFR)评估,观察其主要不良心血管结局和冠脉血流储备之间的关系。研究发现,CFR<2.32的女性患者5年主要不良心血管事件发生率为26.6%,而CFR≥2.32的女性患者仅为9.3%。

五、INOCA诊断
1.INOCA的诊断——非侵入性检测方法。
初步评估方法常见的是运动负荷试验,但其对CMD诊断效能不佳,灵敏度仅为35%,特异性为65%。对于疑诊INOCA患者,在排除阻塞性冠状动脉狭窄之后,可采用无创方法评估冠状动脉微循环功能。
对于疑诊INOCA患者,通过对比静息和最大充血状态下冠状动脉血流(CBF)比值从而获得CFR。CFR是反映冠脉循环的重要生理学指标,综合反映了心外膜冠状动脉和冠状动脉微循环对心肌供血能力。无创功能性成像方法有以下这些:经胸超声冠状动脉血流显像(TTDE)、心肌声学造影超声心动图(MCE)、单光子发射计算机断层成像术(SPECT)、心脏磁共振成像(CMR)、正电子发射计算机断层扫描(PET)。
常用的无创功能性成像方法的优势和不足


2.INOCA的诊断——侵入性检测方法
选择性冠状动脉造影,冠脉造影可以从心外膜冠状动脉显影和心肌显影速度两个方面来间接评价冠脉微血管功能。心外膜冠状动脉显影速度的评价多采用心肌梗死溶栓治疗临床试验(TIMI)血流分级及TIMI血流计帧法。心肌显影速度的评价方法包括:①TIMI心肌显影分级;②心肌显影密度分级;③ TIMI心肌灌注帧数。
有创功能检查,由于冠状动脉解剖学狭窄程度无法准确评估心肌缺血,特别是存在冠脉临界病变的患者,应首先进行FFR评估,当FFR≤0.8提示存在阻塞性冠状动脉疾病。
血管反应性评估。对于INOCA患者,还应通过痉挛激发试验,进一步评估微血管功能障碍机制及血管反应性。进行冠脉痉挛激发试验前,患者应停用钙拮抗剂及长效硝酸酯类药物至少24小时,短效硝酸酯类药物至少6小时。
微循环功能异常的诊断流程及标准
2020 EAPCI专家共识

基于功能性冠状动脉造影结果,可进一步明确INOCA患者亚型及缺血机制。
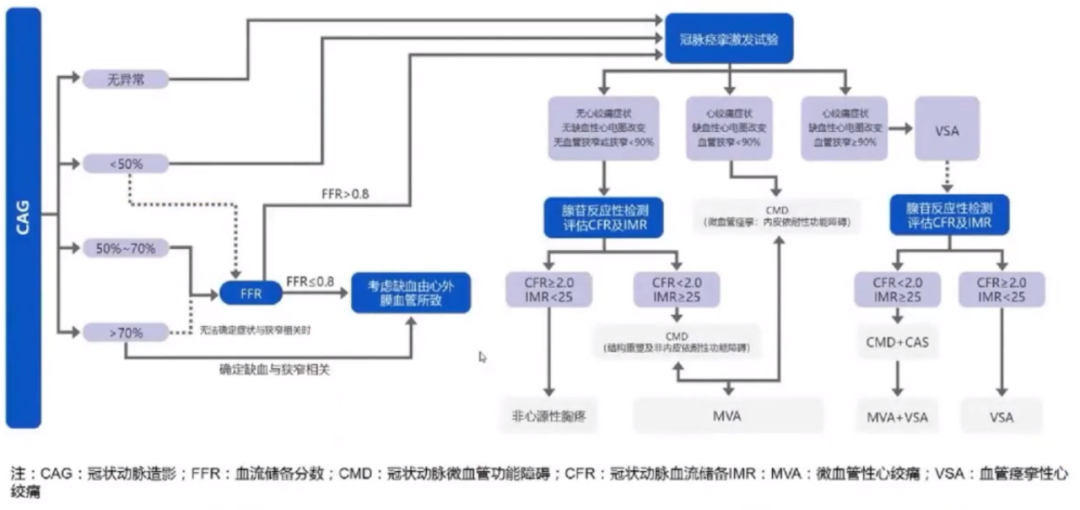
临床实际中可结合各医院及患者实际情况进行选择诊断方式。
INOCA诊断流程图
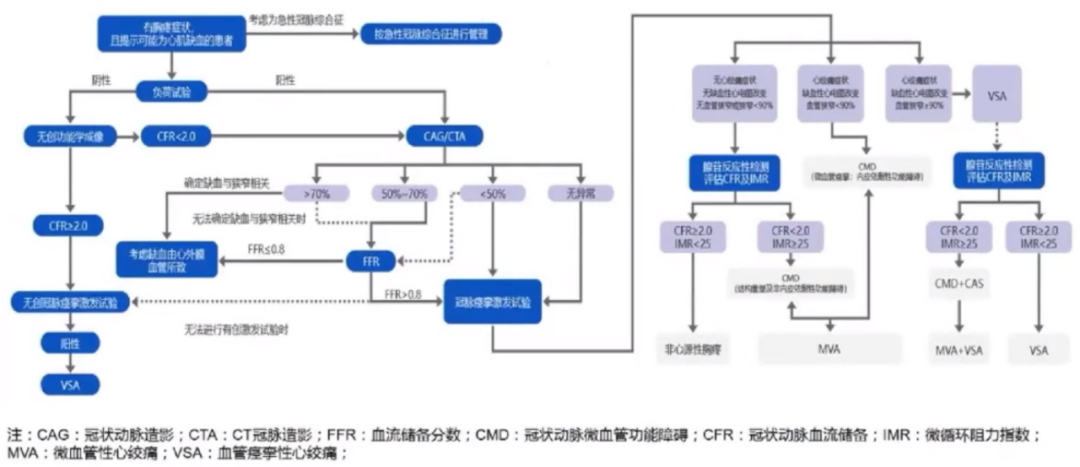
本共识推荐对INOCA患者进行个体化治疗。目前关于INOCA患者管理的循证证据较为缺乏,本共识基于现有研究结果并采纳专家意见,推荐采用联合生活方式、危险因素控制及药物治疗的模式,对INOCA患者进行个体化治疗。生活管理包括戒烟、限酒、饮食管理、适量运动。药物治疗,根据疾病的类型进行对症治疗,具体可见后面内容。非药物治疗,当药物治疗效果不佳时,可考虑非药物治疗。
亮点聚焦1:INOCA患者的生活方式管理
1.戒烟和控制体重,戒烟及控制体重有助于改善CMD患者的血管内皮功能和心绞痛症状。
2.饮食管理,地中海饮食可以降低心血管疾病风险,可能与不饱和脂肪酸改善了内皮功能有关。
3.精神状态,焦虑、抑郁等精神异常状态可能与女性INOCA患者出现心绞痛症状和CAD风险升高相关。定期心理咨询、体育锻炼可能有助于改善患者症状。
亮点聚焦2:INOCA患者的危险因素管理
传统的心血管疾病危险因素如高血压、高脂血症及糖尿病可导致冠状动脉粥样硬化及微血管功能障碍,因此有效的危险因素控制手段可改善患者微血管功能及血流储备能力。
1.降压药物
(1)降压药物的选择主要取决于心肌缺血发生机制。
(2)血管紧张素转换酶抑制剂(ACEI)可改善MVA患者血管重构、CFR并减少心绞痛症状,应作为MVA患者首选降压药物。
(3)血管紧张素受体阻滞剂(ARB)也具有改善CFR和保护内皮的作用2, ACEI不耐受者可选用。
(4)对于VSA患者,钙通道阻滞剂(CCB)则应作为首选。
2.降脂药
WISE研究发现,79%的INOCA患者存在动脉粥样硬化。他汀类药物具有降脂、抗氧化应激、抗炎、改善内皮功能作用,可改善 No-obCAD患者内皮功能和CFR。小剂量阿司匹林可能有助于改善INOCA患者的不良结局。
3.降糖药
钠-葡萄糖协同转运体2抑制剂(SGLT2-i)可降低糖尿病患者 MACE发生风险。体外实验显示,抑制内皮细胞 SGLT2可改善高血糖导致的血管功能障碍。
亮点聚焦3:INOCA患者的抗心绞痛治疗
基于CorMicA研究的结果,应依据INOCA不同机制选择个体化治疗方案。
1.MVA患者多数患者心率增快,β受体阻滞剂可有效降低患者心肌耗氧量,改善患者心肌缺血症状。奈比洛尔除控制心率外,还可扩张血管及抗氧化应激,改善血管内皮功能。伊伐布雷定选择性抑制窜房结If电流,降低窦性心率,减少心肌耗氧量,改善MVA患者症状。
2.VSA患者非二氢吡啶类CCB如地尔硫卓可降低心外膜血管痉挛的发生率,应作为一线治疗药物。部分严重心绞痛患者可能需要大剂量治疗方案或与二氢吡啶类联用以控制症状。不同的CCB对VSA患者心绞痛症状改善无明显差异,但贝尼地平能更有效降低心血管事件的发生。
3.微血管性心绞痛的一线、二线治疗药物选择。
-
一线治疗
β受体阻滞剂:奈比洛尔、阿替洛尔、卡维地洛、美托洛尔。
钙离子拮抗剂(CCB):贝尼地平、地尔硫卓、氨氯地平。
血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂(ACEI/ARB):喹那普利、培哚普利、雷米普利。
-
二线治疗
其他药物:尼可地尔、伊伐布雷定
心肌能量药物:曲美他嗪、雷诺嗪
他汀类:瑞舒伐他汀、阿托伐他汀
4.血管痉挛性心绞痛或合并微血管性心绞痛的一线、二线治疗药物选择。对于合并动脉粥样硬化的INOCA患者,应考虑使用低剂量阿司匹林、他汀及ACEI/ARB的联合为基础治疗方案。
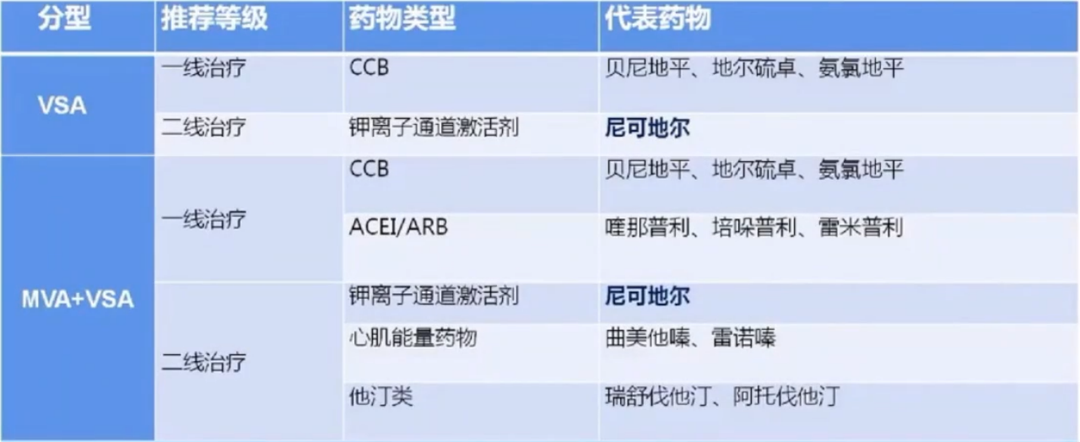
5.INOCA的其他治疗药物
(1)内皮素受体拮抗剂。当MVA患者血清ET-1浓度增加时,可降低诱发心绞痛的运动阈值,而内皮素受体拮抗剂达卢生坦可改善CMD患者的内皮功能。
(2)三环类抗抑郁药。低剂量三环类抗抑郁药物(如丙咪嗪)有助于改善INOCA患者的心绞痛症状。
(3)左旋精氨酸。左旋精氨酸通过促进 NO释放并降低内皮素-1水平,可能改善 INOCA患者内皮功能障碍。
(4)Rho激酶抑制剂。法舒地尔可以抑制乙酰胆碱诱发的微血管痉挛,改善 VSA患者心绞痛症状并显著降低CMD患者IMR(微循环阻力指数)。
(5)磷酸二酯酶抑制剂。西洛他唑可缓解CCB治疗无效的顽固性VSA心绞痛。
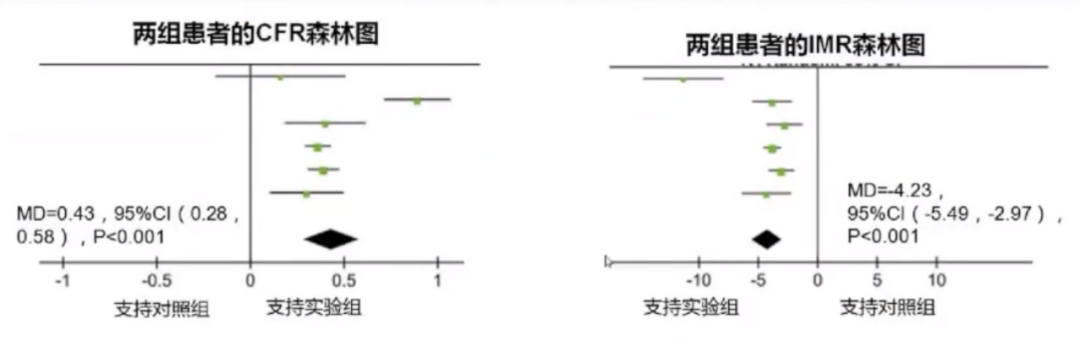
中医药在一定程度上可改善冠状动脉微循环。荟萃分析表明,通心络、麝香保心丸联合常规冠心病治疗方案可增加CFR,降低IMR,有效改善冠状动脉微血管功能。
亮点聚集4:非药物治疗方法在一定程度可改善INOCA患者症状
心脏康复治疗及运动训练可改善CMD患者心绞痛症状。对于常规治疗效果不佳的患者,可考虑增强体外反搏或脊髓刺激疗法,在一定程度上可改善患者内皮功能及疼痛情况。

1.缺血伴非阻塞性冠状动脉疾病(INOCA)发生率高,且存在显著性别及年龄差异。INOCA主要由CMD和/或冠状动脉痉挛导致心肌需氢与血供之间出现不匹配,从而出现缺血相关表现。
2.《缺血伴非阻塞性冠状动脉疾病诊断及管理中国专家共识》从INOCA的定义、发病机制和分型、临床表现、预后、诊断、治疗和管理等方面进行了阐述,为临床治疗提供了借鉴。
3.本共识基于现有研究结果并采纳专家意见,推荐采用联合生活方式、危险因素控制及药物治疗的模式,对于INOCA患者进行个体化治疗。
