

导读:左主干分又病变因解剖部位的特殊性,其血运重建策略一直是临床上争论的焦点。随着经皮冠状动脉介入治疗技术的进步,药物洗脱支架材料和工艺的改进、腔内影像学的发展、新型抗血小板药物的应用以及近年来国内外相关随机对照研究结果提供的有力的循证医学证据,介入治疗已经成为左主干分叉病变的重要治疗策略之一。南京市第一医院张俊杰教授以分叉病变的评估及双支架术式选择为题,深入浅出的为我们论述了对于假性分叉病变和简单真性分叉病变,可选Provisional stenting术式;对于复杂的左主干真性分叉病变,DK-Crush双支架术式是首选策略。

依据2018年ESC指南推荐,对于分叉病变的PCI的患者,建议只在左主干内植入支架,必要时行球囊血管内成形术,伴有或不伴有侧支支架。Ⅰ级推荐,证据质量等级A。
对药物治疗耐药的心绞痛患者或闭塞血管区域有大面积缺血的患者,应推荐CTO的经皮血管重建术。Ⅱa级推荐,证据质量等级B。
在左主干真性分叉病变中,双支架技术可能优于必要时支架植入。Ⅱb级推荐,证据质量等级B。
由此可以看出,对于大多数分叉病变,左主干支架植入和侧支必要时支架植入术应该是首选治疗方法。但是,对于复杂病变:大侧支≥2.75mm伴有长开口侧支病变(≥5mm),或左主干支架植入后预期难以进入重要侧支,以及真性的LM(左主干)末端分叉病变。
01必要时支架植入
对于何种场景可以行必要时支架植入(provisional stenting,PS),张教授提到说对于那些尽管是真性分叉病变,但开口局限,狭窄程度比较轻微的病变,毫无疑问可以provisional stenting。Provisional stenting“标准”流程如下:最佳血管造影影像,评估侧支重要性,病变布线,预扩张,主干支架植入术,近端支架优化技术(POT),侧支治疗-开放/支架。

02何时使用双支架技术
在分叉病变中,对于何时使用双支架技术,2019年EBC(欧洲分叉病变俱乐部)的一项欧洲专家共识中提到了双支架术式的适应证主要针对非常复杂的病变,包括严重钙化的SB(分支血管)病变和/或分支开口病变延伸>5mm;分支导丝通过比较困难。但目前该共识提到的内容证据等级为C,缺乏随机对照的支撑来验证推荐。
03 DEFINITION系列研究
对于简答、复杂病变的判定标准,2014年我国专家陈绍良教授团队在著名杂志《JACC Cardiovasc Interv.》中提出了冠状动脉复杂分叉病变的DEFINITION标准:
-
2个主要标准:(1)左主干远端分叉病变:分支狭窄程度≥70%,分支病变长度≥10 mm;(2)非左主干分叉病变:分支狭窄程度≥90%,分支病变长度≥10 mm。
-
6个次要标准:(1)中重度钙化;(2)多处病变(1、2两个因素已被证实与预后不良有关);(3)分叉角度<45度;(4)冠脉主支直径<2.5 mm;(5)病变处有血栓(通常见于急性冠脉综合征)(6)主支病变长度≥25 mm。
患者只要达到1个主要标准及任何2个次要标准,就能判定为复杂分叉病变。

DEFINITION研究除了提出复杂分叉病变的标准,还去验证了该标准在手术指导选择,以及判定预后的合理性和精准性。研究中可以看到,复杂分叉病变的 1 年 MACE(主要不良心血管事件)和 ST(支架内血栓)发生率较高。双支架和Provisional stenting技术在 1 年的 MACE 中总体相当。然而,复杂病变的双支架技术引起的心源性死亡率和院内 MACE 发生率较低,对于简单病变,院内 ST 和 1 年血运重建率较高。

由此可以看出,简单的冠状动脉分叉病变的PS是主要的治疗方法。系统的双支架方法广泛用于复杂分叉病变(CBL)。但是,对于 PS 和双支架技术用于 CBL 的随机对照研究还缺乏证据。为此,2018年陈绍良教授团队在《BMJ Open》上又发布了DEFINITION Ⅱ试验的基本原理和设计,旨在阐明在 CBL 患者中双支架治疗相对于 PS 的益处。
该试验共纳入 660 名 CBL 患者,将其以 1:1 的方式随机接受 PS 或双支架技术。主要终点是 12 个月目标病变失败率,定义为心源性死亡、目标血管心肌梗死 (MI) 和临床驱动的目标病变血运重建的复合。主要次要终点包括所有死亡原因、心肌梗死、靶血管血运重建、支架内再狭窄、中风和主要终点的每个单独组成部分。安全性终点是确定或可能的支架血栓形成。

最终研究成果于2020年发表在《Eur Heart J. 》上,研究结论认为对于标准定义的复杂冠状动脉分叉病变,与PS方法相比,系统性双支架方法与临床结果的显著改善相关。迫切需要进一步研究以确定导致临时支架植入后 TVMI 发生率增加的机制。

2022年DEFINITION Ⅱ试验完成了三年临床随访,其结果又发表在《JACC Cardiovasc Interv.》上。
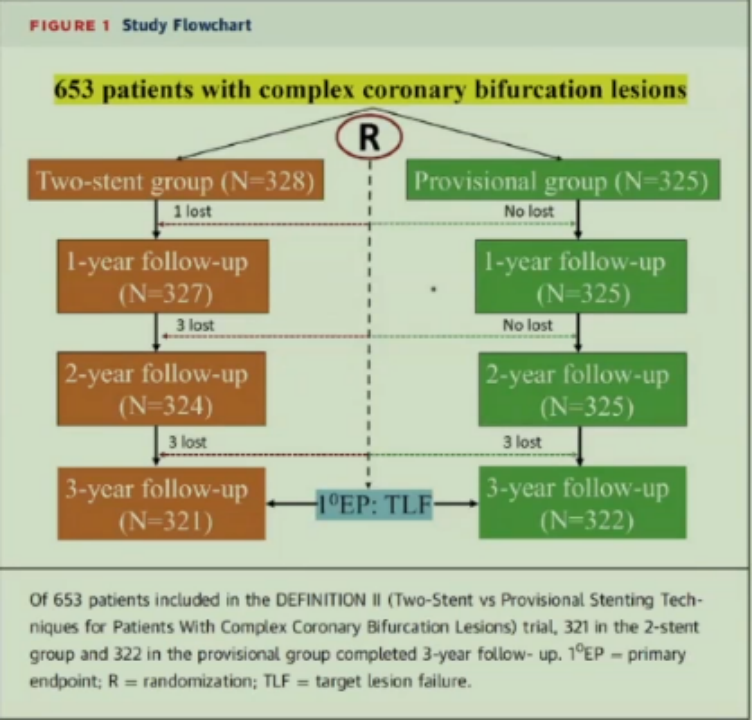
从研究结果中可以看到, 3 年时,PS 组 52 名患者(16.0%)和双支架组 34 名(10.4%)患者发生 TLF(HR:0.63;95% CI:0.41-0.97;P = 0.035 ),主要是由于靶血管心肌梗死增加(8.0% vs 3.7%;HR:0.45;95% CI:0.23-0.89;P = 0.022)和靶病变血运重建(8.3% vs 4.3%;HR:0.50;95% CI:0.26-0.96;P = 0.038)。


进一步分析了PS的亚组数据,可以看出双支架技术的获益主要是源于早期1年内的获益。在第 1 年和第 3 年时,单双支支架组之间的 TLF(靶病变失败)没有显著差异。

此外,在事先定义的PS组中,事后有22%患者在分支也植入了支架,也就是单支架Cross-over到双支架组。在分支植入支架的PS组中可以看出三年的事件率明显增高。因此,对于这种复杂的分叉病变,如果最后在分支植入支架,则患者的预后较差。

该研究还事先定义了围手术期并发症,包括B型或C型的夹层,TIMI血流分级≤3级,急性闭塞、穿孔或支架内血栓形成。研究中看到,一旦患者在围手术期发生上述并发症,3年随访时显著增加靶病变失败。这也提示对于复杂分叉病变,采用双支架技术可以避免围手术期并发症,进而避免随访期间出现更多的不良事件。

PS:Culotte,T,TAP
DK-Crush(double kissing crush双对吻挤压术):分支血管支架置入、主支球囊挤压分支支架、第一次球囊对吻扩张、主干支架置入、POT、最终球囊对吻扩张、及最后POT。
Culotte:确保扩张容量,在大球囊扩张的每次支架植入后立即POT。对于MV(主支)远端开口处狭窄或SB与MV近端存在较大直径差异的患者,可考虑采用其他方法。
T型支架:定位困难,失误后在分支开口留有支架真空区域增加。
TAP:避免在MV中放置太长的SB支架 ,因为会形成金属嵴。
Culotte技术详细操作步骤如下:分支支架释放,回拉后扩张,贴壁好后POT,随后进行第一次Rewire,成功后进行第一次球囊对吻,再植入主支支架,进行主支支架的POT,再进行第二次Rewire,第二次对吻扩张,最终的POT。

Culotte技术的局限性是SB和主支近端之间存在潜在的径线不匹配问题。
观察DK-Crush系列随机对照试验后,一致的发现:相较不同的双支架术式,包括经典Crush、经典Culotte以及PS,不论是主干末端还是非主干末端的分叉病变,DK-Crush获益持续存在;而且不止体现在1年,甚至体现在中长期随访(2年或5年)。

DK-CrushⅢ是迄今为止唯一比较了不同双支架技术治疗左主干末端真性分叉病变的随机对照研究。研究1年和3年的随访结果清楚的显示,DK-Crush对于左主干末端真性分叉病变的远期疗效优于经典Culotte术式。

此外,对于左主干末端真性分叉病变,DK-Crush也是最先比较单支架和双支架技术,1年和3年随访结果也证明,双支架技术由于单支架技术。
基于此,结合多项研究和ESC欧洲指南共同推荐,对于左主干末端的真性分叉病变优先采用DK-Crush双支架术式。
我国学者也于2022年4月发布了《中国冠状动脉左主干分叉病变介入治疗指南》。该指南包括前言、左主干分叉病变的解剖学特点及危险评分系统、左主干分叉病变血运重建策略选择,介入治疗术后双联抗血小板策略,术后越访及长期管理。该指南的领布和实族将为规范我国左主干分叉病变的介入治疗发挥积极作用。

当然,腔内影像学也是有大量循证医学证据。2018年张教授在《JACC》上发表了《血管内超声与血管造影引导的药物洗脱支架植入:终极试验》文章,旨在确定所有患者在 DES(药物洗脱支架)植入期间 IVUS(血管内超声影像)指导相对于血管造影指导的益处。
研究总共纳入1,448 名需要 DES 植入的患者被随机分配(1:1 比例)到 IVUS 指导组或血管造影指导组。主要终点是 12 个月时的TVF,包括心源性死亡、靶血管心肌梗死和临床驱动的靶血管血运重建 (TVR)。如果满足所有 IVUS 定义的最佳标准,则该程序被定义为成功。
PCI 手术后 12 个月发生了 60 例 TVF,其中 IVUS 指导组为 21 例(2.9%),血管造影指导组为 39 例(5.4%)(HR:0.530;95% CI:0.312 至 0.901;p = 0.019 )。两组之间临床驱动的TVR 、TVMI 和 CD 的差异不显著。有 6 例确定/可能ST,IVUS 组有 1 例可能 ST(0.1%),血管造影指导组有 5 例(0.7%)(2 例确定和 3 例可能;p = 0.10)。然而,组间临床驱动的TLR和明确 ST的复合没有显著差异。预先指定的亚组分析显示,患有 ACS 或多支血管疾病的患者可能受益于 IVUS 指导。符合最佳标准的患者在 12 个月时的 TVF 发生率(1.6%)低于接受次优 PCI 手术的患者(4.4%;HR:0.349;95% CI:0.135 至 0.898;p = 0.029 )。IVUS 组 5 例 (0.7%) 和血管造影指导组 3 例 (0.4%) 进行了非靶病变血运重建 (p = 0.726)。

血管内超声 (IVUS) 引导对接受药物洗脱支架 (DES) 植入的所有患者都是有益的,尤其是在实现 IVUS 定义的最佳程序时。如果满足所有 3 个标准,则定义了最佳 IVUS 引导 PCI:1)支架段的最小管腔面积(MLA)>5.0 mm2或远端参考段 MLA 的 90%;2) 支架边缘近端或远端5 mm处的斑块负荷<50%;3) 不涉及长度超过 3 毫米的支架边缘的夹层。如果不满足上述 3 条标准中的任何一条,则定义为次优 IVUS 引导的 PCI。

最终3年的随访结果于2021年公布,从数据中可以看到IVUS指导组获益持续存在,风险降低4%。

张教授最后总结道,DEFINITION 造影的标准可以帮助我们从造影上区分简单和复杂分叉病变;对于复杂的分叉病变,采用双支架技术特别是DK-Crush,3年的随访结果显示,它有更低的靶病变失败,靶血管心肌梗死以及靶病变血运重建,当然获益主要源于术后1年;对于复杂的左主干分叉病变,采用双支架植入技术时,血管内成像有助于评估病变,预测治疗效果,揭示并发症,优化手术结果,降低TVF的风险;DKCRUSH-Ⅷ试验比较IVUS与血管造影指导DK-Crush支架治疗复杂分叉病变的效果正在进行中。
