

高龄是急性冠状动脉综合征( ACS)发病的独立危险因素,也是ACS患者最强的死亡预测因素之一。既往研究显示,1/3因急性心肌梗死(AMI)住院的患者年龄≥75岁,2/3因AMI而死亡的患者年龄≥75岁。然而,关于老年患者临床治疗的循证医学证据仍较缺乏,仅不到7%的ACS临床研究纳入了老年(≥75岁)患者。老年ACS患者的治疗已成为心血管医师面临的最棘手问题之一。此外,老年患者有多器官变化,出血和缺血事件的风险增加,频繁的并发症/药物治疗,以及对处方的依从性降低等因素,使得老年人抗血栓治疗存在巨大挑战。首都医科大学附属北京安贞医院聂绍平教授在一次会议中就“老年ACS患者的优化抗栓治疗策略”作汇报,详细老年ACS抗栓策略。

WHO发布的《关于老龄化与健康的全球报》显示,我国在2050年60岁以上人口将占总人口的30%以上。
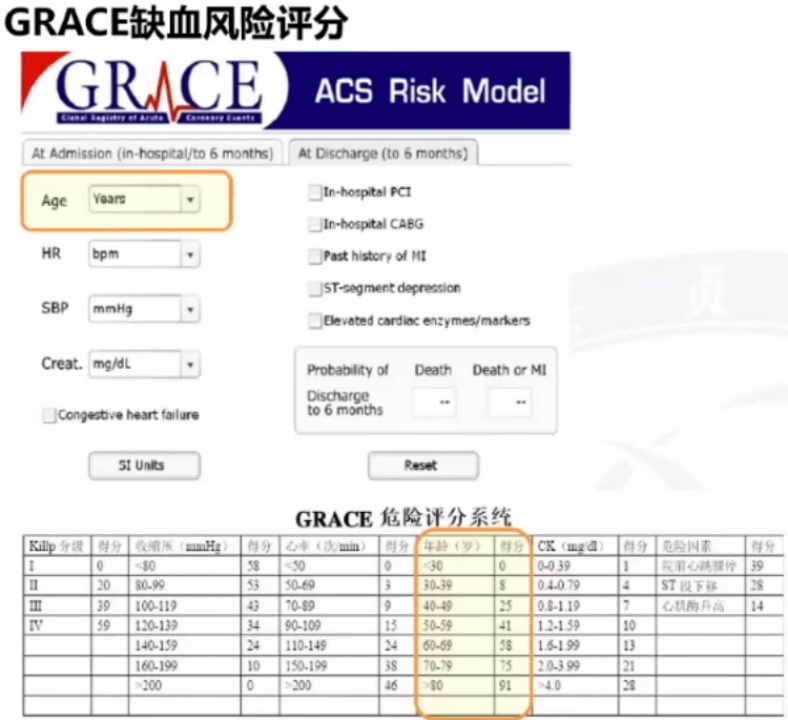
2007年JAMA杂志的GRACE研究对比了ST 段抬高型心肌梗死 (STEMI) 和非ST 段抬高急性冠状动脉综合征(NSTE ACS)患者的医院管理变化是否与临床结果的改善相关。研究显示,在纳入1999.7-2006.12期间14个国家113所医院44372例ACS患者后,结果显示患者年龄多超过65岁。最终,研究结论认为ACS 患者管理的改善与 6 个月时新发心力衰竭发生率和死亡率以及卒中和心肌梗塞发生率的显著降低有关。

2015年EHJ杂志提示,1/3因AMI住院的患者超过75岁,2/3因MI死亡的患者超过75岁。
ACS的出血风险评估及缺血风险评估均将高龄列为危险因素。ARC-HBR(高出血风险学术研究联盟)在临床上首次为PCI术后高出血患者的识别制定了标准化的定义,并提出了PCI术后高出血风险患者的14条主要标准和6条次要标准,患者至少满足一个主要标准或两个次要标准,就属于高出血风险状态。
主要标准:
1.服用口服抗凝药物;
2.严重或终末期慢性肾脏病(eGFR <30 ml/min);
3.中度或重度贫血(Hb<110 q/L);
4.6个月内发生需要住院和/或输血的自发性出血或在任何时间内的再发出血;
5.中度或重度血小板减少症(<100 x109/L);
6.慢性出血性体质;
7.肝硬化伴门静脉高压;
8.过去12个月内存在活动性恶性肿癌;
9.颅内自发性出血史(既往任何时间);
10.12个月内存在创伤性颅内出血;
11.已知的脑动静脉畸形;
12.6个月内有中度或重度缺血性卒中;
13.计划DAPT期间进行大手术;
14.PCI前30天内的大手术或严重创伤。
次要标准:
1.年龄≥75岁;
2.中度慢性肾脏病(eGFR 30-59 ml/min);
3.轻度贫血(男性Hb 110-129 g/L,女性Hb 110~119 g/L);
4.12个月内发生需要住院和/或输血的自发性出血(未满足主要标准);
5.长期应用NSAID类与类固醇类药物;
6.任何时间的缺血性卒中(未满足主要标准)。
老年ACS患者常合并心房颤动、慢性肾脏病(CKD)、脑血管疾病(颅内出血)、慢性气道疾病、外周血管疾病和低体重/营养不良等,复杂的病情也最终会影响患者的个体化治疗。
2021年聂教授团队在《中国心血管杂志》中提到了ACS抗栓治疗时合并颅内出血是抗栓治疗的致死性并发症,超过1/3的颅内出血为致死性出血。研究显示,与未发生颅内出血的患者相比,发生颅内出血的PCI术后患者死亡风险增加23倍。大量研究证实,高龄与抗栓治疗时合并颅内出血密切相关。Blee MACS注册研究显示,高龄是ACS患者颅内出血的独立预测因子。荟萃分析显示,年龄每增长10岁颅内出血风险升高1.6倍。因此,老年ACS患者在抗栓治疗中防治颅内出血至关重要。
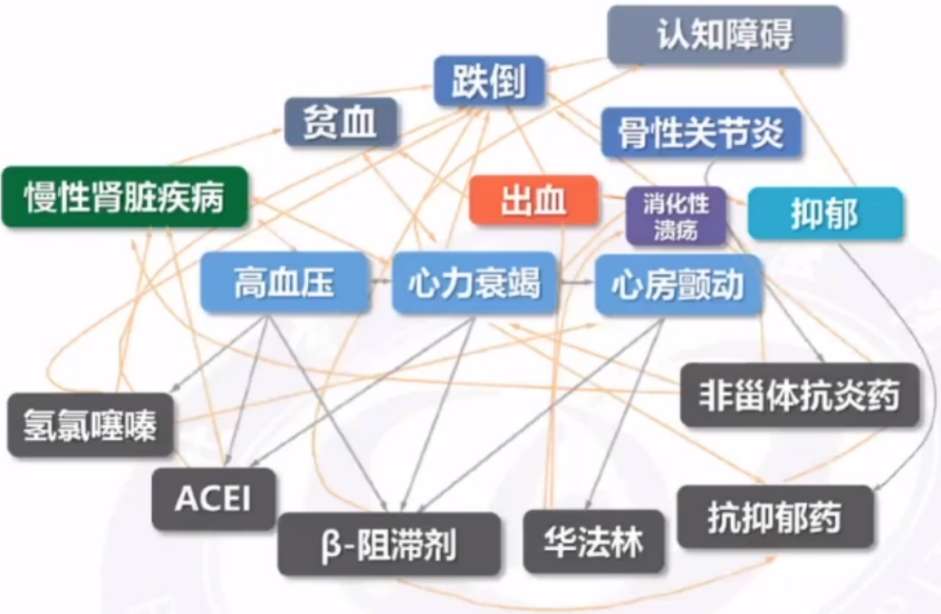
服用多种药物,可能存在药物间相互作用
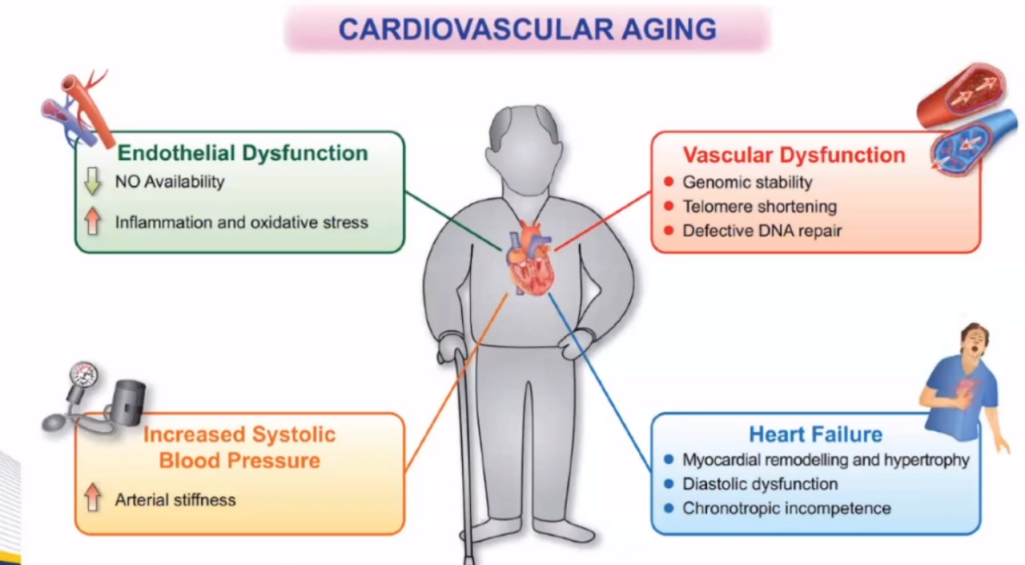
老年患者心血管相关的诸多病理生理过程发生变化
欧洲老年抗栓专家共识报道,不到7%的ACS临床研究纳入了高龄患者。

1.老年患者抗栓治疗的出血发生率和严重程度均高。
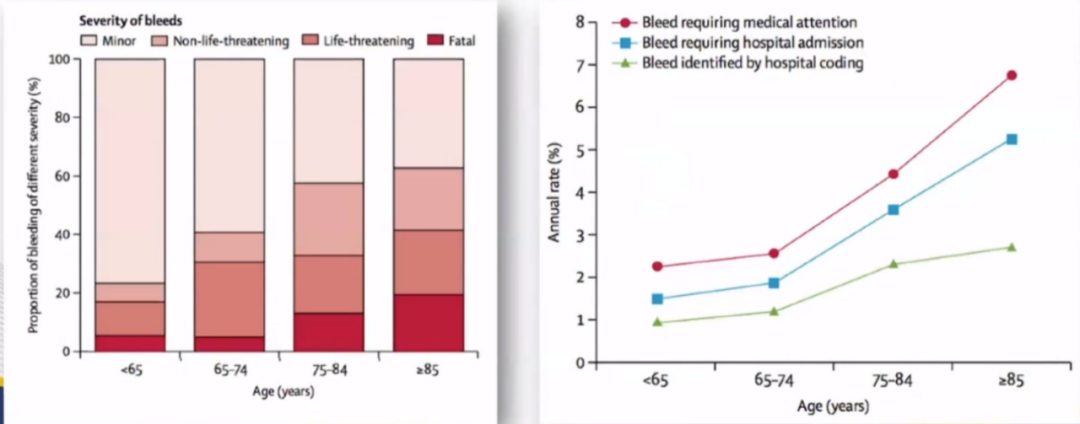
抗栓治疗的出血发生率和严重程度随年龄的增长而升高。2017年Lancet杂志发布了《血管事件后长期抗血小板治疗的年龄特异性风险、严重程度、时间过程和出血结局:一项基于人群的队列研究》,对 2002 年- 2012 年牛津血管研究中首次发生短暂性脑缺血发作、缺血性中风或心肌梗死并接受抗血小板药物治疗(主要是基于阿司匹林,未常规使用 PPI)的患者进行了一项基于人群的前瞻性队列研究,随访到 2013 年。研究通过 10 年的面对面随访确定了出血的类型、严重程度、结果(残疾或死亡)和需要医疗护理的时间过程。
在 13509 患者年的随访期间,3166 名患者(1582 [50%] 年龄≥75 岁)发生了 405 起首次出血事件(n=218 胃肠道出血,n=45 颅内出血,n=142 其他出血事件)。在入院的 314 名出血患者 (78%) 中,有 117 名 (37%) 被管理编码遗漏。非大出血的风险与年龄无关,但大出血随着年龄的增长急剧增加(≥75 岁风险比 [HR] 3·10,95% CI 2·27-4·24;p<0·0001),尤其是对于致命性出血,并在长期随访期间持续存在。大的上消化道出血也是如此(≥75 岁 HR 4·13, 2·60-6·57;p<0·0001),特别是如果是致残或致命的。
在 75 岁或以上时,主要的上消化道出血大多是致残或致死的(73 例复发性缺血性卒中患者中有 45 例 [62%] vs 213 例患者中有 101 例 [47%]),并且超过致残或致死性脑出血(n=45 vs n=18),每 1000 名患者年的绝对风险为 9·15 (95% CI 6·67-12·24)。在 5 年内常规使用 PPI 预防 1 次致残性或致命性上消化道出血的估计 NNT 从 65 岁以下个体的 338 下降到 85 岁或以上个体的 25。
溶栓时代对ACS后颅内出血的发生率进行了详细研究;然而,在PCI治疗时代,大部分数据都来自临床试验。在此背景下,2019年Eur Heart J Acute Cardiovasc Care杂志发表了BleeMACS研究,旨在分析接受PCI的ACS患者出院后颅内出血的发生率、时间、预测因素和预后影响。
研究发现在 11136 名患者中,30 名患者在第一年出现颅内出血 (0.27%)。颅内出血的中位时间为 150 天(四分位间距 55.7-319.5)。颅内出血的死亡率非常高(30%)。多变量分析后,只有年龄(亚风险比 1.05,95% 置信区间 1.01-1.07)和既往卒中/短暂性脑缺血发作(风险比 3.29,95% 置信区间 1.36-8.00)与较高的颅内出血风险独立相关。高血压显示出与较高的颅内出血率相关的趋势。年龄较大(75岁)、既往中风/短暂性脑缺血发作和/或高血压的组合使我们能够识别出大多数颅内出血患者 (86.7%)。颅内出血年发生率为0。
研究结论:接受PCI后的ACS患者1年内颅内出血的发生率较低。高龄、既往中风/短暂性脑缺血发作和高血压是颅内出血风险增加的主要预测因素。

2.老年患者存在诸多易出血的机制
(1)老年患者血小板数量降低,凝血功能异常。
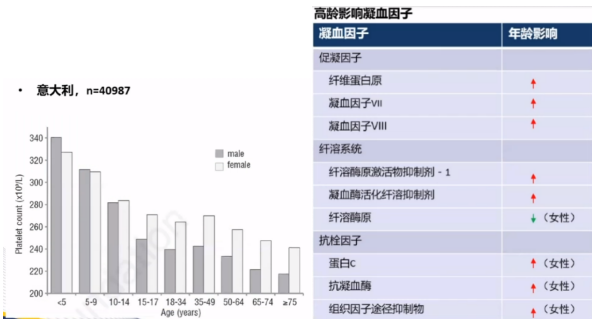
3.年龄已成为出血风险调评估的重要因素
2015年欧洲老年抗栓专家共识强调,在缺血和出血风险的平衡中应整合年龄因素。

合理选择和使用 P2Y12抑制剂
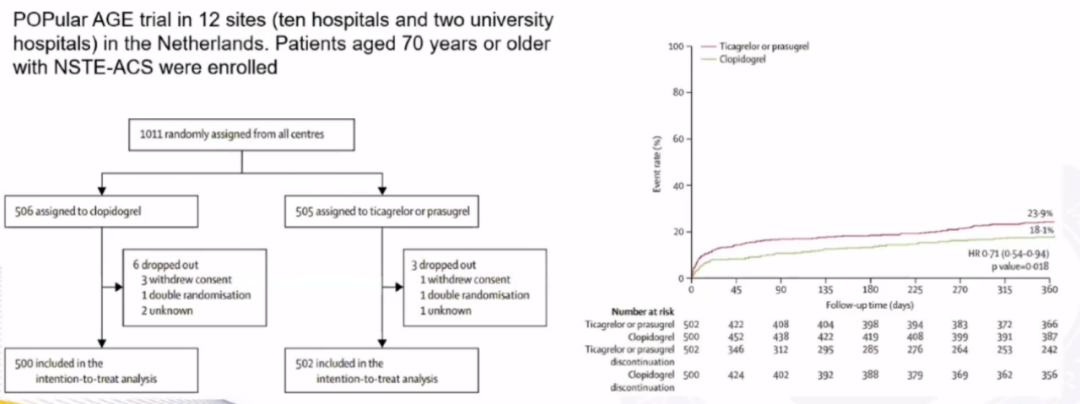
2020年Lancet杂志POPular AGE研究发现:在 70 岁或以上的 NSTE-ACS 患者中,氯吡格雷是替格瑞洛的有利替代品,因为它可以减少出血事件,而不会增加全因死亡、心肌梗死、卒中和出血的综合终点。因此与新型P2Y12抑制剂相比,氯吡格雷在老年患者中的获益更大。
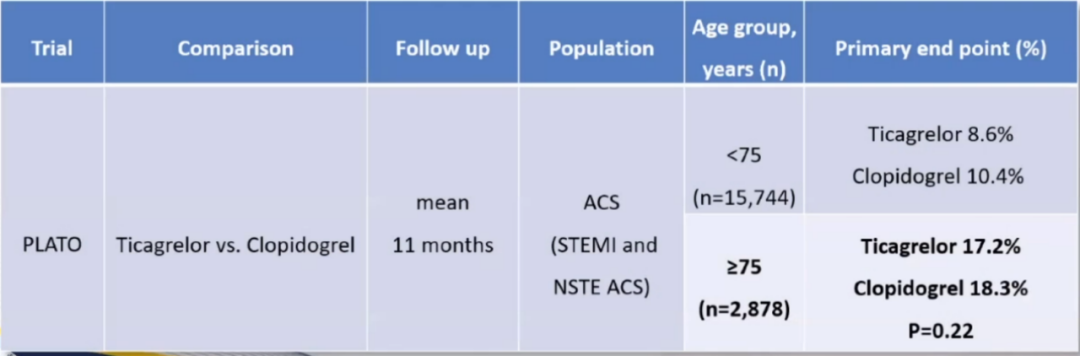
2009年NEJM杂志的PLATO(血小板抑制和患者预后研究)老年亚组显示:在伴或不伴 ST 段抬高的ACS患者中,与服用氯吡格雷的患者相比,服用替格瑞洛患者未显著降低心血管死亡、心肌梗死和卒中的风险。
2016年Int J Cardiol杂志的KAMIR-NIH(韩国急性心肌梗死登记-国立卫生研究院)研究提示:替格瑞洛在高龄患者中的大出血风险显著高于氯吡格雷,尤其在≥75岁患者中的TIMI大出血风险显著升高。研究统计了2011 年 11 月至 2015 年 6 月期间 8010 名成功进行血运重建的患者(1377 名患者服用替格瑞洛,6633 名患者服用氯吡格雷),排除停用或院内在两种抗血小板药物之间转换的患者。
聂教授最后强调,我们要关注老年人群的诸多出血高危因素,注重临床评估。基于出血风险评估,制定个体化抗栓治疗策略,这样才能实现抗栓治疗的最大获益,从而减少患者不良事件,尤其是出血并发症。
