候静波教授:ECMO支持下危重冠心病患者的介入治疗(上)
自2022年2月,哈尔滨医科大学附属第二医院(简称哈医大二院)心血管内科单中心ECMO团队开展ECMO手术302例,其中冠脉ECMO 296例,死亡12例,成功率95.3%,对于ECMO支持的危重冠心病患者介入治疗积累了丰富的经验。候静波教授代表中心在龙江会上就“ECMO支持下危重冠心病患者的介入治疗”作汇报。关于ECMO辅助下的CHIP经验,她在汇报中总结了两点:1.大部分CHIP-ECMO 手术结束即撤除ECMO,降低局部血管并发症及对左心功能影响,必要时撤除ECMO,改为IABP辅助;2.术中根据患者血压及血氧饱和度调整ECMO支持流量,起始1.5L左右,血流动力学变化较大时可加到3.0L左右。

候教授在授课伊始说道,实际上危重冠心病患者主要是指CHIP(复杂高危有指征)患者,对于CHIP患者是否需要进行PCI手术,需要术者权衡风险和获益孰轻孰重。如果患者风险较高,而获益不多时,就没有必要冒着高风险去完成PCI手术;但如果一旦疏通患者血管获益较大,那有风险也是值得的。
当然,危重患者的治疗,需要一定的器械支持。在2014年JACC杂志发表的研究中可以看到,2007年前后短期内应用MCS(机械循环辅助)模式发生了很大的转变,从之前的经皮切开缝合到经皮穿刺,而且器械支持的理念是早上早撤,避免靶器官多器官的损害。
该项研究分析了 2004 年至 2011 年在美国接受短期 MCS 的所有成年患者。结果发现从 2007 年到 2011 年,用于短期 MCS 的经皮装置使用增加了 1511%,而非经皮装置增加了 101%。死亡率在此期间下降(p = 0.027),从 2004 年至 2007 年的 41.1% 下降到 2008 年至 2011 年的 33.4%。心源性休克患者亚群也观察到类似的趋势,从 51.6% 下降至 43.1%(p = 0.012)。在此期间,医院成本也有所下降(p = 0.011)。多变量分析显示球囊反搏(OR:2.00;95% CI:1.58 至 2.52)、凝血病(OR:2.35;95% CI:1.88 至 2.94)和心肺复苏(OR:3.50;95% CI:2.20 至 5.57)在短期 MCS 之前是最重要的死亡率预测因子之一。
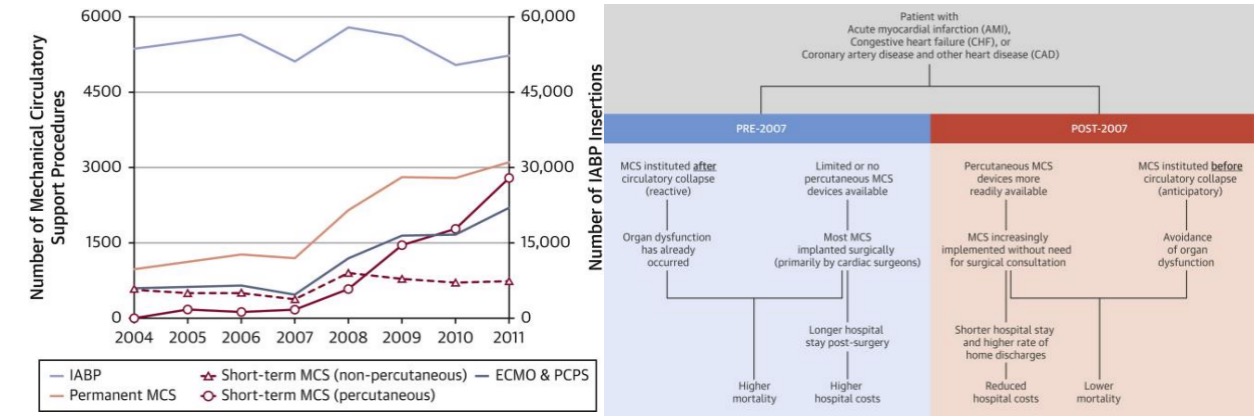
从器械支持来说,常用的机械辅助循环由弱到强依次包括IABP(主动脉内球囊反搏)、IMPELLA、TANDEMHEART和VA-ECMO(静脉-动脉体外膜肺氧合)。候教授也主要就ECMO做详细介绍,ECMO作为危重症冠心病患者的首选MCS器械支持,横跨范围从1-2L一直到5-7L,具体可以根据患者心脏指数来调节。若术中心脏停跳,ECMO可以升高流量;若不需要它还可以降低流量。综合来说,ECMO是一种相对简单的可调整需要支持力度的辅助器械,这一点对于术中的维护是不可或缺的。
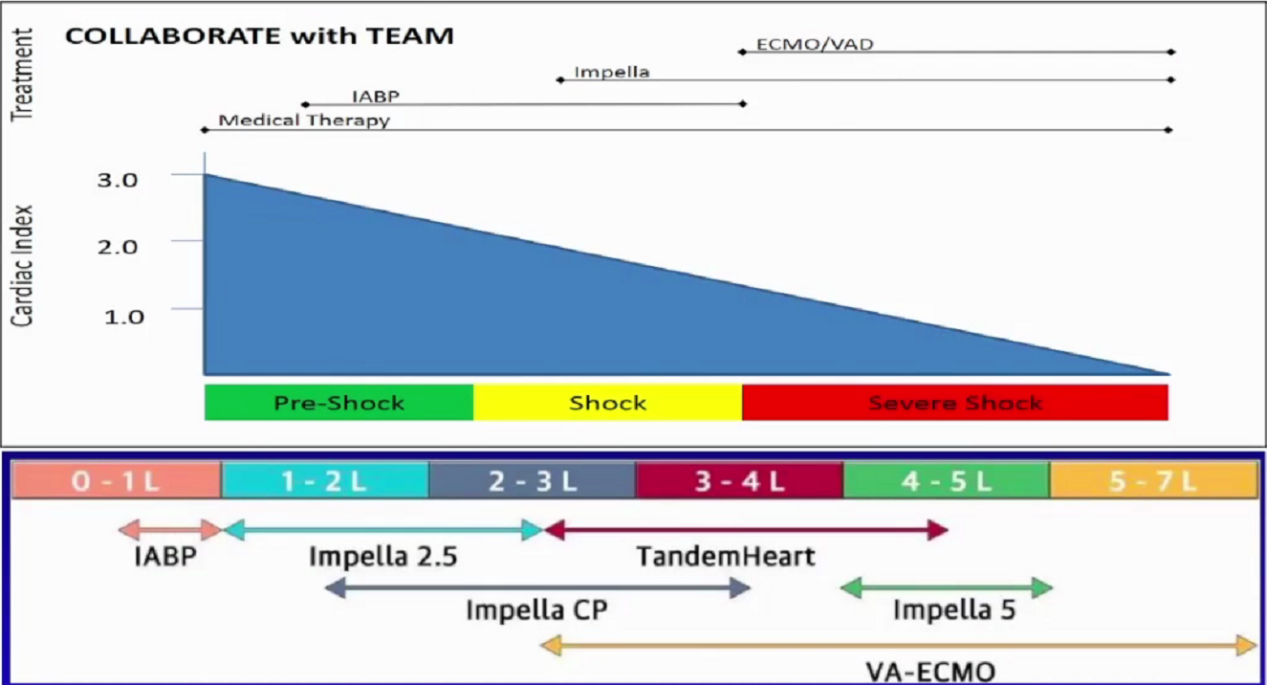
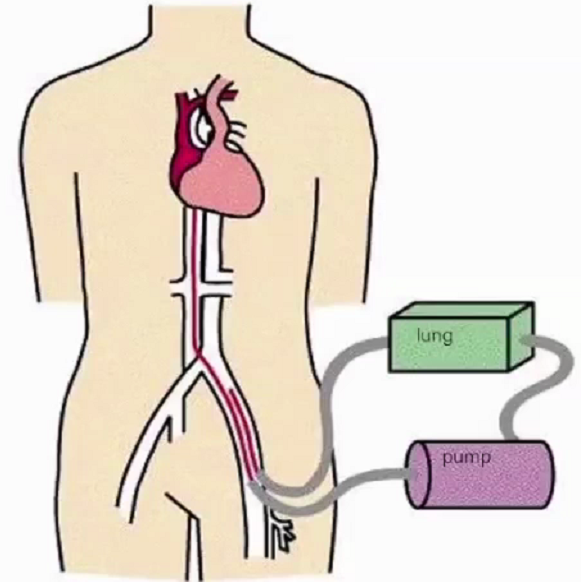
泵(人工心脏)将静脉血引至体外,通过膜肺(人工肺)气体交换,然后动脉血输回患者体内。在病人自身心肺循环通路上并联了一套人工心肺辅助装置。ECMO降低了患者右心室前负荷,进而减低左心室前负荷,使受损的心肌得到休息,改善心功能;它还可以有效替代心肺功能,保证全身组织器官氧合和血流动力学平稳(严重心脏衰竭、恶性心律失常、心跳骤停等)。

VA-ECMO 的生理状态包括以下四个方面:1.心肺转流:右心室前负荷降低,肺血流降低,搏动血流降低。2.全身灌注增加:心脏输出量+泵输出量。3.灌注的不均衡:动脉插管位置决定;异向血流,交接平面;局部灌注不足(下肢远端)。4.心室后负荷增加:心室扩张。
ECMO的循证医学证据。目前来说,临床还缺少ECMO相关的RCT观察性研究。2016年Intensive Care Med杂志的一项队列研究进行了系统回顾和荟萃分析,比较了在难治性心脏骤停和心源性休克并发急性心肌梗死的情况下接受和不接受ECMO支持治疗患者的死亡率。其中关于机械循环辅助下的CHIP-ECMO患者,观察性研究表明ECMO可能降低心源性休克PCI(经皮冠状动脉介入治疗)的死亡率,但是纳入研究及患者数目较少。
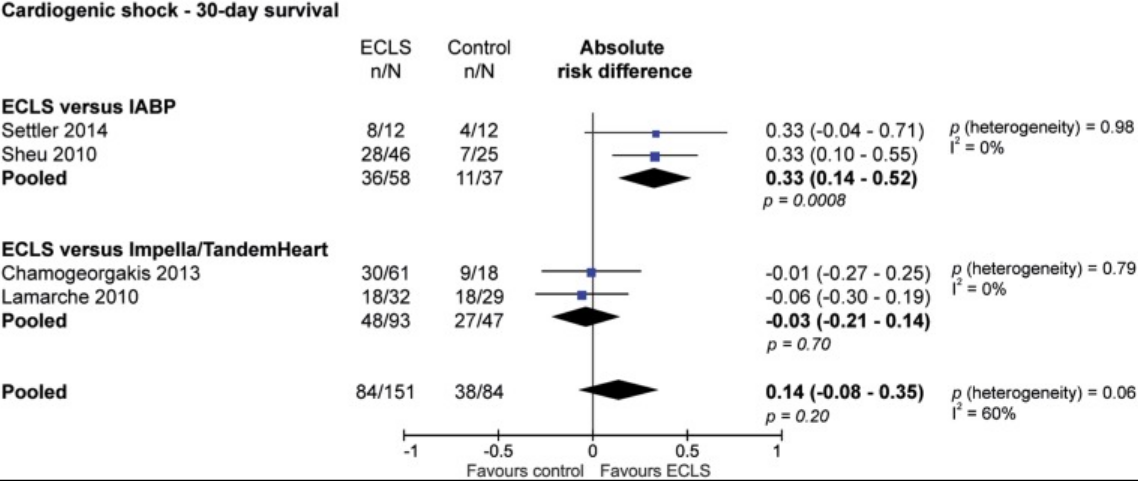
从临床经验来讲,IABP+ECMO才能达到搏动性组织血流灌注最理想的模态。IABP优点是搏动性血流,缺点是辅助流量有限;而ECMO优点是辅助流量充足,缺点是恒流状态,组织灌注差。所以两者相结合的搏动性血流+充足辅助流量,才能使心脏充分卸负荷,达到理想的组织灌注的临床满意结果。
1.心源性休克:急性心肌梗死、急性暴发性心肌炎、心脏术后难治性低心排、急性大面积肺栓塞、慢性心力衰竭急性失代偿、心脏移植术后移植心脏的急性功能障碍、严重心律失常、围术期心肌病、应激性心肌病等。
2.心跳骤停:包括院外心跳骤停和院内心跳骤停(常规CPR无效或不能维持有效的动脉血压而心、脑功能有恢复的可能)。
3.高危PCI。
1.经皮机械循环支持设备使用专家共识声明:对于左主干、多支病变,尤其是不能进行外科手术或射血分数严重降低与心脏充盈压升高的患者,在PCI过程中应考虑包括ECMO在内的植入经皮机械循环辅助设备。(2015)
2.中国经皮冠状动脉介入治疗指南:对于ECMO等辅助装置可降低危重复杂患者PCI病死率,有条件时可选用。(2016)
3.ESC血运重建指南:对ECMO在内的循环辅助设备推荐级别为Ⅱb/C,用于急性冠脉综合征合并心源性休克的短期循环支持。(2018)
此外,提前应用ECMO辅助下行PCI是一种有效的治疗方法:例如无保护左主干病变,完全血运重建,复杂CTO,解剖结构复杂的病变(弥漫病变或严重钙化病变),仅存在单支生命依赖的血管,无复流,以及严重左心室功能不全(LVEF <35%)。
1.充分评估适应证,精细化的管理是成功的关键。
2.重视团队合作,严格无菌。
3.固定的ECMO腿部穿刺小组,建立巡视制度,责任到人,减少血管并发症。
4.早上机,早撤机。
5.密切观察,尽早发现并发症,及时处理。
6.尽量清醒ECMO,降低肺部感染机会,营养保证。
7.确保穿刺质量,置管前超声评估血管,穿刺置管前预埋线。
8.常规放置远端灌注管。
9.监测凝血,肝素化状态下尽量减少有创操作。
ECMO建立。置管型号由之前的根据患者身高体重估测,到超声测量血管直径及评估血管条件。灌注管也由不放灌注管改为常规放置;动静脉置管前穿刺置管;以及ECMO运转后,超声定位穿刺。
ECMO团队—CCU+导管室。建立有效的心内科独立团队包括以下两个团队:
-
介入团队:预充(护士)、穿刺置管、ECMO的连接、撤除ECMO时术区缝合器缝合、冠脉介入PCI治疗。
-
CCU团队:镇静,气管插管,有创呼吸机支持(医生+呼吸治疗师);ECMO运转后的维护(医生+护士)。
候静波教授:ECMO支持下危重冠心病患者的介入治疗(下)
自2022年2月,哈尔滨医科大学附属第二医院(简称哈医大二院)心血管内科单中心ECMO团队开展ECMO手术302例,其中冠脉ECMO 296例,死亡12例,成功率95.3%,对于ECMO支持的危重冠心病患者介入治疗积累了丰富的经验。候静波教授代表中心在龙江会上就“ECMO支持下危重冠心病患者的介入治疗”作汇报。关于ECMO辅助下的CHIP经验,她在汇报中总结了两点:1.大部分CHIP-ECMO 手术结束即撤除ECMO,降低局部血管并发症及对左心功能影响,必要时撤除ECMO,改为IABP辅助;2.术中根据患者血压及血氧饱和度调整ECMO支持流量,起始1.5L左右,血流动力学变化较大时可加到3.0L左右。
以下数据统计了单中心ECMO支持下高危PCI 200例数据,实际总死亡率(300例)不到5.5%,因并发症死亡4例。
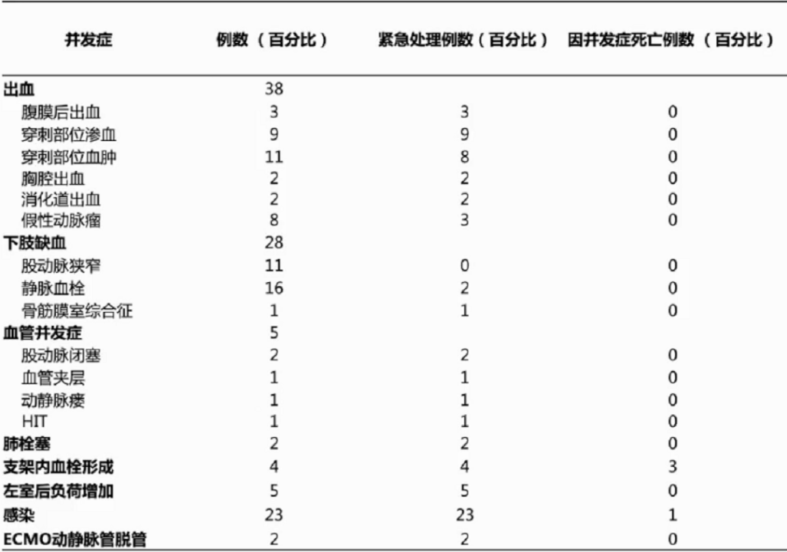
Case 01
男性患者61岁,主诉阵发性胸痛伴呼吸困难1日,加重2小时入院。既往有高血压病史,否认吸烟史。体格检查:血压脉搏测不出,呼吸30次/分,意识模糊,浑身湿冷,口唇发绀,双肺呼吸音粗,可闻及散在干湿啰音。心律齐,心率111次/分,腹部查体不能配合,余查体未见异常。血气分析:pH 6.96,pCO2 46mmHg, pO2 78mmHg,lac>15.0mmol/L,HCO3- 10.3mmol/L,BE -21.6mmol/L,SO2(血红蛋白氧饱和度)84%。CTNI 51.178pg/ml,NTPro-BNP 3264pg/ml,EF 15.8%。给予纠酸,升压,抗休克;抗栓、改善心功能,对症治疗;气管插管,机械通气;IABP或ECMO支持下急诊冠脉介入治疗。
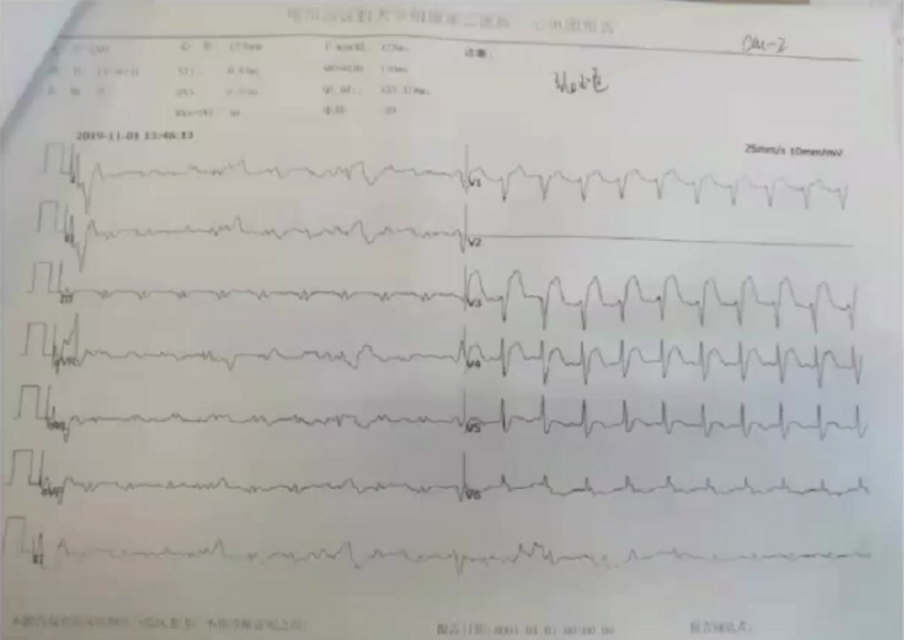
治疗策略:患者右冠次全闭塞,前降支(LAD)闭塞,中间支闭塞,左回旋支(LCX)次全闭塞,心源性休克,应在ECMO及IABP辅助下完全血运重建才有存活可能。
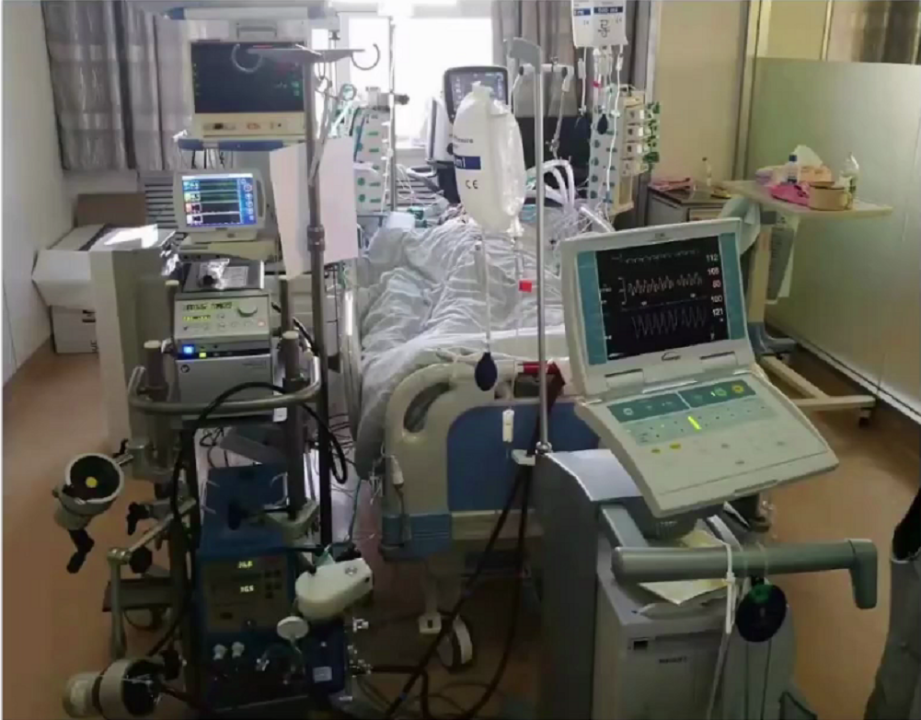
术中在ECMO支持下,右冠脉在最短的时间内先将球囊扩张后植入支架,迅速结束;左冠脉在LAD扩张之后植入支架,最快的速度后扩张;中间支也是开通后植入支架;LCX基本接近闭塞,也植入了一个支架。可以说,四支血管四个支架也是尽可能用最短的时间,最快的速度来开通血管。患者在血管开通之后,心脏收缩明显增强。随后又从患者做手术的左腿植入IABP。术后患者意识镇静,有创机械通气,镇静状态,IABP+ECMO支持,升压药物维持,血压111/55mmHg。术后1小时血气分析:pH 7.57,PCO2 25mmHg,PO2 164mmHg,lac 6.1mmol/L,HCO3- 22.9mmol/L,BE 1.9mmol/L,SO2 100%。

患者入院当天:第5天:第8天的超声变化
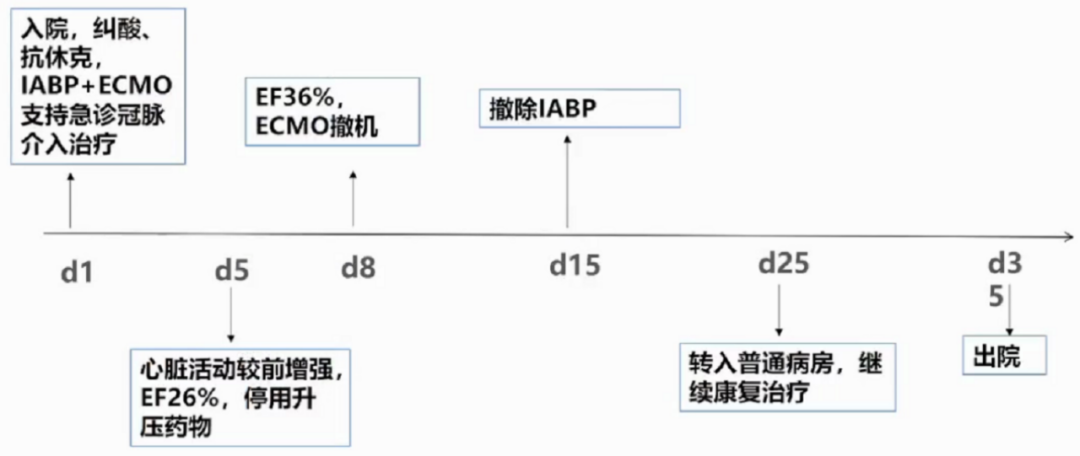
病情转归
经验总结:患者状态危重,急性心肌梗死、心源性休克,死亡风险极高,应用IABP+ECMO联合辅助支持的策略,在保持器官灌注的前提下,开通冠脉,将死亡风险降到最低,一次性处理所有的冠脉问题。
IABP联合ECMO不仅可以保障器官灌注,还可以产生搏动性血流,更接近生理,同时在心功能逐渐恢复时,可以更有效的改善冠脉的血流,促进心脏功能的恢复。
Case 02
男性患者76岁,主诉发作性胸闷胸痛半月入院。现病史:半月前因胸闷胸痛于当地医院行CAG(冠脉造影),提示三支病变,为行进一步治疗来我院。既往史:高血压病20余年,血压控制不佳;糖尿病病史9年,胰岛素治疗。
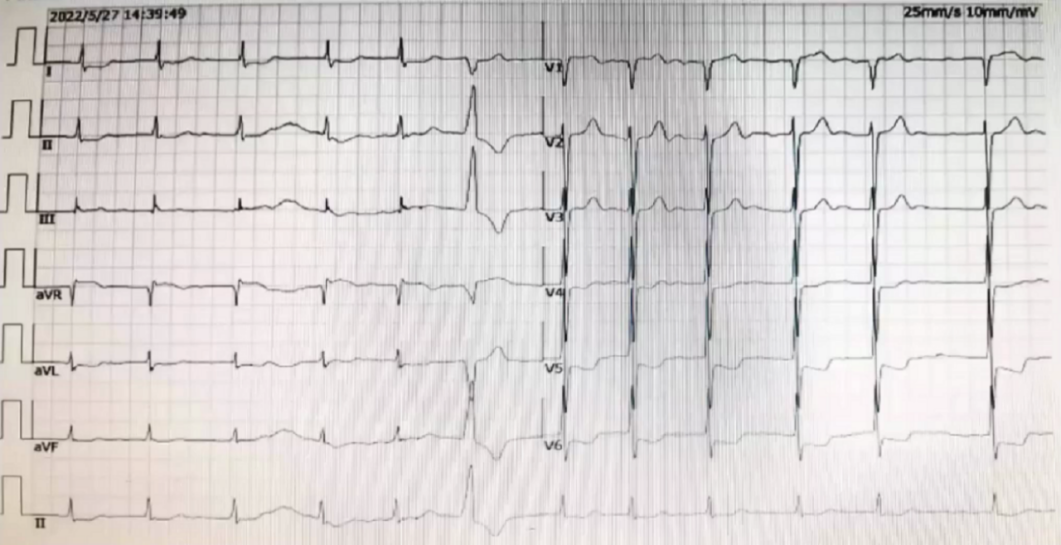
心电图:ST段压低

超声心动图
查体:BP 120/80mmHg,HR76次/分,心律不齐,双肺无啰音,心脏无杂音。化验:TNI、CKMB(-)、BNP 1694ng/L、LDL 1.33mmol/L。
临床诊断:
-
冠心病
不稳定型冠心病
-
心律失常
心房纤颤
-
高血压病
-
糖尿病
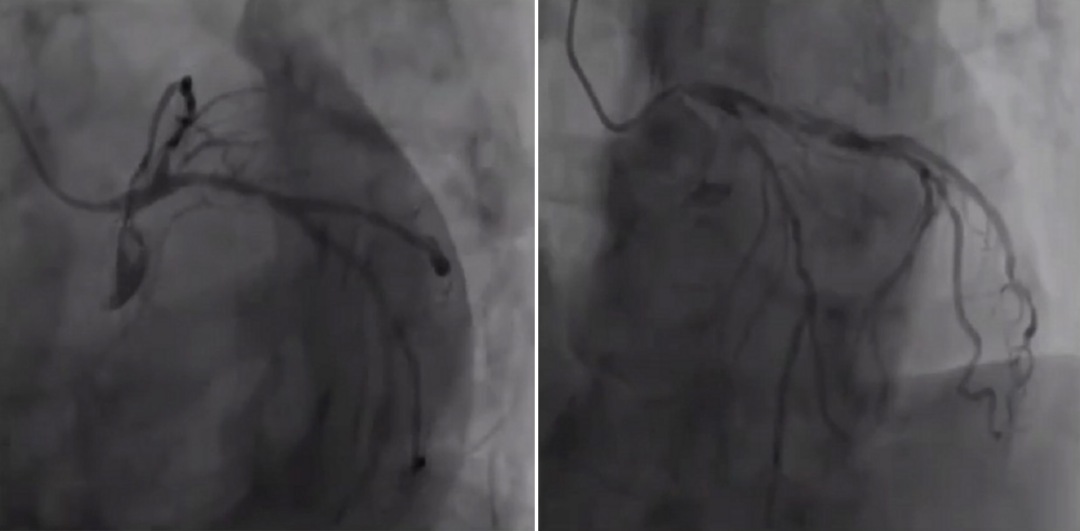
入院前当地医院CAG:LCX近端90%,LAD 95%,LAD钙化严重。
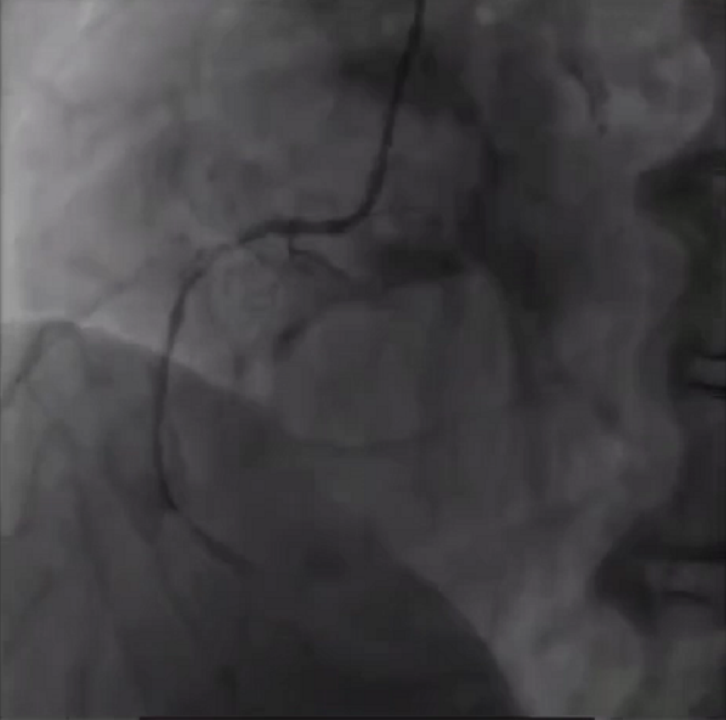
右冠脉次全,钙化严重
处理策略:患者三支病变,钙化重,当地医院已建议CABG或转上级医院PCI。考虑到患者比较抵触CABG(冠状动脉旁路移植术),遂选择PCI手术,分次处理,先右冠后左冠,并且做好旋磨准备。
CAG过程:
1.造影后发现血压快速呈直线下降,多巴胺、肾上腺素,无效。
2.患者出现呼吸困难,SaO2 82%,立即气管插管!
3.喉头水肿,插管困难,反复尝试,最终插管成功,历时7分钟!
4.心率减慢,40次/分,交界部逸博,胸外按压,有创呼吸机及大量升压药下HR 92次/,BP 46/33mmHg,SaO2 61%,9:33决定启动ECMO,9:46ECMO置入完成
5.期间间断胸外按压,多次除颤。
患者ECMO后HR 110次/分,BP 127/95mmHg,Sa0 97%。此时已不能再用造影剂,只能在当地CAG的指导下,行右冠脉PCI手术,导丝从P50升级到P150一直到P200,通过导丝后扩开行IVUS指导。IVUS选择近参和远参。
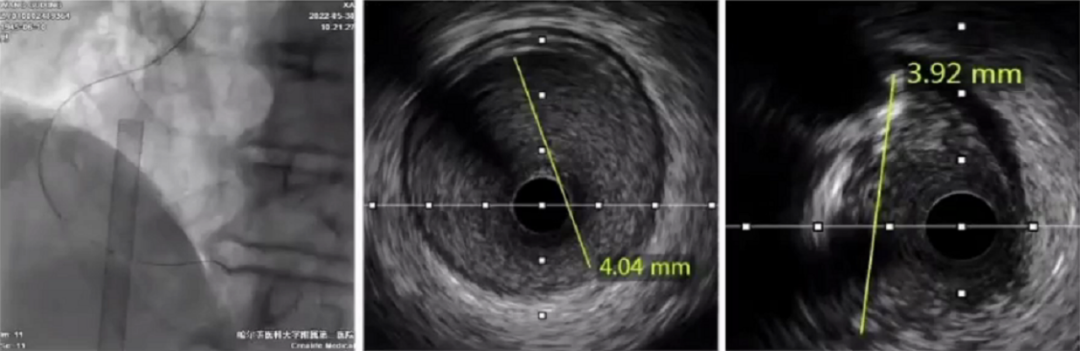
植入两枚支架:3.5*33支架2枚,4.0*19支架。
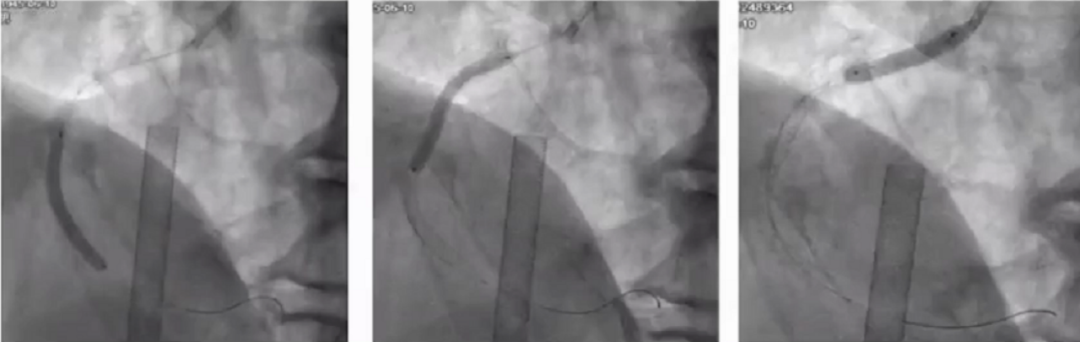
LCX相对简单好处理一些,导丝通过后,由于有大的钝缘支所以送了两根导丝,在IVUS检测近参和远参之后,植入了一枚3.0*33支架,3.0、3.5球囊后扩张。
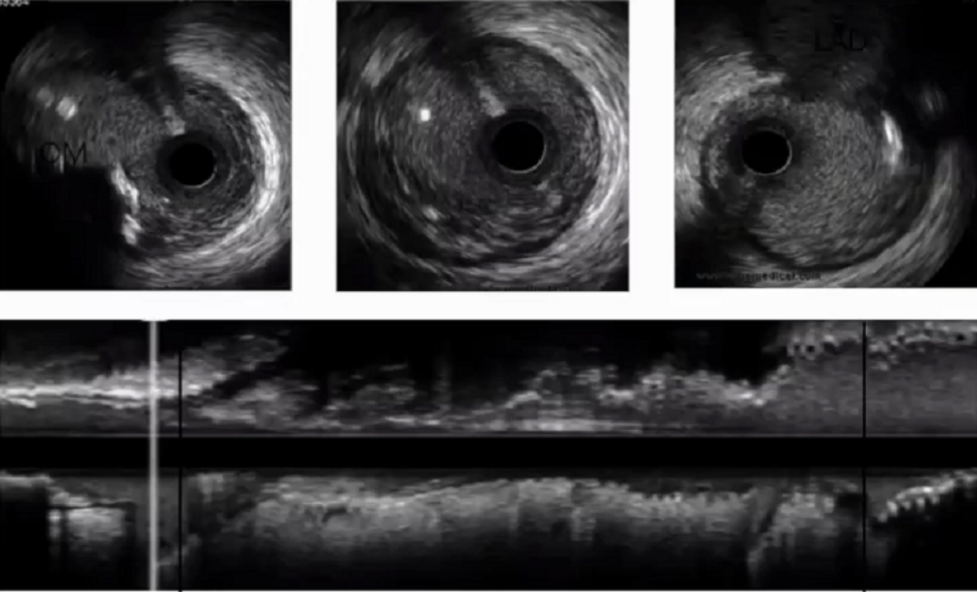
LAD相对困难,导丝很难通过较大的钙化成角的弯,最终在IVUS指导下艰难通过。随后植入2.5*33,3.0*24的支架。
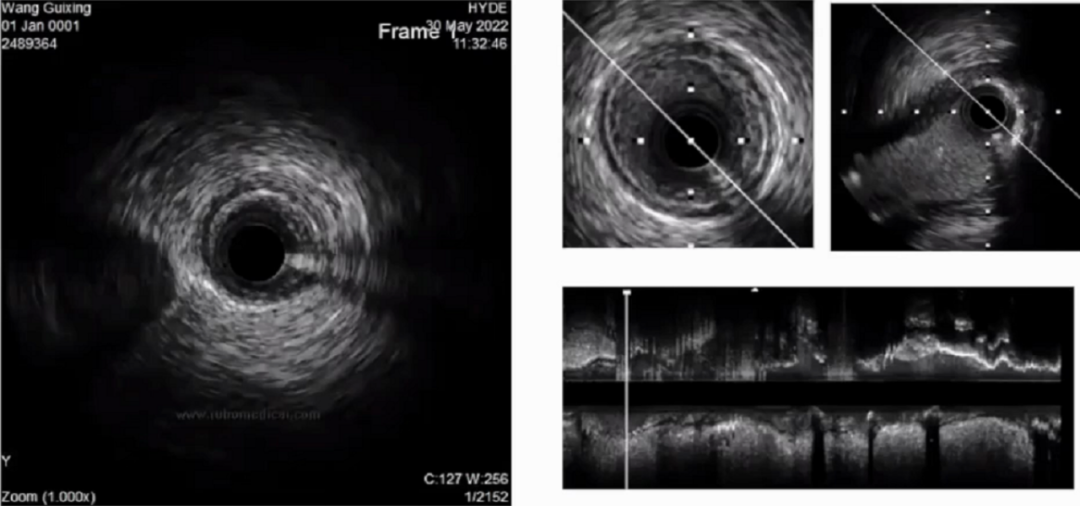
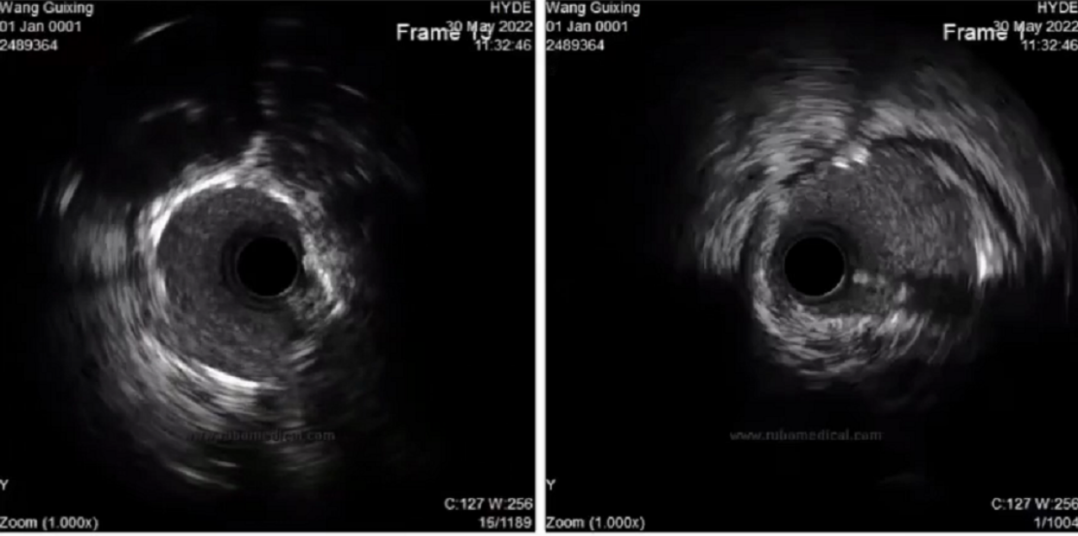
根据IVUS结果示基本上是“V”支架,3.5后扩张球囊完成对吻。最终IVUS结果较满意。术后2小时,患者清醒,血流动力学稳定,撤除ECMO及气管插管。
Case 03
82岁女性患者,主诉发作性胸闷胸痛1月余,加重3天入院。既往史:高血压病50余年,血压控制不佳。
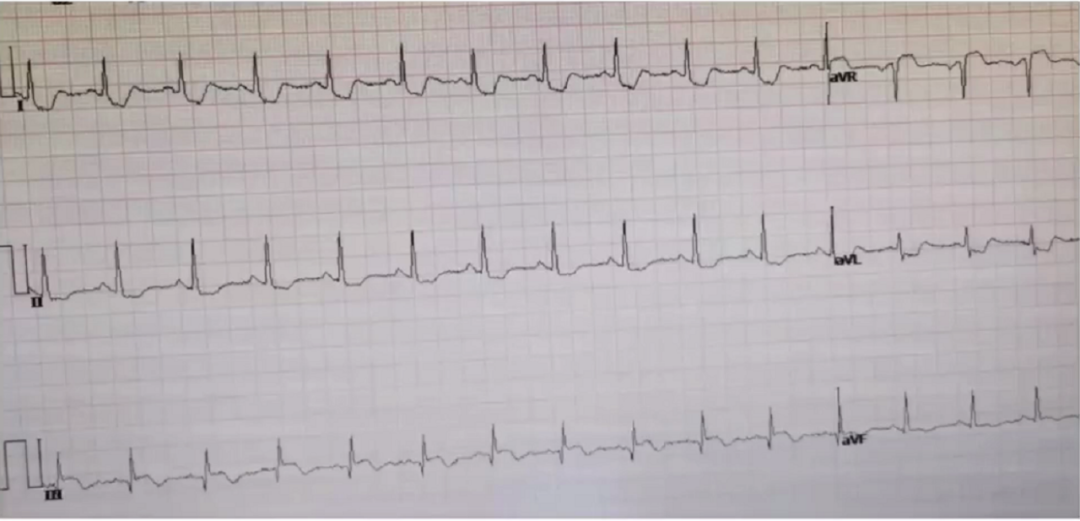
心电图:ST段压低明显,avR导联抬高。

超声:EF值37%
查体:BP 60-70/45mmHg,HR 110次/分,心律齐,双肺啰音,心脏无杂音
诊断:
-
冠心病
急性非ST段抬高型心肌梗死
-
心源性休克
-
心力衰竭
心功能Ⅳ级
-
高血压病
CAG显示LAD狭窄,还伴有瘤样扩张,成角钙化;LXC很小但闭塞;右冠脉较大,接近第二转折闭塞,严重钙化成角一直延展到三叉。术中在ECMO辅助后,先开通右冠脉但是过程也比较艰辛,从XT-R到Gaia1到Gaia3,升级到Pilot200到C-pro到最硬导丝Cp8-20,在通过第二转折后降级到Gaia3终于到达远段血管。但所有球囊在闭塞的近端不能通过,尝试GZ-1.0/1.2/1.25后依然不能通过。团队考虑到患者ECMO支持,把流量增加到4.0L,左冠脉后扩张后迅速植入支架。在LAD完成后,继续对右冠脉进行激光消蚀处理,最终球囊可以通过,右冠脉较大,随后又进行了旋磨。最终结果良好。
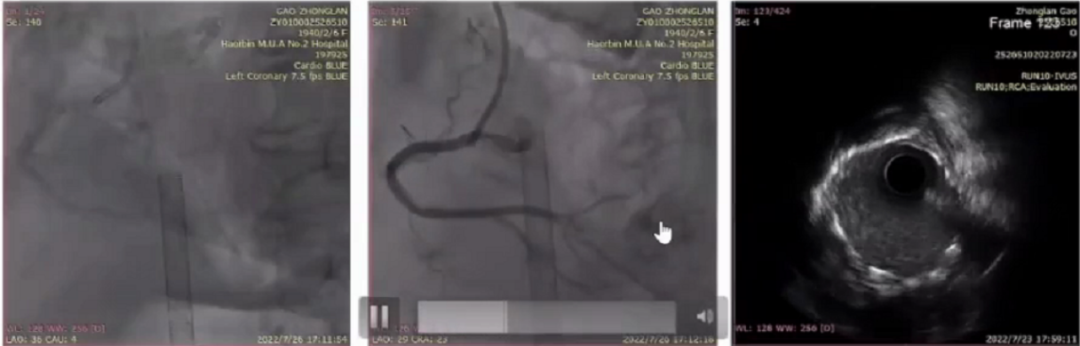
Case 04
患者主因“阵发性胸闷、胸痛不适9天”入院。入院诊断:冠状动脉粥样硬化性心脏病、急性下壁心肌梗死、高血压病3级(极高危)、2型糖尿病。入院后予降压、降糖、抗血小板,降脂,改善循环,纠正心功能对症治疗。建议冠脉介入检查,必要时进一步介入治疗。
CAG显示左主干严重钙化,狭窄85%,前降支弥漫狭窄90%,回旋支开口钙化、闭塞。
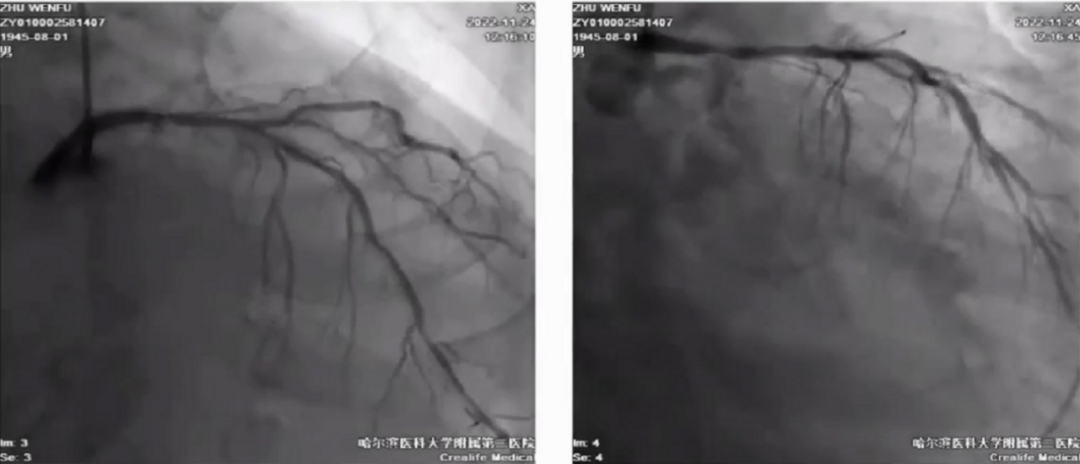
右冠弥漫钙化狭窄,开口狭窄80%,中段90%,远端次全闭塞,钙化、成角。
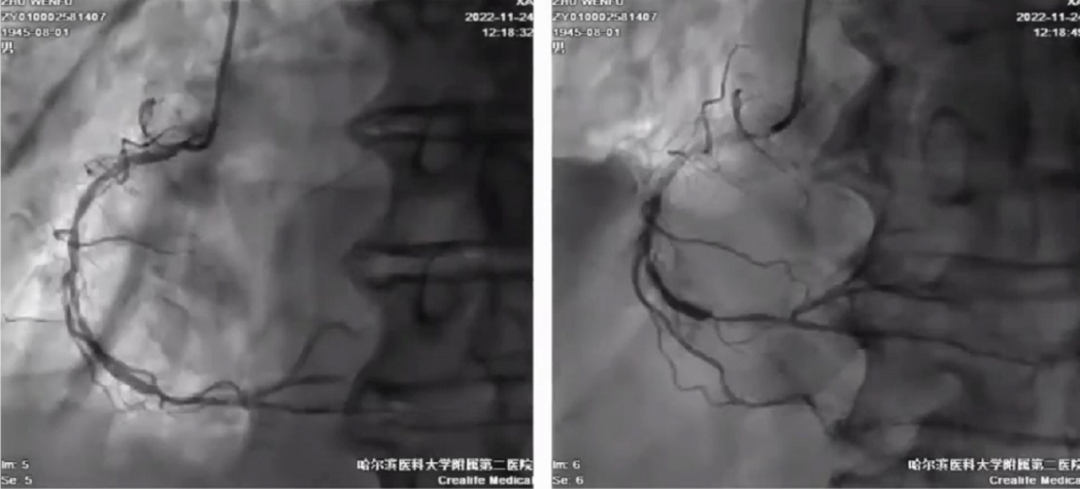
最终策略:ECMO支持下行介入治疗,放弃回旋支。右侧股动脉超声检查重度狭窄,血流不佳,选择左侧入路。
术中左室后支导丝无法进入,考虑钙化严重所致,球囊无法通过远端钙化狭窄处。准备旋磨但微导管在三叉无法通过狭窄处,不能交换旋磨导丝,血流尚可。遂选择激光消蚀术,由近及远,消蚀导管艰难前行,但到第二转折后通过困难,将近端扩张后又应用延长导管送消蚀导管至远端。通过耐心、多次消蚀,消蚀后1.0小球囊顶住病变处扩张,扩张后造影更换2.0球囊,但预扩大球囊不能返回,再次尝试保护分支,撤回系统后重新进入导丝。由于导丝无法进入,放弃保护,启动旋磨1.25旋磨头180000转速。旋磨后输送球囊顺畅、无阻,继续扩张。为达到更好的效果,积极使用SHOCKWAVE球囊2.5X12,多次扩张。造影后血流通畅,再次尝试分支保护。高压扩张,IVUS检查钙化环打开后,在右冠脉植入三枚支架。
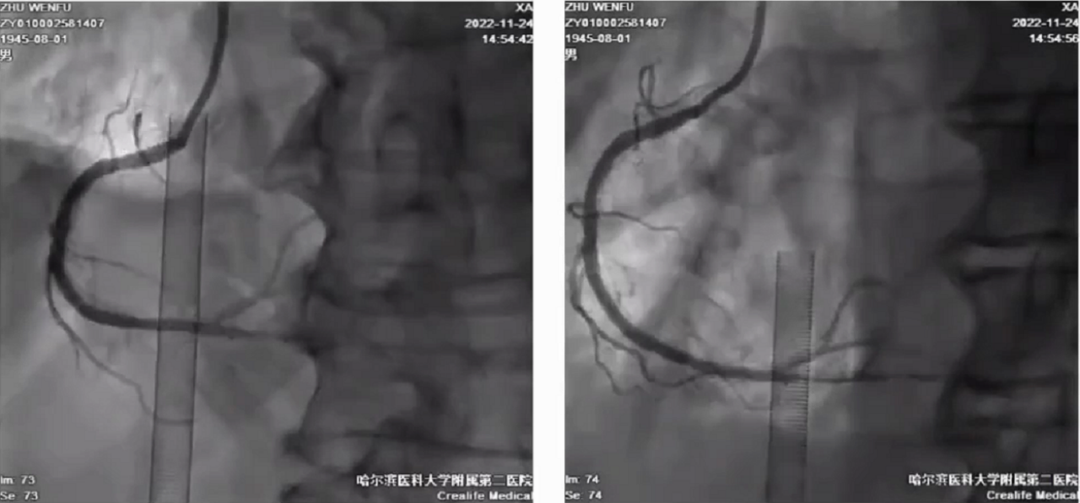
右冠脉最终造影
处理左侧血管,7F指引导管,分支保护,IVUS检查。IVUS导管通过困难,1.5mm球囊不能通过。IVUS显示钙化结节、环形钙化。
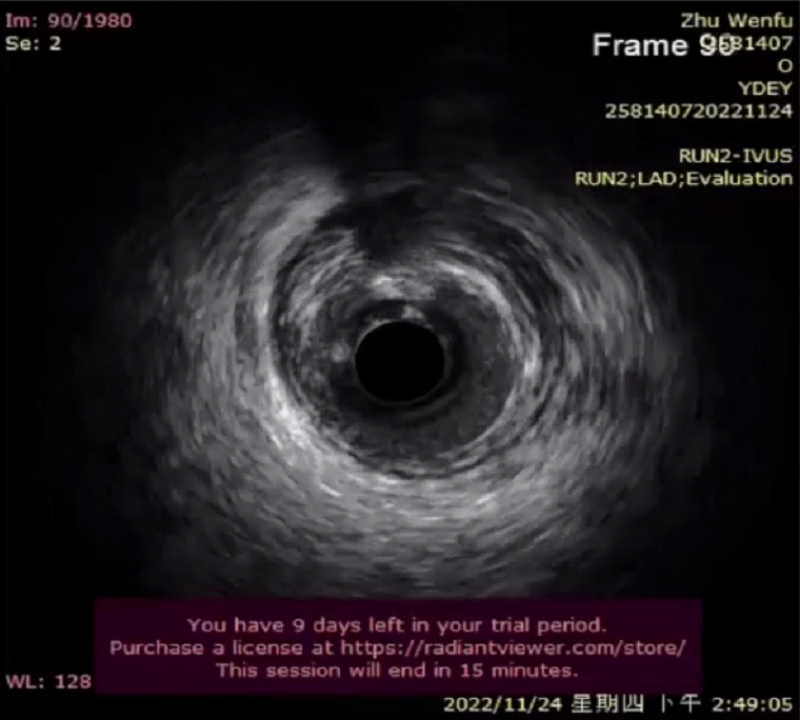
血流通畅,启动旋磨1.5旋磨头180000转速。旋磨后2.5球囊后扩张,远端有夹层又对远端植入支架,继续高压扩张。但近端IVUS检查,钙化仍很严重。为达到更好的效果,积极使用SHOCKWAVE球囊2.5X12,多次扩张,随后钙化明显减轻,可见撕裂。
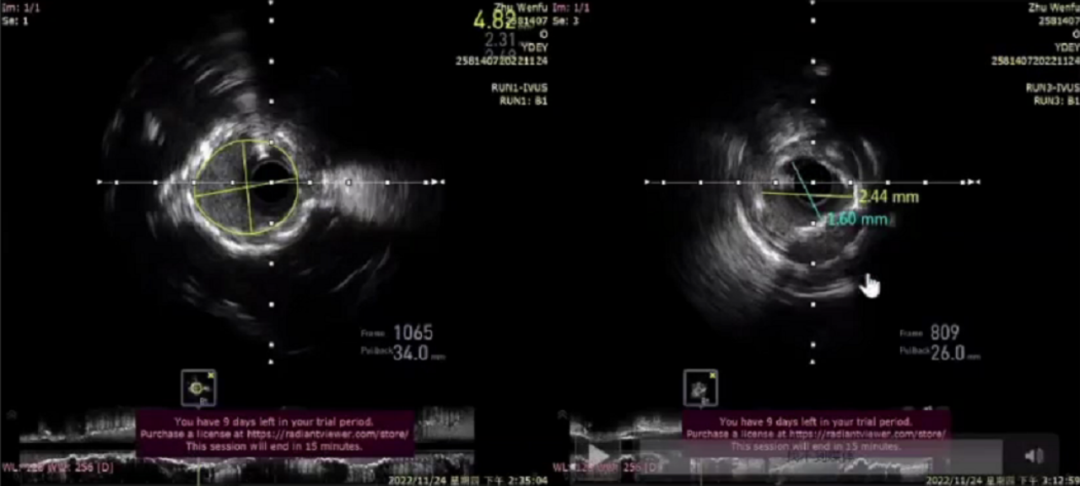
SHOCKWAVE球囊前后对比
之后再顺序植入支架,高压球囊充分后扩张。给予硝酸甘油后行IVUS检查和冠脉造影。最终结果良好。
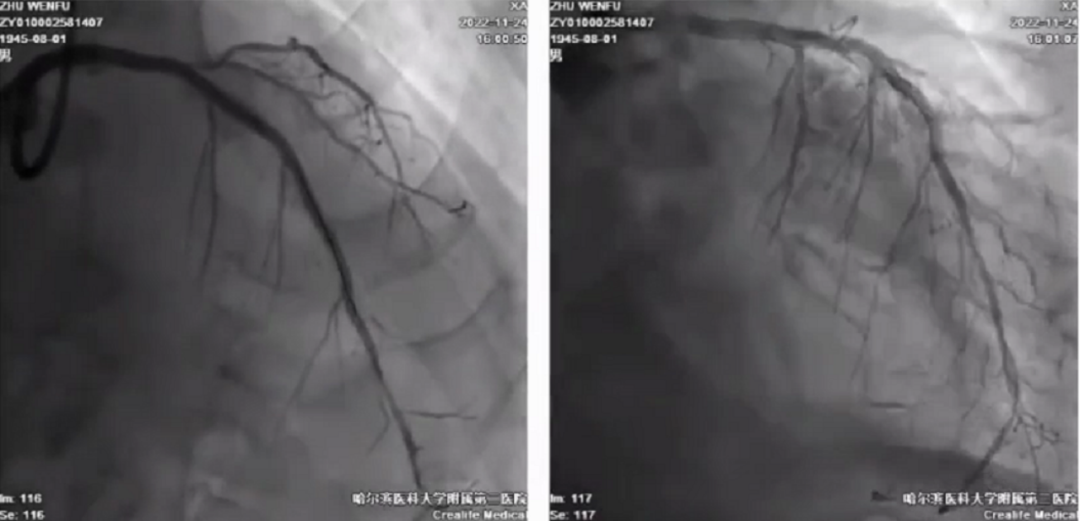
临床上对于上述四个危重病例的处理,若没有ECMO支持,基本很难开展救治手术,对于医生而言属于半放弃的状态。由此可见,ECMO在危重症患者的诊疗中具有重大的作用和价值。
1.机械辅助装置为重症冠心病患者(尤其是心肌梗死、缺血性心肌病)的治疗提供重要保障。
2.充分理解各种装置的原理,结合患者血流动力学特点和术者经验,合理为病人选择机械辅助装置。
3.机械辅助装置对临床预后的影响,仍需要进一步研究。