

经导管肺动脉瓣置换术(TPVR),又称经皮肺动脉瓣置入术( PPVI),具有创伤小、安全性高、术后恢复快等优势,可替代外科肺动脉瓣置换。我国自2013年完成首例TPVR以来,多个中心已陆续开展,在技术规范、器械创新等层面均取得了创新和进展。中国医学科学院阜外医院张戈军教授擅长各种复杂先天性心脏病的介入治疗以及各种经导管瓣膜植入技术及修复技术。在今年的中国结构周上,张教授以“经导管肺动脉瓣置换术的应用现状及展望”为题,报告了TPVR技术的发展历程以及我国在该领域取得的进展,并提出展望。

1.全球首例TPVR
经导管肺动脉瓣置换术(TPVR),于2000年,Philipp Bonhoeffer医生团队首次报道,是首例应用于临床的经导管瓣膜置换技术,主要被用于治疗紫绀型先心病外科术后并发右室流出道功能不全患者(狭窄或反流)。
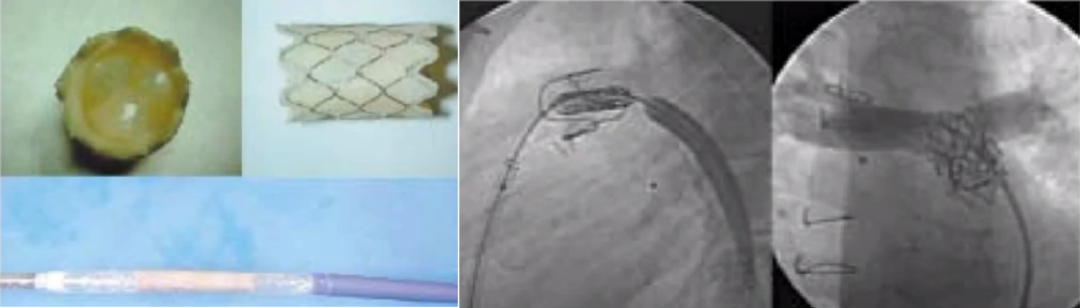
2.Melody valve
Philipp Bonhoeffer医生发明的器械经过改良,进一步发展为Melody瓣膜,是第一款上市的商业化瓣膜。
-
球囊扩张式瓣膜:牛颈静脉+可扩张CP支架;
-
两种尺寸:16mm(可扩张到20mm)、18mm(可扩张到24mm);
-
主要用于右室流出道外管道或肺动脉生物瓣衰败的患者。
Melody瓣膜术后10年随访显示良好的瓣膜耐久性和临床预后:
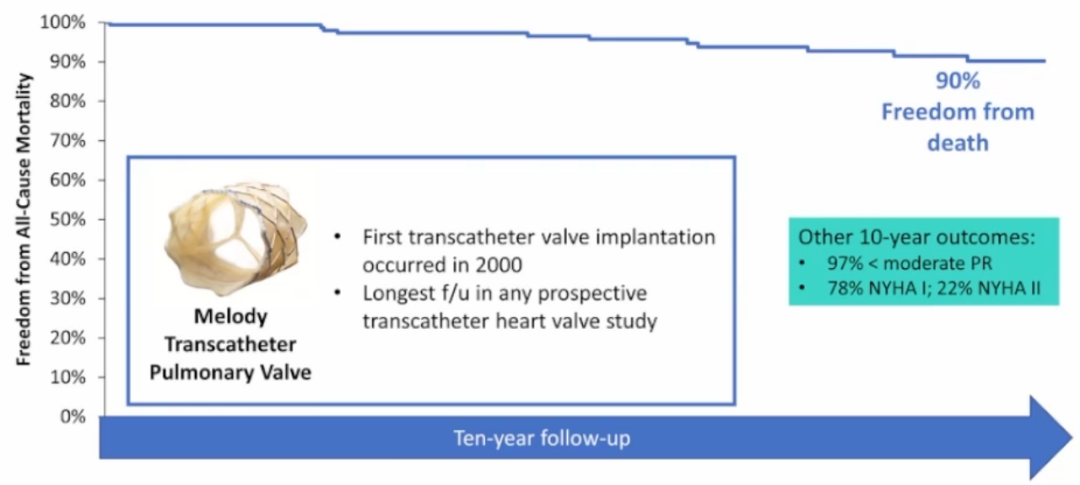
2022年发表在《Circulation: Cardiovascular Interventions》上的一篇报道显示,Melody瓣膜10年随访显示53%的患者未出现瓣膜功能不全,79%未再次介入或外科干预。
2020年报道的由慕尼黑心脏中心进行的一项研究,经过长达12年的随访,对经导管Melody瓣膜植入与外科手术长期效果比较,结果显示,经导管Melody瓣膜植入在生存率、再次干预率与外科手术类似。由于侵入性较小,认为TPVR应被视为治疗右心室流出道功能障碍患者的一种方法。
基于以上研究,2020年欧洲心脏病协会、ACC都将Melody瓣膜用于解剖形态适合的患者可以作为一类适应证推荐。
3.Sapien valve
-
球囊扩张式瓣膜:20mm,23mm,26mm,29mm;
-
2016年获得FDA批准用于肺动脉瓣位;
-
可以用于流出道直径达29-30mm的患者;
-
支架断裂风险低,可以不需要预支架植入;
-
Commander输送系统能实现更精准的锚定。
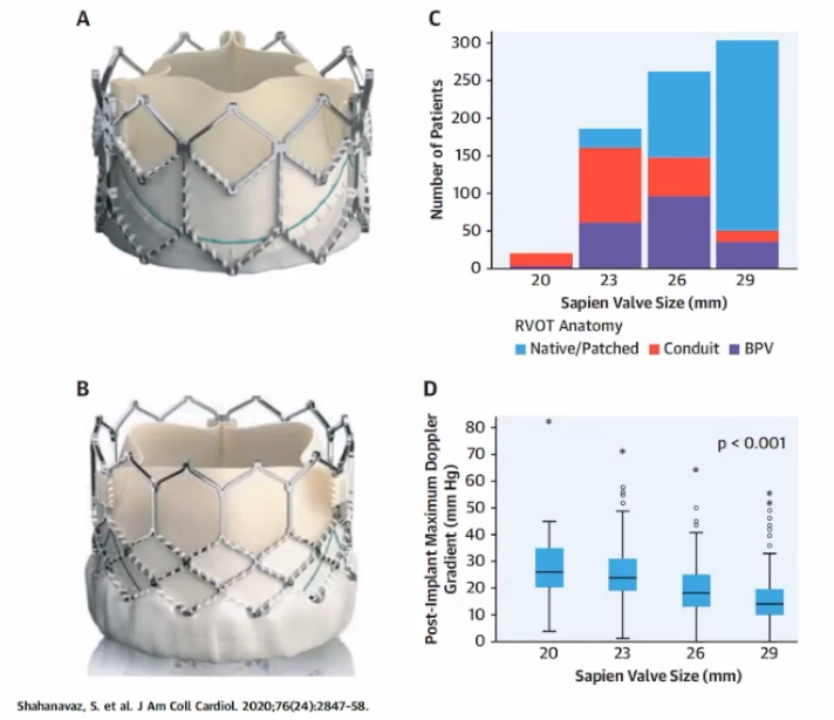
为适应更大的流出道结构,自膨式肺动脉瓣发展起来。
1.Harmony(Medtronic)
该瓣膜几乎是与我国自膨式瓣膜处于同期发展。
-
自膨式肺动脉瓣设计:牛心包瓣膜;
-
TPV22, TPV25;
-
早期临床试验(2017)显示植入后血流动力学表现良好;
-
术中1名患者因瓣膜移位行急诊开胸手术。

(1)早期随访中1名患者因支架断裂(type ll)行外科开胸手术
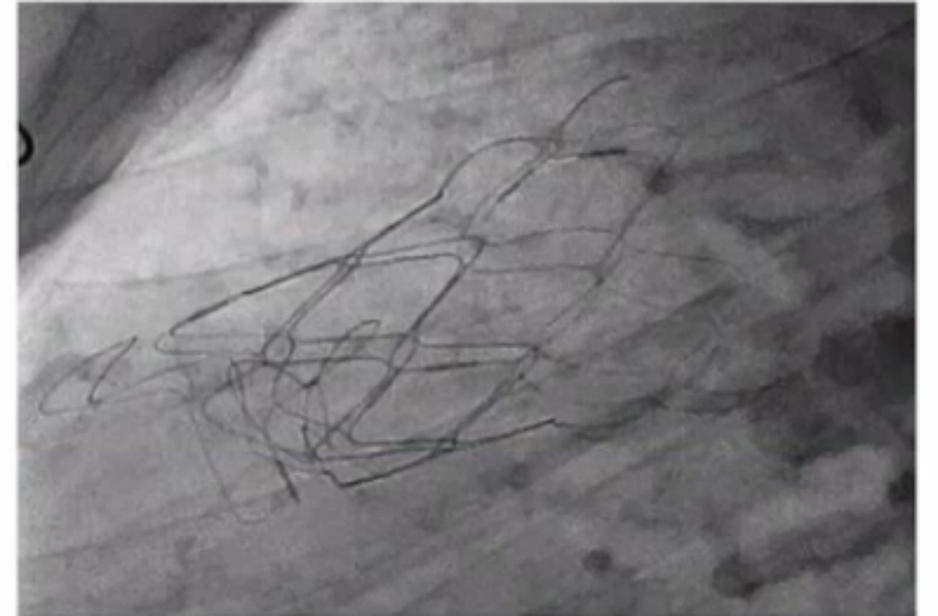
(2)5年随访显示预后良好
1例死亡:不能确定与TPVR的相关性,3年随访瓣膜功能正常。
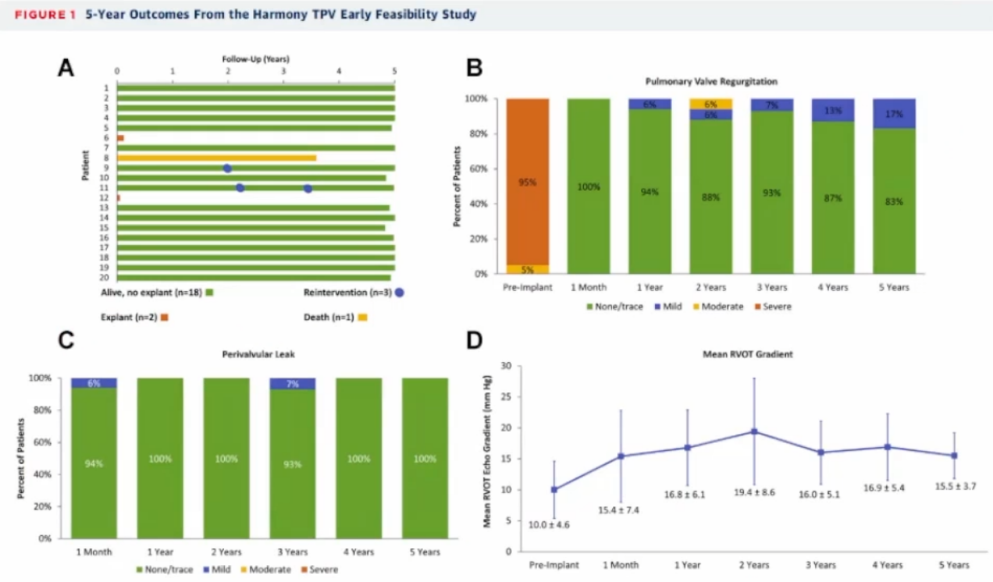
(3)FDA批准上市后的IDE队列随访结果
88.3%的患者术后6个月随访显示瓣膜功能正常且未进行再次干预。但后来发现有相当一部分患者在围手术期或术后早期出现心律失常,术后室性心律失常为主要的器械相关不良事件:室性心动过速(17.8%),室性早博(8.4%)。

基于以上因素,这款瓣膜今年被召回,这也可以看出国外相关监管机构对涉及到相对比较年轻患者的器械要求还是很高的。
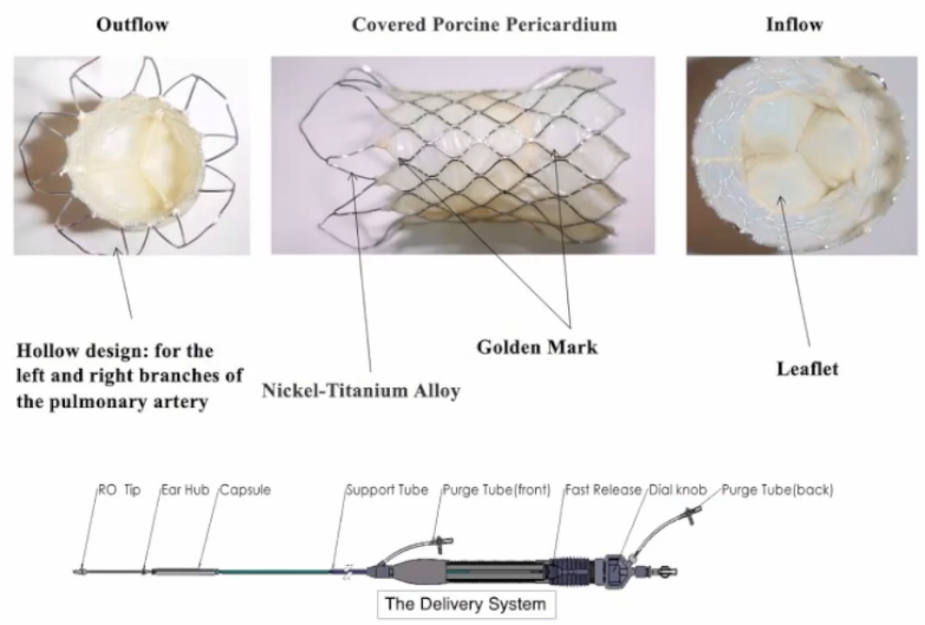
2.Venus-P瓣膜(启明)
-
自膨式肺动脉瓣膜:适用于RVOT结构较大的患者;
-
直径:24mm、26mm、28mm、30mm、32mm、34mm、36mm;
-
长度:25mm、30mm、35mm;
-
输送系统:22Fr、24Fr。
(1)中远期随访显示Venus-P瓣膜具有良好的临床预后
-
多中心临床试验纳入55名重度肺动脉瓣反流患者;
-
5年随访显示仅2.2%(n=1)患者出现中量以上的反流;
-
无跨瓣压差升高的病例;
-
2例患者分别在术后3月和6月死亡;
-
5例患者出现感染性心内膜炎。
(2)8名患者术后出现支架断裂但均为type l型,瓣膜功能无异常
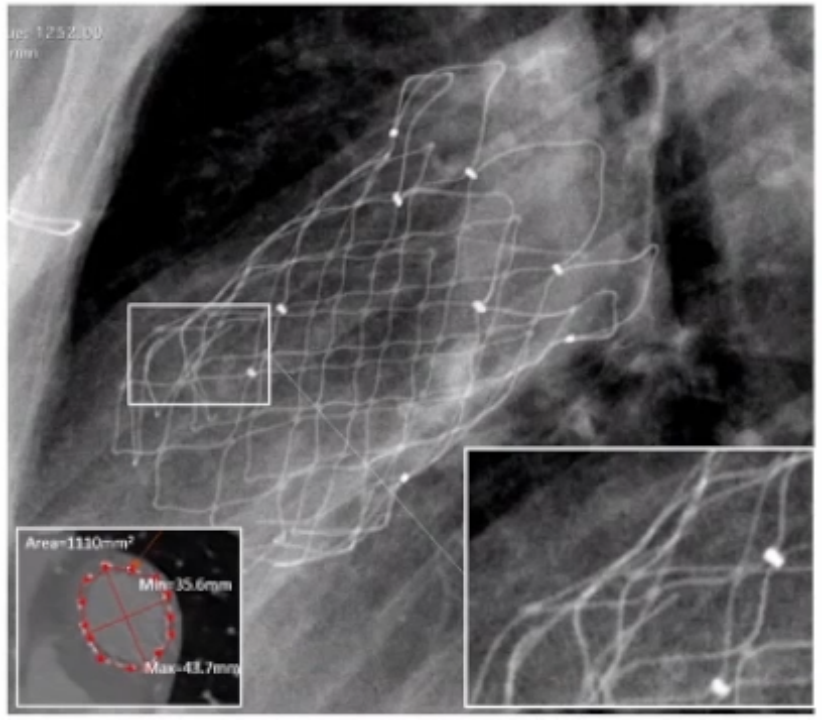
(3)植入形态分析:多数形态良好,严重的支架变形少见
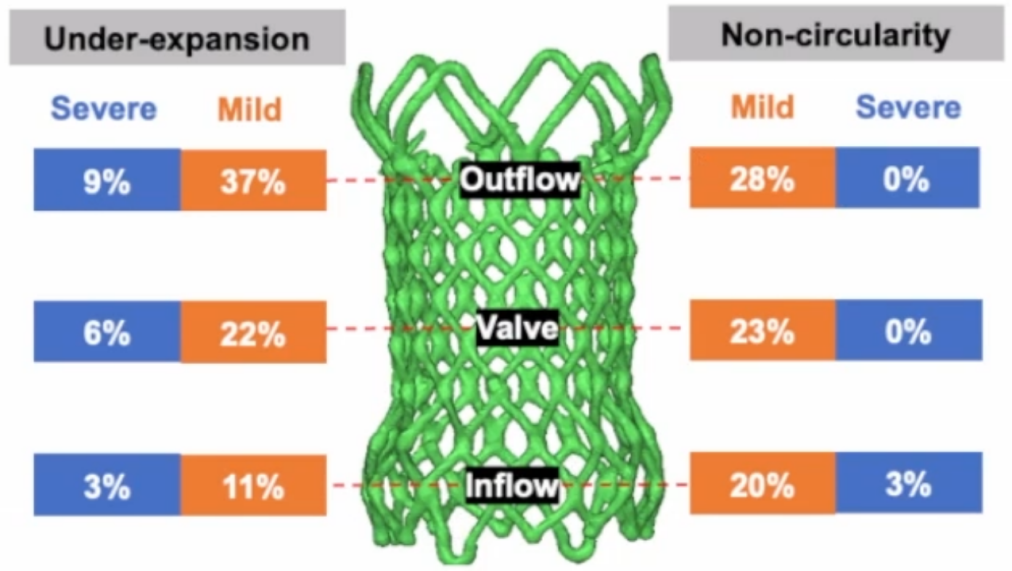
1.Alterra支架
2018年开发了一款经皮置入的Alterra自适应性预置入支架,旨在内部重塑自体RVOT,缩小RVOT直径并产生刚性着陆区。支架为对称的沙漏型设计,除流出端外支架大部分以PET覆膜缝合在支架内表面,流出部网眼为非覆膜,流入和流出直径为40mm,中心直径为27mm,总长度48mm,完全覆膜部分的长度30mm,通过16 Fr eSheath置入自体流出道后搭配29mm Sapian 3瓣膜置入。
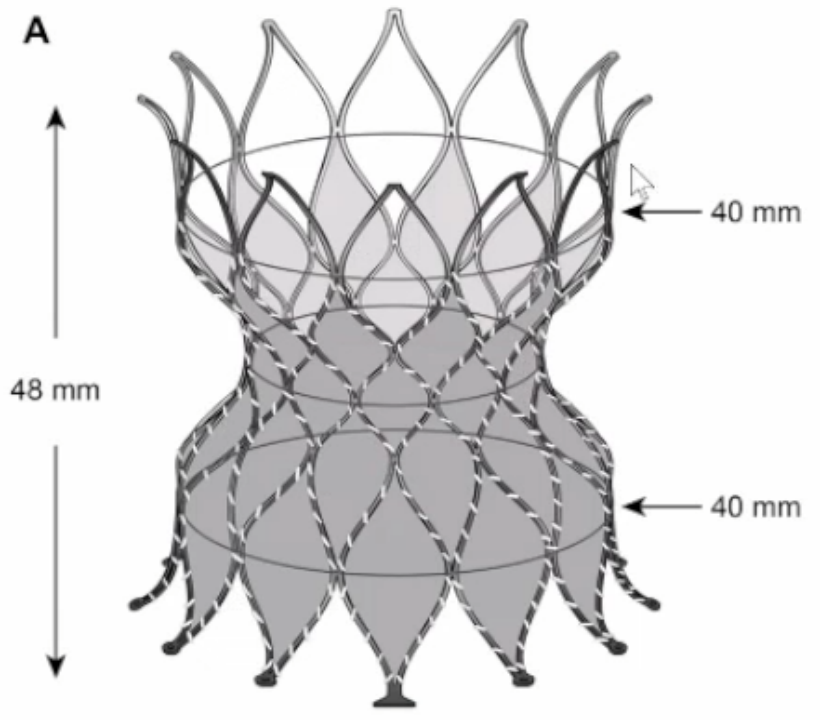
Alterra + S3 for PR:

可能由于器材的外扩式flare设计,Alterra支架植入后有33.3%患者出现器械植入相关的心律失常,因此还需要对该器械风险和获益做进一步评估。
2.分支瓣膜植入
有些术者为了扩大球扩瓣的适应证,把瓣膜植入到两侧肺动脉开口,相当于移动了肺动脉瓣的位置,初期应用证实血流动力学改善和右心室重构。
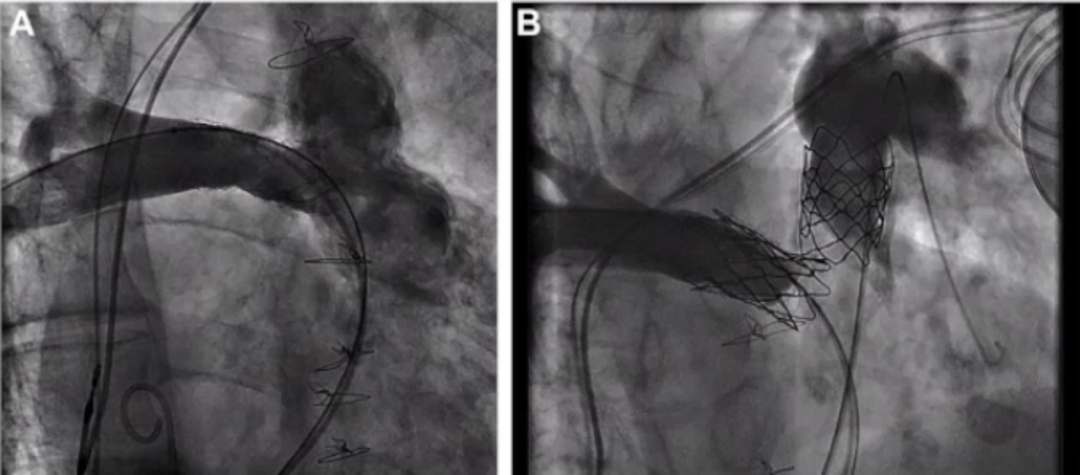
1.稳定的锚定方式
未来临床中,随着自膨胀瓣膜的到来,适应证一定会扩大,尤其我国很多患者做的跨瓣环补片,对于这类患者的锚定方式是一个问题,目前有学者对此进行了研究,尝试通过多种影像学手段评估瓣膜的最佳位点。如通过CT测量模拟植入后的接触范围评价,利用计算机模拟技术计算植入面积。
2.支架断裂(stent fracture)
-
早期Melody瓣膜植入后有着较高的支架断裂率,且与瓣膜早期衰败相关;
-
预置支架植入有效降低瓣膜支架断裂的发生率;
-
Sapien瓣膜未见支架断裂报道;
-
自膨式瓣膜在合并狭窄的患者中SF发生情况仍需进一步研究。
3.感染性心内膜炎
-
在2476名患者的多中心登记数据报道感染性心内膜炎的年发生率为2.2%,56%的患者是金黄色葡萄球菌和草绿色链球菌。
-
多因素回归显示的风险因素包括低年龄、即往感染性心内膜炎病史和残余压差。
-
部分研究提示瓣膜材质(猪心包vs牛心包)影响感染性心内膜炎的发生。
-
强调高风险人群的围术期管理以及患者教育。
4.TPVR最佳手术时机
(1)有症状的重度肺动脉瓣反流或者至少中度的流出道梗阻患者。
(2)对于无症状患者,应满足以下之一(lla,C)
-
运动耐力下降;
-
右室扩张;
-
右室收缩功能异常;
-
狭窄患者右室收缩压大于80mmHg。
未来还需进一步研究影响TPVR术后右心室重构的因素以确认手术的最佳时机。
TPVR经过20年的发展技术已经趋于完善,目前已作为先心病术后右室流出道功能不全人群的首选治疗方式。自膨式肺动脉瓣膜使得结构更大的患者行TPVR成为可能,我国在这方面的发展也处于世界先进水平,但瓣膜的锚定方式和围术期心律失常问题仍需进一步解决。张戈军教授指出,确认手术的最佳时机至关重要,在逆转右室重构的同时尽量减少患者终生干预次数。另外,研发更长耐久性的瓣膜是一个重要的研究发展方向。
