黄从新教授:基于循证数据的心脏脉冲消融技术展望
脉冲电场消融(PFA)技术从2019年在HRS会议上首次亮相后,因其独特的选择性损伤机制备受业内关注。2021年FARAPULSE脉冲电场消融系统作为首个在欧洲上市的PFA系统,积累了大量上市后真实世界数据,2023年8月底该系统首项与传统消融能量(射频、冷冻)对比的随机对照试验ADVENT IDE结果公布[1],因其设计严谨、随访完善,该项研究结果被视作脉冲消融能量临床表现的风向标。此后,随着越来越多循证证据的问世,加速推进了PFA的临床应用与研究。
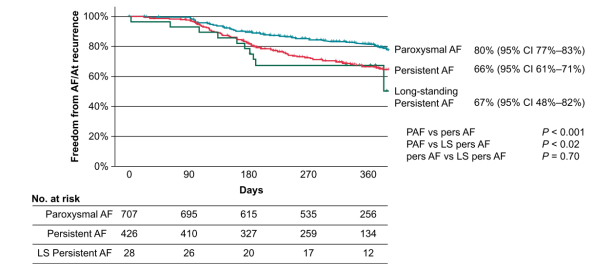
ADVENT IDE试验中纳入的患者群体均为抗心律失常药物(AAD)治疗失败或不耐受的阵发性心房颤动患者,PFA组中有1.3%的患者为术前AAD禁忌/不耐受,98.7%的患者为AAD治疗失败。随着2023版AHA心房颤动诊断与管理指南[2]的问世,将“阵发性房颤”“持续性房颤”这类基于临床表现的诊断更新为房颤不同阶段来诠释,提出早期节律控制的重要性,使得PFA这项安全有效的治疗手段赋予了更多的可能性。从近期公布结果的上市后调研数据MANIFEST 17K[3]中可以看到,纳入调研的17, 642例患者中有35%的患者为持续性房颤,而在EUropean真实世界数据[4]中,一年随访无房颤/房速发生的比例,持续性房颤为66%(95%CI 61%~71%),长程持续性房颤为67%(95%CI 48%~82%)。
当前的FARAPULSE技术乃至业内的其他研发、注册中的产品,目前都聚焦在固定术式,或者说标准化疗法的领域,而心律失常治疗的难点,不仅限于肺静脉隔离,心房外膜传导束的消融、心耳特殊位置的消融、窦房结/房室结/传导束周围区域等都是潜在的消融目标,而现有的消融能量对这些区域的透壁、均质化消融都有待优化。FARAPULSE在一些病例报道中已经安全地运用在这些区域,表现出顶部线以及后壁消融的可行性,在前壁、峡部消融期待更多其他形态的导管设计[5];而心室消融方面,尽管心室的标测技术有了长足的发展,建立了内外膜传导以及肌间传导的理论模型,但正是由于心室肌的成分复杂、厚度以及大片疤痕后对射血分数的影响,传统的消融能量始终无法均质化地消融,且尽可能少地影响泵功能。
心室消融技术在能量方面仍有待突破。从现有的动物试验数据可以看到[6],脉冲消融能量能够成功地穿透疤痕组织,并在健康组织与梗死组织形成了相似深度的消融灶(5.7±1.3mm vs 5.9±1.0mm;P=0.53),显示出FARAPULSE对于解决均质化消融挑战的可能性。
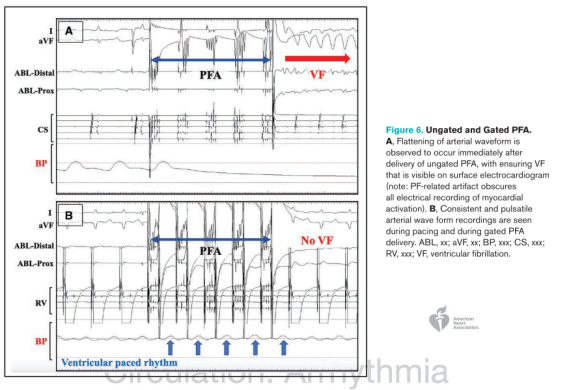
FARAPULSE从2013年开始研发,通过大量的临床前研究对参数进行微调,在此过程中对于该项技术对不同心肌组织的影响因素都积累了相当的经验,现有的房颤解决方案除了波形的优化之外,更从器械设计和消融流程上考虑到了电场的方向变化以及脉冲能量的重复性对损伤的影响,从近期的动物实验也能看到[6],保留有脉冲发放的同步技术在心室消融中仍可能具有安全性获益。此外,进一步降低消融房颤的复发率、提升远期成功率;进一步针对不同个体,丰富理论认知与优化临床术式则是后续亟待深化研究的问题。
创新技术的开发、验证与拓展使用都会是一个逐步提升研发的过程,PFA系统自2021年欧洲上市后,2年间获得了多项真实世界数据,为拓展临床应用提供了借鉴。应在此基础上,继续升华相关研究,以期使该项技术日臻完善,日趋科学。
- End -
专家简介
关注我们
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。



发表留言
暂无留言
输入您的留言参与专家互动