杨兵教授:心室壁内室速:基质特征与消融技巧

导管消融术是室性心律失常(VAs)的一线治疗选择,然而部分患者的触发灶起源于心肌深部或某些特殊部位(如左室顶部等),常规消融手段由于无法满足所需的消融深度,治疗常难以奏效,成为电生理领域的一大难题。针对此类患者的有效治疗,或将依赖于新的消融策略和技巧。在近期召开的2023亚心国际心血管病大会期间,同济大学附属东方医院杨兵教授分析了心室壁内室速的基质特征,并结合最新研究和临床经验分享了此类室速的标测与诊断要点及消融技巧。

心室壁内室速的基质特征
导管消融术是治疗特发性和瘢痕相关性VAs的有效方法。部分病例消融手术失败是由于心肌深部的致心律失常基质存在,传统消融方法消融能量无法到达深部。这种心肌深部致心律失常基质不仅存在于特发性VAs,也存在于缺血性心肌病患者中。在心肌梗死后室性心动过速(VT)患者中,22%的患者关键峡部包括室间隔,11%的患者致心律失常基质位于深部心肌。此外,据统计约8%的特发性VAs和20%的左室流出道VAs起源于心肌深部触发灶。近年来,一些非传统的消融方法可以有效地根治心肌深部起源的VAs。
心外膜激动标测提示该室速为局灶性激动,3-D立体结构标测提示该室速为跨壁8字折返。如下图所示,主要的折返环、缓慢渗透区、关键峡部可能都位于心肌深部,若消融能量可以达到,且在最靠近关键峡部进行消融,则有可能成功消融,但一部分患者并不能在心内膜或心外膜实施损伤到关键峡部的消融。
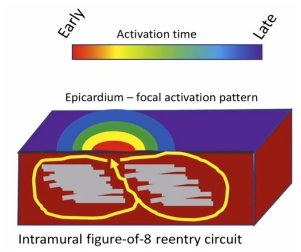
很多室速都是在一个心腔或者是一个层面,如心内膜或者心外膜,传统2-D VT标测,多极电极可以标测到关键峡部电位,占据整个心动过速周长,但这种情况相对少见。以下示意图较为理想,实际临床中折返环可能不规则,即使有多个舒张期电位,排满后也不一定是该室速最关键的通道。
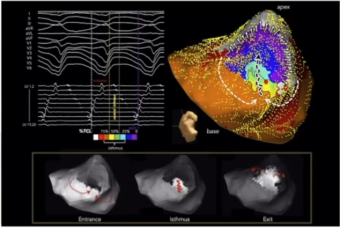
中层心肌来源的折返性VT在心内外膜面激动标测表现为激动时间缺失。
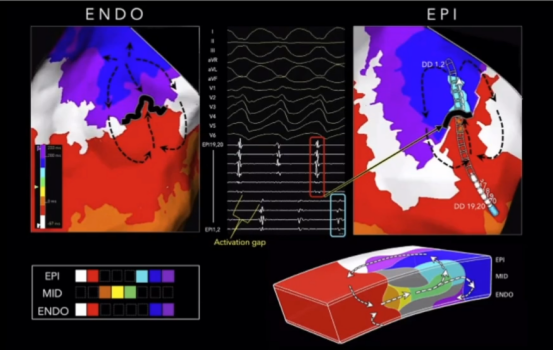
心室壁内室速的标测与诊断
仅根据常规的十二导联心电图常常难以诊断心肌深部起源的VAs,通常需要电生理检查才能做出诊断。术前和术中的影像对于识别心肌深部的VAs起源病灶有一定的作用,如在心脏MRI中表现为心肌延迟增强,或者在超声心动图中表现为强回声。
室早激动标测时,发现心室壁两侧的激动时间(室间隔左右侧、心室游离壁心内膜和心外膜侧)正好或稍早于体表QRS波(小于20ms),通常考虑为心肌深部起源的VAs。
术中室早激动标测过程中最早区域无法聚焦,单极电位无QS波,且可以记录到远场电位,考虑病灶起源可能来源于心肌深部。
单极电压异常及间隔部起搏跨壁传导时间延迟也考虑VAs起源于心肌深部。
2020年Heart Rbythm杂志上发表的一篇文章总结了心室壁内室速标测和诊断的线索:
-
起搏标测匹配较差
-
传统消融方法可有延迟抑制,但很快复发
-
瘢痕相关折返性VT在心内膜面或心外膜面标测不到收缩早期电位或者舒张中期电位
-
呈显性拖带表现
从已发表的文献和目前术中使用的标测技术来看,传统单极电图预测室壁内病灶深度缺乏特异性。未来可能研发出新型心内-外膜标测设备来有效用于预测心律失常病灶深度。
心室壁内室速的消融技巧
1. 同步单极射频消融
同步单极射频消融需要2根开放式灌注消融导管,连接到单独的射频发生器上,使射频能量被同时传递到目标心室肌层的两侧。采用这种方法,2根消融导管必须以互相垂直的朝向放置。
在临床前研究中,同步单极射频消融与序贯单极射频消融相比,具有以下优势:1)可产生更大更深的消融灶;2)减少来自心内膜面(或心外膜面贴近冠状静脉)大血流量的对流冷却效应,这最终将有利于深部心肌组织的升温效应,促进心肌深层触发灶的射频消融;3)降低深层心肌作为散热器的能力,增加单个消融导管的能量传导区域。
但是,与双极射频消融相比,同步单极射频消融没有能量传递的“方向性”。
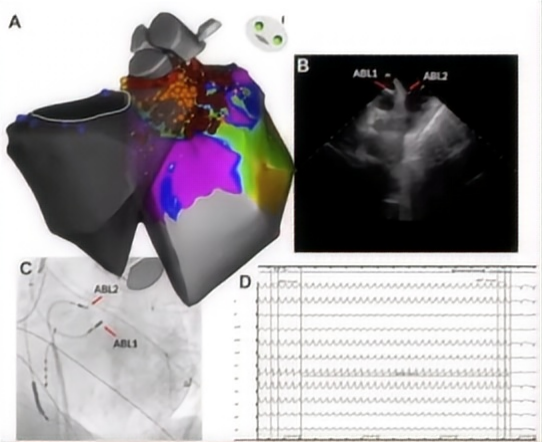
同步单极射频消融治疗难治性间隔心肌深部起源VT
经ICE (图B) 和X线透视 (图C) 验证,两个单独的消融导管位于左室流出道心内膜面 (图A: 红色消融灶) 和对侧室间隔右心室流出道 (图A: 黄色消融灶);射频期间患者VT终止 (图D)
2. 半量浓度生理盐水消融
使用半量浓度生理盐水消融比使用生理盐水可产生更深的消融灶,可以用于治疗常规消融难以治疗的心肌深部来源的心律失常。其机制可能是低浓度的生理盐水增加了消融导管周围的阻抗,从而减少了射频能量的消耗,提高了射频能量传递到心肌组织的效率。
此消融方法易于实施,在血流较少的区域有效,如心外膜或小口径静脉,但是容易发生Steam POP。
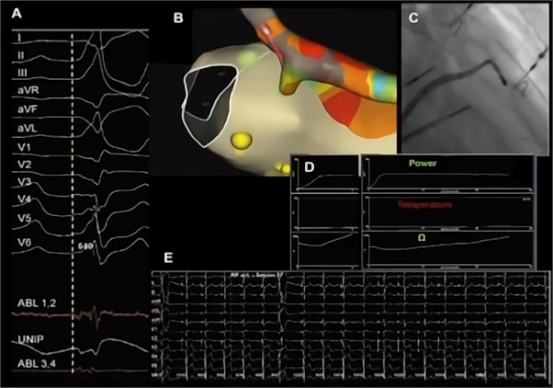
经AIV行左室顶部PVC消融
图A: ECG以及腔内图;放置在AIV内的消融导管记录到最提早的激动(图A-C),但是此处的消融是不成功的,左室心外膜面对侧的心内膜面消融也未成功。后将灌注液换成半量浓度生理盐水,再次进行射频消融,阻抗或温度没有突然升高(图D), 3秒后PVC成功终止(图E)
3.针状电极消融
针状电极消融起源于心肌内给药导管的改进,其尖端为可伸缩的细针,可用于记录电位、起搏和传递消融能量。针尖插入热电偶进行温度监测,并通过针尖向心肌灌注生理盐水。由于针尖较小,灌注盐水后可增加组织导电性,引起深部心肌组织温度升高。而且针尖起搏标测利于判断起源灶,局部注射造影剂可确认在心肌部位。目前缺乏已验证导管,有心脏穿孔风险。
4.酒精消融
酒精消融是通过动脉或静脉途径使用微导管将高浓度酒精至靶静脉内进行心肌深部病灶的消融手段,适用于左室顶部和间隔处VAs,也可进行心肌深部的标测。但是它受血管解剖限制,无法控制酒精浸润心肌组织范围。因此在使用此技术时,要熟悉静脉组织分布,并熟练掌握影像技术。
针对射频消融无效的VAs,酒精消融是一种切实可行的技术选择。研究发现,酒精消融后77%的患者无心律失常复发。
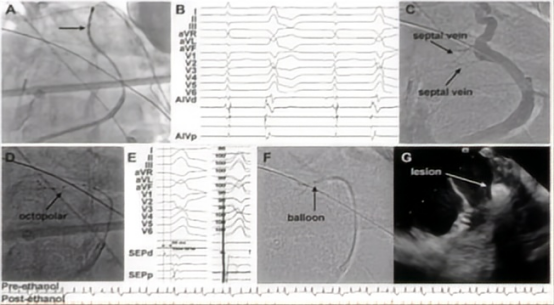
图A/B: 多极导管位于前室间静脉 (AIV) 电图最提早的位置(箭头);图C:冠状静脉窦造影显示AIV及其间隔分支;图D:将小型章鱼14导管(EP Star, Baylis, Toronto,CA)插入AIV信号最提早的间隔分支;图E:起搏标测,尽管可能有远场夺获,心肌深部信号(SEP)显示间隔有一个早期电位;图F:将气囊置入隔静脉;图G:经球囊选择性注射酒精后,心腔内超声可以发现一个回声区,并终止室早二联律
5.双极射频消融
双极射频消融是在致心律失常基质的两侧进行消融,一个主动导管连接到射频发生器的激动端口,另一个回路导管连接到射频发生器的无关电极端口。两个导管尖端之间传递射频能量,将高密度能量传递至心肌深部。
与单极序贯消融相比,双极射频消融可产生更深、更集中的消融灶,其组织穿透性可达20-25mm。而且双极射频消融对于两个电极贴靠的要求不高。

进行双极射频消融的难点是对于心室壁内室速起源点的判断,需要有一定的经验性。一般能够有短暂易过性的抑制的部位,可能是一个比较好的消融点,根据这个暂时有效的消融点,再设计一个对应的解剖消融位置,就可以形成一个射频消融损伤带。
双极射频消融适用于顽固性流出道室早/室速、左室顶部室早/室速。国外有文献报道与单极序贯消融相比,双极射频消融在损伤透壁性、损伤广度及深度、POP发生率及阻抗变化方面具有优势。而且另有文献报道,在左室顶部室速患者中,经常规贯序标测消融失败后改用双极射频消融,即刻成功率可达89%;12个月随访,复发率为44%。
在我国,双极射频消融目前也已有临床应用。杨兵教授团队自主设计了双极消融转接盒,可连接最新型的消融仪,并取得专利。相关分析顽固性OT-VAs心电图和电生理特征、评估双极消融策略的安全性和有效性的研究文章已经于2022年发表。此项研究纳入2014年10月至2019年5月在南京医科大学第一附属医院和同济大学附属东方医院行OT-VAs导管消融治疗的患者1022例,其中12例患者符合实施双极消融治疗的入选标准。患者QRS波较宽(156.5ms: 128-180 ms),7例患者V1导联为左束支传导阻滞图形,7例胸前导联移行区指数(TZI)< 0,1例最大折转指数(MDI)≥0.55,10例峰值折转指数(PDI)>0.6。
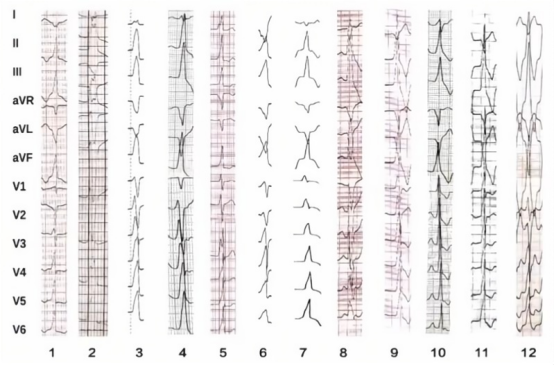
根据患者的解剖、激动标测结果及单极消融反应设计不同的双极消融模式,主要是RVOT憩室、OT间隔和左室顶部。共使用8种导管配对模式。7例(58.3%)患者两侧EA均可记录到“rS”形态单极电图,双极消融即刻成功率达83.3%。

三种双极消融模式示意图
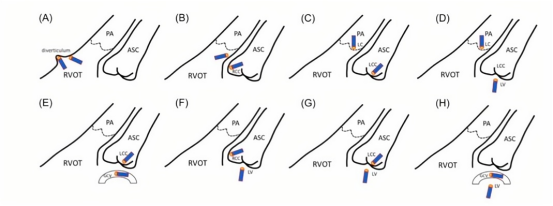
8种双极消融配对模式示意图
该项研究主要发现:约有超过1%的OT-VAs在常规单极序贯消融失败后,可考虑行双极消融,术中可使用8种导管配对模式;流出道憩室相关难治性VAs可采用双极消融成功;流出道对应侧如能同时记录到“rS”形态单极电图,提示心肌深部起源及双极消融必要性;左室基底部内膜与LCC(LV-LCC)或与GCV配对(LV-GCV)的双极模式可成功用于左室顶部VAs消融。
总结
心室壁内室速消融对于电生理医生而言是一个特殊的挑战。目前临床上已经提出了各种新的消融策略,以实现更深层更持久的消融效果。但是在实际操作过程中,需要根据患者的激动标测结果、解剖关系等信息结合多组合策略优势制定个体化的消融方案。在众多消融策略中,双极消融技术优势明显,安全性也得以证实,或将成为顽固性或病理性室速的必要消融措施。
专家简介
文中图片均来自授课幻灯
本文为医谱学术原创文章,转载请标注来源
- End -
关注我们
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。




发表留言
暂无留言
输入您的留言参与专家互动