杨文艺教授:解读最新EHJ综述,探寻PCI术后抗血小板最佳治疗策略

在经皮冠状动脉介入治疗(PCI)术后的抗血小板治疗中,传统的双重抗血小板治疗(DAPT)方案长期作为常规治疗,但伴随出血风险的增加。为了解决这一问题,医学界开始探索新的治疗策略。近期,EHJ发表了一篇综述,聚焦于无阿司匹林的抗血小板治疗策略[1]。该综述综合了现有的临床证据、专家共识及未来研究方向。上海交通大学附属第一人民医院杨文艺教授对该综述进行深入解读,并分享了其在无阿司匹林抗血小板治疗策略方面的临床经验和个人观点。本文特此整理,以供临床参阅。

P2Y12受体抑制剂单药治疗与DAPT对比
已有多项研究比较了PCI术后标准的DAPT与1~3个月短期DAPT后P2Y12受体抑制剂单药疗法(替格瑞洛或氯吡格雷)的治疗效果。
●DAPT后转替格瑞洛单药治疗
GLOBAL LEADERS研究[2]比较了在PCI术后使用1个月DAPT后转为替格瑞洛单药治疗至24月vs.12个月DAPT后转为阿司匹林单药治疗至24月的效果,主要终点事件为PCI术后730天内全因死亡及新发Q波心梗的复合终点。结果显示,两组在主要终点累积发生率分别为3.81%vs4.37%,差异没有统计学意义,且出血事件风险两组相似。根据研究方案,2年随访期间,试验组和对照组分别在一个月和一年调整治疗药物,研究也预设了这两个时间点的界标分析(Landmark analysis),一月内两组治疗一致。一年期界标事后分析[3]结果提示实验组方案较标准治疗显著降低30天~1年主要出血相对风险48%,而且实验组较标准治疗显著降低缺血终点事件相对风险21%。TWILIGHT研究[4]则入选接受PCI治疗后经过3个月替格瑞洛和阿司匹林DAPT且无重大出血事件的高风险患者,比较后续12月内继续接受替格瑞洛和阿司匹林DAPT治疗或替格瑞洛单药治疗患者的出血和缺血事件发生率。结果显示与继续DAPT组相比,替格瑞洛单药治疗可在不增加随机分组后1年内缺血事件的基础上显著降低出血风险。此外,仅入组韩国患者的TICO研究[5]发现,与12个月DAPT相比,DAPT治疗3个月后使用替格瑞洛单药治疗,1年的净不良临床终点事件发生率显著降低,这主要归因于大出血事件的减少,而缺血事件无显著差异。
今年美国心脏病学会(ACC)年会上公布了ULTIMATE-DAPT研究[6]结果。该研究是一项前瞻性、多中心、是否IVUS指导和是否缩短DAPT的二次随机、对照试验,旨在探讨针对急性冠脉综合征(ACS)患者IVUS指导的药物洗脱支架(DES)置入术的获益及支架术后一个月替格瑞洛联合阿司匹林DAPT后替格瑞洛单药治疗vs.继续替格瑞洛联合阿司匹林DAPT相比能否在不增加PCI后1~12个月期间发生主要不良心脑血管事件(MACCE)的风险的基础上,降低临床相关出血风险。研究结果显示,相较常规DAPT组,一月后替格瑞洛单药治疗组降低了临床相关出血风险达55%(HR 0.45,95%CI 0.30-0.66,P<0.0001),且两组MACCE发生率无显著差异(3.6%vs3.7%,HR 0.98,95%CI 0.69-1.39,P=0.89)(如图2)。值得一提的是,由于该研究共纳入中国患者占88.1%,因此研究结果更能代表中国的患者与中国临床实践。
综合上述研究结果不难发现,与标准DAPT(12个月)相比,短期一个月DAPT后转为替格瑞洛单药治疗可获得相似或更有益的结局。开放标签的T-PASS研究[7]探索了甚至更短的DAPT都不增加传统缺血相关事件风险。T-PASS研究发现,ACS患者在1个月内(中位数16天)停用阿司匹林后,替格瑞洛单药治疗的净复合终点优于12个月DAPT,驱动原因自然是缩短DAPT显著减少了大出血事件。
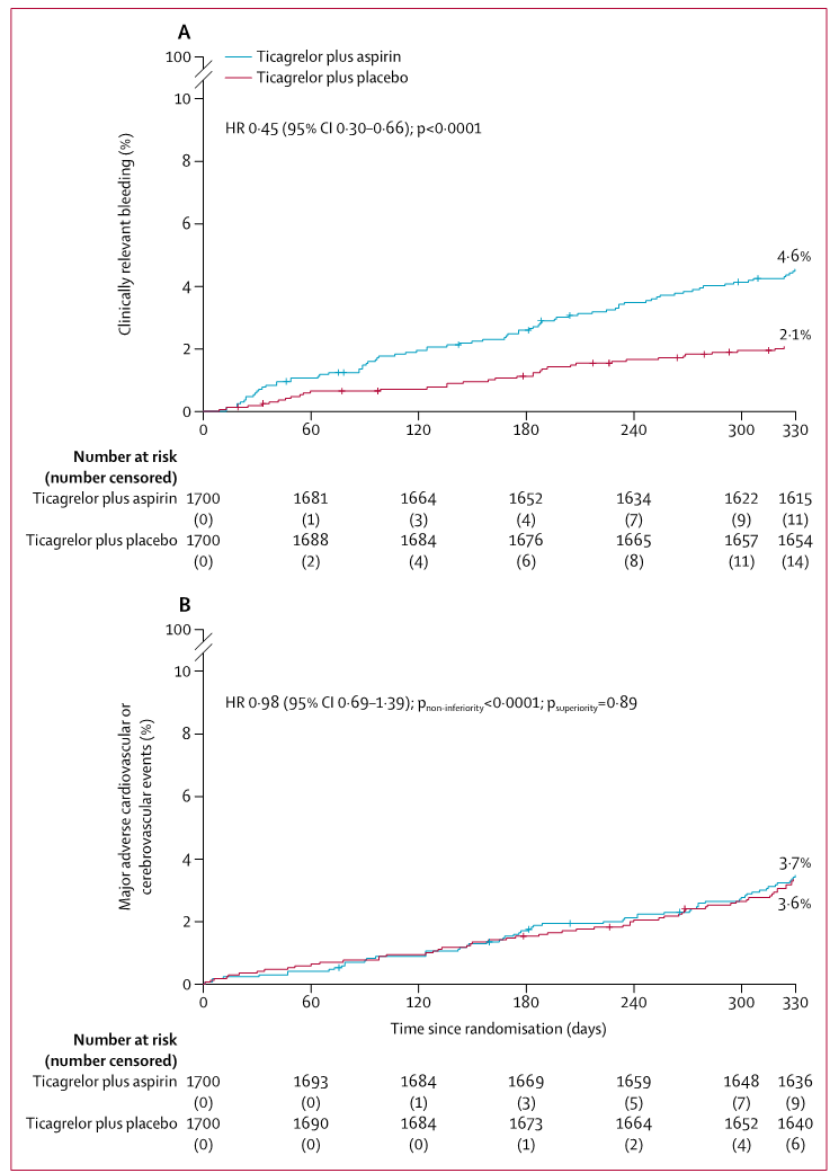
图2:ULTIMATE DAPT研究主要结果[6]
●DAPT后转氯吡格雷单药治疗
SMART-CHOICE研究[8]纳入2993名PCI术后的韩国患者,分析显示与常规12月DAPT相比,3个月DAPT后转为P2Y12受体抑制剂(P2Y12i)单药(氯吡格雷占77%)治疗在1年内对于缺血事件的主要复合终点达到了非劣效,且出血风险显著降低;但缩短DAPT组在6个月和12月时分别有14.4%和8.9%的患者还在继续使用阿司匹林,稀释了两组之间缺血相关事件的差异;另外比较大的非劣界值降低了样本量的需求,但也不可避免降低了该研究发现两组差异的统计效能。在日本PCI术后患者(n=3045)中开展的STOPDAPT-2研究[9]发现,DAPT一月后氯吡格雷单药治疗在净复合终点上优于常规12个月DAPT,主要由于减少总体出血,而未增加缺血事件风险。但STOPDAPT-2研究的主要终点事件发生率低于计算样本量时的预计、净获益终点包括轻微出血、选择性入选了低缺血风险患者以及研究中腔内影像学技术指导比例(99.7%)远比临床实践高;鉴于这些问题,该研究结果的外推性存在一定问题。
加上STOPDAPT-2中入组的及另外入组的ACS患者,STOPDAPT-2 ACS研究[10]总共纳入4136名日本ACS并进行PCI的患者,结果显示与12个月的DAPT治疗相比,接受1或2个月DAPT后转为氯吡格雷单药治疗增加心梗事件风险,导致心血管和出血事件的净复合终点未能达到非劣效。研究主要终点的发生率低于预期,在试验统计效能不足的情况已发现缺血事件增加,更加强调了长期使用不同P2Y12受体抑制剂极大影响了何时可以终止DAPT而选择P2Y12受体抑制剂单抗。
OPT-BIRISK研究[11]纳入中国出血和缺血双高危的ACS患者,在完成9~12个月的标准DAPT治疗后,比较了给予氯吡格雷单药治疗是否优于继续DAPT。研究结果显示,继续给予9个月的氯吡格雷单药治疗在减少临床相关出血风险方面优于继续DAPT,且缺血性事件发生率较低。结合Host-Exam研究[12]和DAPT研究[13]结果,对于不符合DAPT研究入组标准的PCI术后患者,氯吡格雷单药治疗优于阿司匹林单药或者长期DAPT治疗。
总之,上述临床研究结果表明短期DAPT后选择氯吡格雷单药疗法在非高危稳定性冠心病患者中具有与标准DAPT(12个月)相似或更好的安全性和疗效。在标准DAPT双抗后,采用氯吡格雷单药治疗也优于阿司匹林单抗和继续DAPT治疗。
●DAPT后转为P2Y₁₂受体抑制剂单药疗法(替格瑞洛或氯吡格雷)的荟萃分析
一项纳入GLOBAL LEADERS、SMART-CHOICE、STOPDAPT-2、TWILIGHT和TICO研究在内的研究水平荟萃分析显示[14],PCI术后DAPT1~3个月后停用阿司匹林可显著减少出血事件发生,且不会增加缺血事件发生。针对DACAB、GLASSY、SMART-CHOICE、STOPDAPT-2、TWILIGHT和TICO等研究个体水平的荟萃分析[15]显示,DAPT使用1~3个月停用阿司匹林并继续使用替格瑞洛或氯吡格雷单药治疗在死亡、脑卒中或心梗复合终点上非劣于常规DAPT[HR 0.93(95%CI 0.79-1.09),非劣比较P=0.005],而且出血风险显著降低 [HR 0.49(95%CI 0.39-0.63)]。
近期发表的一项个体水平荟萃分析[16]纳入(GLASSY、SMART-CHOICE、STOPDAPT-2、TWILIGHT、TICO和STOPDAPT-2 ACS)并分别比较了替格瑞洛或氯吡格雷单药治疗是否优于常规DAPT。结果显示,与常规DAPT相比,短程DAPT后转为替格瑞洛单药治疗(纳入GLASSY、TWILIGHT及TICO研究)在全因死亡、心肌梗死或脑卒中复合终点方面非劣于常规DAPT[HR 0.89 (95%CI 0.74-1.06),非劣比较P=0.004],且降低了大出血风险[HR 0.47 (95%CI 0.36-0.62)]和净不良心脑血管事件 [HR 0.74 (95%CI 0.64-0.86)](如图3所示)。
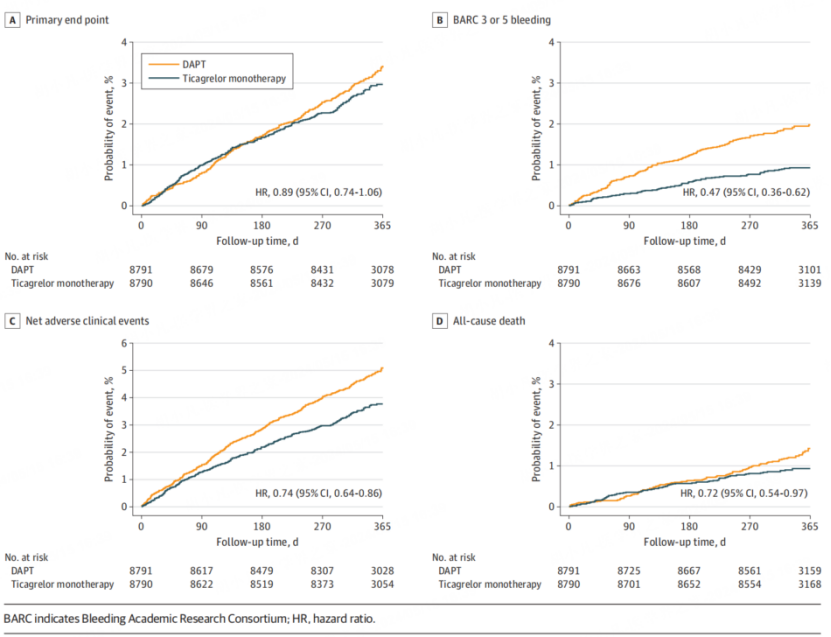
图3:接受替格瑞洛单药治疗vs.DAPT的患者的临床结局分析[13]
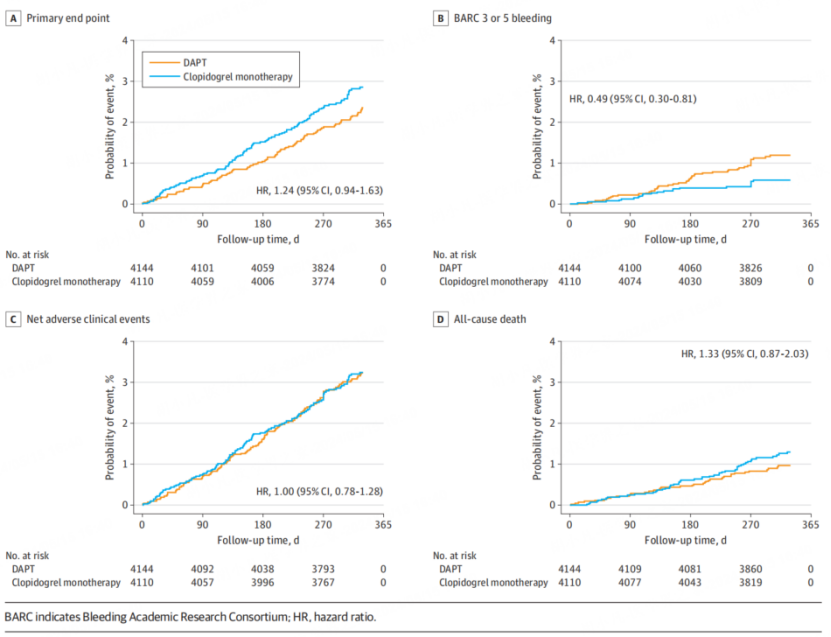
图4:接受氯吡格雷单药治疗 vs. DAPT的患者的临床结局分析[13]
P2Y12受体抑制剂(单药治疗)与DAPT治疗的亚组比较
●急性冠脉综合征
众多探索缩短双抗的研究入组了缺血风险完全不同的慢性(CCS)和急性冠脉综合征患者,仅TICO、T-PASS和STOPDAPT-2 ACS研究仅纳入ACS患者。在STOPDAPT-2 ACS研究中,与DAPT相比,氯吡格雷单药治疗倾向于增加缺血风险。而在TICO和T-PASS研究中,替格瑞洛单药治疗在总ACS人群和高风险亚组[如糖尿病和ST段抬高型心肌梗死(STEMI)]中显示出与DAPT相似的抗缺血疗效。由于仅纳入韩国人群、采用复合净获益临床终点及研究事件率低于预期的原因,TICO和T-PASS研究结果内部验证和外推性都受到质疑。但在GLOBAL LEADERS一年随访数据界标分析和TWILIGHT试验ACS亚组分析中依然可以看出替格瑞洛单药治疗在ACS患者中的良好效果和更低的出血风险。
与GLOBAL-LEADERS总体人群研究2年随访结果不同,在仅纳入GLOBAL LEADERS研究中ACS患者(n=7487,其中28%是急性心梗患者)并进行一年界标分析发现,与以替格瑞洛为基础的常规DAPT相比,1月DAPT后改为替格瑞洛单药治疗显著降低了48%的大出血风险,并在数量上降低了死亡或Q波心梗的发生[3]。此外,在TWILIGHT亚组分析中,与常规DAPT相比,3个月DAPT后改为替格瑞洛单药治疗在NSTE-ACS患者中显著减少了出血风险达53%,在CCS中显著减少了24%的出血风险[17]。这些结果表明,与CCS患者相比,短期DAPT后转为替格瑞洛单药治疗在ACS患者中具有更好获益。究其原因可能与ACS患者的出血风险较慢性冠脉综合征患者更高有关。为了进一步证实这些亚组分析结果,还需纳入高危ACS患者进行专门的随机对照研究。
●复杂PCI
一些研究的亚组分析和荟萃分析[18]显示,在复杂PCI患者中,DAPT治疗1~3个月后采用P2Y12受体抑制剂单药治疗与常规12月DAPT相比,可以减少出血风险且不会增加缺血事件。另一项纳入GLASSY、SMART-CHOICE、STOPDAPT-2、TICO和TWILIGHT研究的22941例患者的荟萃分析(复杂PCI的患者占20.4%)显示[19],在包括全因死亡、心梗和卒中的主要复合终点上,短期DAPT后P2Y12受体抑制剂单药治疗与常规DAPT治疗结果相比的HR,在复杂PCI和非复杂PCI中相似。此外,短期DAPT后P2Y12受体抑制剂单药治疗减少大出血事件发生率,也与PCI复杂性无关。然而,鉴于这些阳性结果是在特定患者特征(37%来自东亚人群、CCS患者占39%及STEMI人数少)的条件下获得的,尚需开展更多临床研究来验证目前的研究结果。
●高出血风险(HBR)
在对短期DAPT后P2Y12受体抑制剂单药治疗与标准DAPT比较的随机对照研究中HBR患者的荟萃分析发现,无论HBR状态如何,短期DAPT后P2Y12受体抑制剂单药治疗都倾向减少出血事件且不增加复合缺血事件[20]。
P2Y12受体抑制剂(单药治疗)与阿司匹林(单药治疗)治疗对比
目前大多数P2Y12受体抑制剂(单药治疗)的研究都以DAPT作为对照组,较少研究直接比较PCI术后在不同时间采取P2Y12受体抑制剂或阿司匹林的治疗效果。
●P2Y12受体抑制剂单药治疗(替格瑞洛或氯吡格雷)与阿司匹林单药治疗对比
HOST-EXAM是唯一直接比较PCI术后6-18个月DAPT后阿司匹林与氯吡格雷的RCT研究。研究结果显示,相比阿司匹林,氯吡格雷在2年内主要净不良临床终点相对减少了27%[12]。主要原因为显著减少了出血、卒中和ACS再入院。但鉴于HOST-EXAM研究主要在亚洲人群中进行,可能限制了研究结论在其他人群中的外推性。一般认为亚洲人群氯吡格雷慢代谢基因型比例更高,提示在欧美人群中应该有类似、甚至更好的净获益。
在GLOBAL LEADERS研究中,直接比较了PCI术后第2年使用替格瑞洛与阿司匹林的有效性和安全性。该研究发现,与阿司匹林相比,替格瑞洛组心梗风险较低。综合分析SMART-CHOICE和SMART-DATE研究对P2Y12受体抑制剂与阿司匹林在PCI后的效果进行间接比较,结果显示P2Y12受体抑制剂倾向于减少心梗和出血风险。由于是间接比较,研究结论需要谨慎对待。
●P2Y12受体抑制剂单药治疗(替格瑞洛或氯吡格雷)与阿司匹林单药治疗对比的荟萃分析
一项网状荟萃[21]分析比较了在PCI后DAPT停用情况下,P2Y12受体抑制剂与阿司匹林的疗效。荟萃分析共纳入19项研究的73126名患者。结果显示,与P2Y12受体抑制剂单药相比,阿司匹林组心梗相对增加了32%。在死亡、卒中和支架内血栓形成复合终点方面,两种单药治疗无显著差异。
P2Y12受体抑制剂单药治疗的指南建议和思考
此前,2020年欧洲指南[22]和2021年美国指南[23]推荐,对于PCI术后患者短期DAPT后,可以采用P2Y12受体抑制剂单药治疗。基于这些指南,根据荟萃分析欧洲多学会(EAPCI、ACVC和EAPC)共识建议1~3个月DAPT后转为P2Y12受体抑制剂单药治疗,只有在缺血风险高和出血风险极低的患者中采用常规/延长DAPT[24]。
随着P2Y12受体抑制剂单药治疗研究不断深入,2023年美国和欧洲指南[25-26]推荐,6个月和12个月DAPT分别是稳定性CAD或ACS患者PCI术后的标准治疗;而对于使用DAPT3~6个月后无事件发生且不伴有高缺血风险的患者,应考虑采用抗血小板单药治疗(优选P2Y12受体抑制剂)(IIa,A)。因此,临床对于非HBR的患者,应首选标准DAPT治疗;而对于非高缺血风险的患者,可考虑短期DAPT后继续P2Y12受体抑制剂治疗,以减少不必要的DAPT暴露。
对于HBR患者,越来越多的证据支持短期DAPT(1~3个月)后P2Y12受体抑制剂单药治疗应作为低中度缺血风险患者的治疗策略之一,或作为有高缺血风险患者的标准DAPT的替代方案。
在临床实践中,P2Y12受体抑制剂单药疗法具体应选择哪种药物?欧洲指南[25]建议,对于接受PCI的ACS患者,可以优先考虑普拉格雷,但目前普拉格雷单药治疗的研究数据仍然有限,且暂未在中国获批。在CCS合并HBR,同时伴高缺血风险的患者中,短期DAPT后选择替格瑞洛/普拉格雷可能优于氯吡格雷。基于STOPDAPT-2 ACS研究结果,对于ACS患者,在PCI后DAPT治疗(1个月)后,选用氯吡格雷单药治疗并非合适的选择。相反,在无HBR且缺血风险低的CCS患者中,氯吡格雷或可优先考虑。
此外,目前对P2Y12受体抑制剂单药治疗的疗程仍不确定,尚不明确是否应长期维持替格瑞洛90mg单药治疗,或改为替格瑞洛60mg,以及换成阿司匹林或氯吡格雷治疗。此外,尽管单臂研究显示在欧美人群进行PCI后以每日普拉格雷10mg和在日本人群中采用每日3.75mg的起始单抗血小板治疗方案,具有非常好的安全性和有效性。但是近期在日本人群中开展的STOPDAPT-3研究[27]提示,与一个月DAPT转为每日普拉格雷3.75mg组相比,起始小剂量普拉格雷单药并没降低出血风险,但增加支架内血栓的风险。
小结
PCI后短期DAPT转为P2Y12受体抑制剂单药进行抗血小板治疗一直是临床研究的焦点。虽然部分研究存在局限性,但结果总体上支持采用无阿司匹林策略作为标准DAPT的替代方案。与持续DAPT相比,短期DAPT后的P2Y12受体抑制剂单药治疗可显著降低出血风险,同时不会增加血栓性或缺血性事件。临床上最佳抗血小板决策应根据患者的具体情况个性化制定,目前单药抗血小板方案还有尚未解决的问题。正在进行的比较DAPT与P2Y12受体抑制剂单药治疗的RCT研究,将有望为无阿司匹林治疗方案提供更多的认识。
来源:医学界心血管频道
专家简介
参考文献:
[1].Piera Capranzano, et al. Aspirin-free antiplatelet strategies after percutaneous coronary interventions. Eur Heart J. 2024 Feb 21;45(8):572-585.
[2].Vranckx P, et al. Ticagrelor plus aspirin for 1 month, followed by ticagrelor monotherapy for 23 months vs aspirin plus clopidogrel or ticagrelor for 12 months, followed by aspirin monotherapy for 12 months after implantation of a drug-eluting stent: a multicentre, open-label, randomised superiority trial. Lancet. 2018;392(10151):940-949.
[3].Tomaniak M, et al. Benefit and Risks of Aspirin in Addition to Ticagrelor in Acute Coronary Syndromes: A Post Hoc Analysis of the Randomized GLOBAL LEADERS Trial. JAMA Cardiol. 2019;4(11):1092-1101.
[4].Mehran R, et al. Ticagrelor with or without Aspirin in High-Risk Patients after PCI. N Engl J Med. 2019; 381(21): 2032-2042.
[5].Kim BK, et al. Effect of Ticagrelor Monotherapy vs Ticagrelor With Aspirin on Major Bleeding and Cardiovascular Events in Patients With Acute Coronary Syndrome: The TICO Randomized Clinical Trial. JAMA. 2020;323(23):2407-2416.
[6].Zhen Ge, et al. Ticagrelor alone versus ticagrelor plus aspirin from month 1 to month 12 after percutaneous coronary intervention in patients with acute coronary syndromes (ULTIMATE-DAPT): a randomised, placebo-controlled, double-blind clinical trial. The Lancet. 2024 May 11; 403(10439):1866-1878.
[7].Hong SJ, et al. Stopping Aspirin Within 1 Month After Stenting for Ticagrelor Monotherapy in Acute Coronary Syndrome: The T-PASS Randomized Noninferiority Trial. Circulation. 2024; 149 (8): 562-573.
[8].Hahn JY, et al. Effect of P2Y12 inhibitor monotherapy vs dual antiplatelet therapy on cardiovascular events in patients undergoing percutaneous coronary intervention: the SMART- CHOICE randomized clinical trial. JAMA 2019; 321:2428–37.
[9].Watanabe H, et al. Effect of 1-month dual antiplatelet therapy followed by clopidogrel vs 12-month dual antiplatelet therapy on cardiovascular and bleeding events in patients receiving PCI: the STOPDAPT-2 randomized clinical trial. JAMA 2019; 321:2414–27.
[10].Watanabe H, et al. Comparison of clopidogrel monotherapy after 1 to 2 months of dual antiplatelet therapy with 12 months of dual antiplatelet therapy in patients with acute coronary syndrome. JAMA Cardiol 2022; 7:407–17.
[11].Li Y, et al. Extended antiplatelet therapy with clopidogrel alone versus clopidogrel plus aspirin after completion of 9-to 12-month dualantiplatelet therapy for acute coronary syndrome patients with both high bleeding and ischemic risk. Rationale and design ofthe OPT-BIRISK double-blinded, placebo-controlled randomized trial. Am Heart J 2023; 228:1–7.
[12].Koo BK, et al. Aspirin versus clopidogrel for chronic maintenance monotherapy after percutaneous coronary intervention (HOST-EXAM): an investigator-initiated, prospective, randomised, open-label, multicentre trial. Lancet. 2021;397(10293):2487-2496.
[13].Mauri L, et al. Twelve or 30 months of dual antiplatelet therapy after drug-eluting stents. N Engl J Med. 2014;371(23):2155-2166.
[14].O'Donoghue ML, et al. The safety and efficacy of aspirin discontinuation on a background of a P2Y12 inhibitor in patients after percutaneous coronary intervention: a systematic review and meta-analysis. Circulation 2020;142:538–45.
[15].Valgimigli M, et al. P2y12 inhibitor monotherapy or dual antiplatelet therapy after coronary revascularisation: individual patient level meta-analysis of randomised controlled trials. BMJ 2021;373:n1332.
[16].Marco Valgimigli, et al. Ticagrelor or Clopidogrel Monotherapy vs Dual Antiplatelet Therapy After Percutaneous Coronary Intervention: A Systematic Review and Patient-Level Meta-Analysis. JAMA Cardiol. 2024 May 1; 9(5): 437- 448.
[17].Vranckx P, et al. Efficacy and safety of ticagrelor monotherapy by clinical presentation: pre-specified analysis of the GLOBAL LEADERS trial. J Am Heart Assoc 2021;10:e015560.
[18].Dangas G, et al. Ticagrelor with or without aspirin after complex PCI. J Am Coll Cardiol 2020;75:2414–24.doi: 10.1016/j.jacc.2020.03.011.
[19].Gragnano F, et al. P2y12 inhibitor monotherapy or dual antiplatelet therapy after complex percutaneous coronary inter ventions. J Am Coll Cardiol 2023; 81:537–52.
[20].Costa F, et al. Dual antiplatelet therapy duration after percutaneous coronary intervention in high bleeding risk: a meta-analysis of randomized trials. Eur Heart J 2023; 44:954–68.
[21].Andò G, et al. P2y12 inhibitor or aspirin following dual antiplatelet therapy after percutaneous coronary intervention: a network meta-analysis. JACC Cardiovasc Interv 2022; 15:2239–49.
[22].Lawton JS, et al. 2021 ACC/AHA/SCAI guideline for coronary artery revascularization: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol 2022; 79:e21–e129.
[23].Collet JP, et al. 2020 ESC guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J 2021; 42: 1289–367.
[24].Navarese EP, et al. Within and beyond 12-month efficacy and safety of antithrombotic strategies in patients with established coronary artery disease: two companion network meta-analyses of the 2022 joint clinical consensus statement of the European Association of Percutaneous Cardiovascular Interventions (EAPCI), European Association for Acute CardioVascular Care (ACVC), and European Association of Preventive Cardiology (EAPC). Eur Heart J Cardiovasc Pharmacother 2023; 9:271–90.
[25].Virani SS, et al. 2023 AHA/ACC/ACCP/ASPC/NLA/PCNA guideline for the management of patients with chronic coronary disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol 2023; 82:833–955.
[26].Byrne RA, et al. 2023 ESC guidelines for the management of acute coronary syndromes. Eur Heart J 2023;44:3720–826.
[27].Natsuaki M, et al. An Aspirin-Free Versus Dual Antiplatelet Strategy for Coronary Stenting: STOPDAPT-3 Randomized Trial . Circulation. 2024 Feb 20;149(8):585-600.
医谱app
扫码或者点击图片下载
微信公众号
扫码或点击图片关注
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、上载、下载、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。





发表留言
暂无留言
输入您的留言参与专家互动