GW-ICC/AHS.25 | 直面"甘"扰—甘油三酯在ASCVD中的罪与罚,全球专家激辩前沿

2025年10月13日,在第36届长城心脏病学大会暨亚洲心脏大会2025期间,一场由国际动脉粥样硬化学会(IAS)与长城会联合举办的高端论坛在线上召开。论坛聚焦于当前血脂领域最具争议和潜力的热点—甘油三酯(TG)与动脉粥样硬化性心血管疾病(ASCVD)。多位IAS领导层核心成员及海内外顶尖学者,围绕TG的流行病学、致病机制、新疗法及未来展望进行了深入探讨,为我们厘清了这一复杂领域的现状与未来。

Raul Santos教授:TG的当代流行病学—无处不在的"隐形"风险
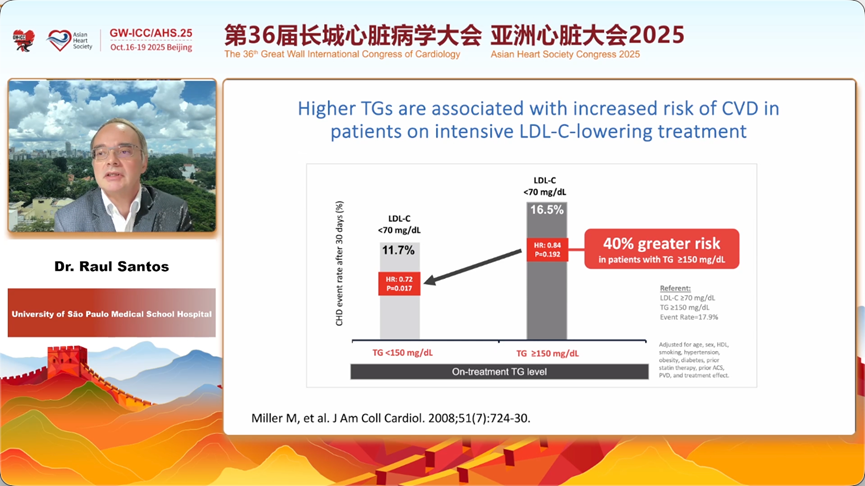
IAS前任主席、巴西圣保罗大学的Raul Santos教授首先用翔实的数据描绘了高甘油三酯血症的全球图景。他指出,血液中升高的TG是富含甘油三酯的脂蛋白(TRLs)及其残粒积聚的标志,而后者已被孟德尔随机化研究证实是ASCVD的独立致病因素。
Santos教授重点介绍了INSPIRE国际研究的结果。这项覆盖全球13个国家(包括中国)的研究发现,即便在接受现代他汀治疗的ASCVD二级预防人群中,仍有高达三分之一的患者存在高甘油三酯血症,这一现象与肥胖、糖尿病和吸烟密切相关,凸显了生活方式干预的重要性。然而,他也指出了治疗上的困境:备受瞩目的PROMINENT研究显示,尽管贝特类药物Pemafibrate能显著降低TG,却未能带来心血管获益。他推测,未来的临床试验可能需要靶向更高TG水平、风险也更高的人群,才能验证降TG治疗的价值。目前,强化降低LDL-C/ApoB、改善生活方式、应用GLP-1受体激动剂及高纯度鱼油(二十碳五烯酸乙酯)是应对这一挑战的主要策略。
吴娜琼教授:来自中国的证据—残粒胆固醇是ASCVD的独立"元凶"
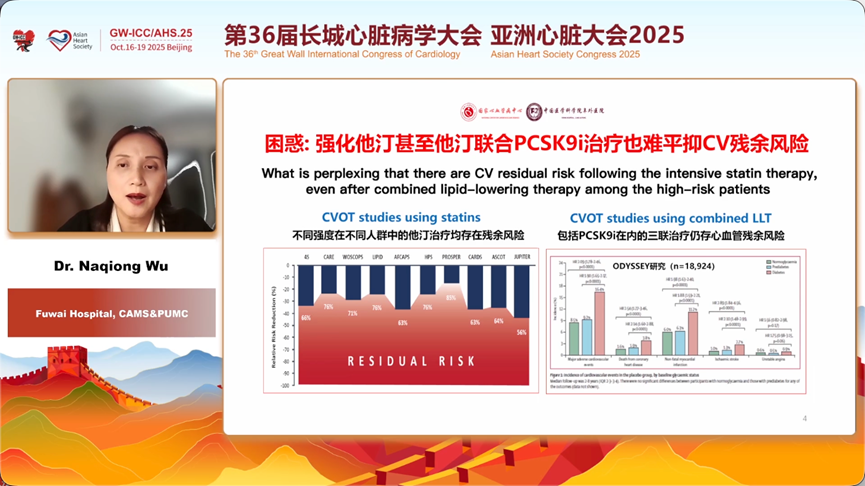
中国医学科学院阜外医院的吴娜琼教授代表李建军教授团队,分享了基于中国人群的大量原创性研究,为TRLs的致病性提供了坚实的“本土证据”。其团队聚焦于TRLs的核心致病成分——残粒胆固醇(RC),其计算公式为:RC = 总胆固醇 - 高密度脂蛋白胆固醇(HDL-C) - 低密度脂蛋白胆固醇(LDL-C)。
阜外医院一系列研究清晰地揭示了RC的临床危害:
-
在接受PCI的糖尿病患者中,高RC水平显著增加了围术期心肌损伤的风险。
-
在冠心病合并糖代谢异常(糖尿病或糖尿病前期)的患者中,高RC与不良预后密切相关,提示其与代谢紊乱存在协同致病作用。
-
在高强度他汀治疗的冠心病患者中,高RC预测复发性心血管事件的作用独立于炎症水平(hs-CRP),表明RC拥有独特的致动脉粥样硬化通路。
-
即使在LDL-C已达标(<1.8 mmol/L)的患者中,RC及ApoC3等TRL相关标志物升高,仍预示着更差的远期预后。 这些来自中国人群的高质量证据,雄辩地证明了残粒胆固醇是ASCVD残留风险中一个不容忽视的独立致病因子。
Peter Libby教授:从遗传学到新疗法—靶向TG的新希望
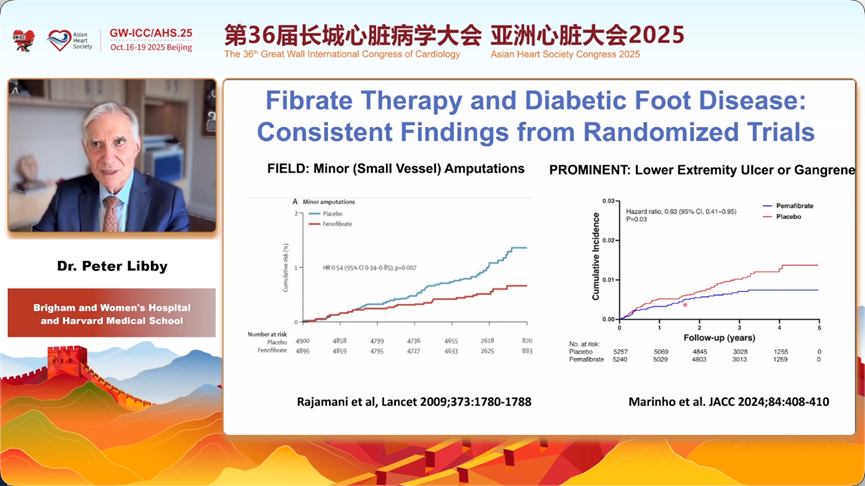
IAS即任前主席、哈佛医学院的Peter Libby教授高屋建瓴地指出了降脂治疗的未来方向。他首先明确,在经历无数次失败后,升高HDL已不再是可行的治疗策略。临床的焦点必须转向天平的另一端—以TG为代表的TRLs。他强调,TRLs不仅是致病的,其促炎效应远强于LDL,是驱动残留风险的关键因素。
那么,如何有效干预TRLs?Libby教授直指核心:调控脂蛋白脂酶(LPL)的活性。LPL是分解TRLs的关键酶,而ApoC3和血管生成素样蛋白3(ANGPTL3)是其天然的抑制剂。因此,通过基因疗法(如反义寡核苷酸、siRNA)或单克隆抗体抑制ApoC3和ANGPTL3,从而“解放”LPL的活性,是当前最有前途的降TG治疗策略。他回顾了贝特类药物和普通Omega-3脂肪酸的失败,并指出只有高纯度、高剂量的二十碳五烯酸乙酯(Icosapent Ethyl)在REDUCE-IT等研究中显示出获益。展望未来,以RNA疗法为代表的新一代药物正蓄势待发,有望最终攻克TG这一顽固的残留风险。
Brian Tomlinson教授:追本溯源—餐后高脂血症中,谁是真正的罪魁祸首?
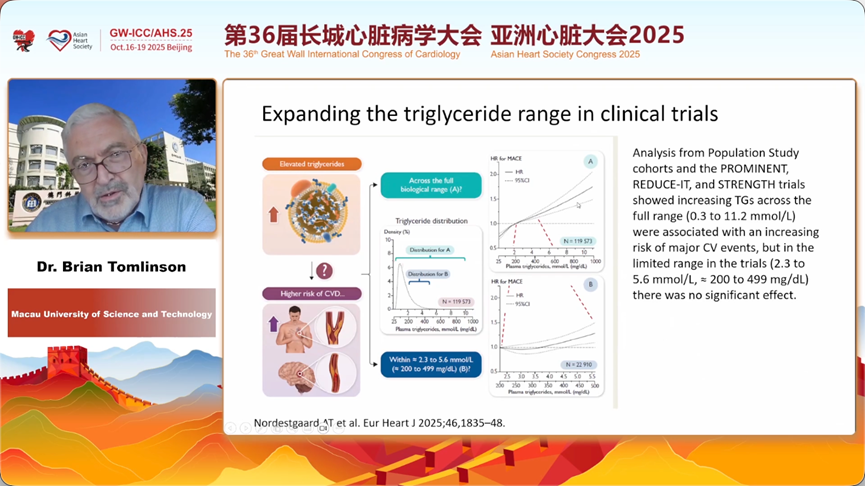
澳门科技大学的Brian Tomlinson教授带领大家深入探讨了餐后高脂血症的致病机制,并回答了一个根本性问题:“乳糜微粒(Chylomicrons)本身致病吗?”他指出,人体大部分时间处于餐后状态,因此非空腹TG水平更能反映真实风险。
他精辟地辨析道:完整的乳糜微粒:由肠道吸收膳食脂肪后形成,其颗粒巨大,无法穿透血管内皮进入血管壁,因此可能不直接致病。这可以解释为何经典的家族性乳糜微粒血症患者ASCVD风险不高。乳糜微粒残粒:是乳糜微粒经过LPL初步分解后的产物。它们颗粒变小,能够穿透内皮,并被巨噬细胞吞噬形成泡沫细胞,是高度致动脉粥样硬化的元凶。 此外,Tomlinson教授还提出一个新颖观点:脂解过程本身即可促炎。LPL在血管内皮表面分解TG时释放的游离脂肪酸,可能直接激活局部炎症反应,这为TRLs的致病性提供了另一重解释。他总结,我们的关注点不应是乳糜微粒本身,而应是其代谢后产生的、更小、更致病的残粒。
结语
本次IAS联合论坛传递了一个强有力的信息:在后他汀时代,对甘油三酯的忽视必须终结。来自遗传学、流行病学和基础研究的证据链已趋于完整,共同将富含甘油三酯的脂蛋白及其残粒推上了ASCVD残留风险的“审判席”。尽管以贝特类为代表的传统降TG疗法令人失望,但以抑制ApoC3和ANGPTL3为靶点的新一代精准疗法正孕育着巨大希望。本次论坛明确了未来的方向——管理ASCVD,必须从“唯LDL论”走向“全面风险管理”,直面并攻克由甘油三酯带来的严峻“甘”扰。

发表留言
暂无留言
输入您的留言参与专家互动