解放军总医院第六医学中心心血管外科肖苍松教授团队原创“CPFT”新技术:可最大限度降低A型夹层全弓置换术神经系统损伤风险
神经系统损伤是全主动脉弓置换(TAR)术后常见并发症之一。为降低神经系统并发症风险,解放军总医院第六医学中心心血管外科肖苍松教授团队创新性提出“脑灌注优先技术”(CPFT,cerebral perfusion-first technique),为Stanford A型主动脉夹层的TAR治疗提供了全新的技术路径。
团队为22例无灌注不良的Stanford A型主动脉夹层实施CPFT-TAR手术,取得了令人鼓舞的早期结果:术后30天零死亡、无卒中、无截瘫,几乎无谵妄。CPFT可最大限度地降低神经系统损伤风险,可能是一种更为优化的TAR手术策略。本文将通过肖苍松教授团队发表于JTCVS Techniques上的一例复杂病例,对CPFT技术展开详细介绍。

患者42岁男性,因胸痛入院,经CTA检查确诊为Stanford A型主动脉夹层合并主动脉瓣反流,对其进行紧急CPFT-TAR手术。
上半胸骨切开术
常规进行脑氧饱和度监测,从胸骨切迹至第四肋间进行倒“T”形上半胸骨切开术。通过该微创方法进行TAR手术,去除胸腺脂肪垫并离断头臂静脉,暴露主动脉弓。接着游离无名动脉(IA)、左颈动脉(LCA)及左锁骨下动脉(LSCA),并小心分离周围组织(包括肌肉、神经和结缔组织)。
体外循环(ECC)
ECC的动脉流入线呈三叉状。
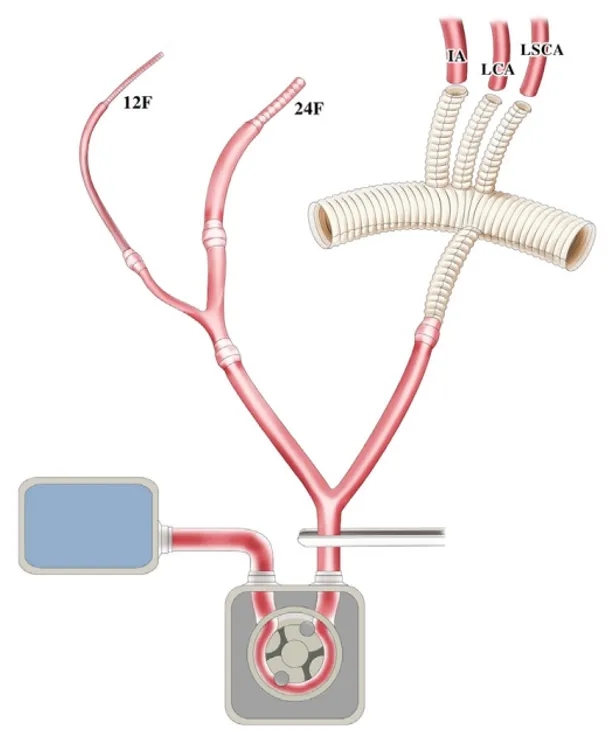
ECC装置
动脉插管与LCA吻合
LCA或IA均可作为动脉插管部位。本例选择LCA,使用3/0 PROLENE缝线对LCA根部进行褥式缝合,固定近端及远端后,从前方打开LCA四分之三,将24-F动脉插管送入LCA真腔,插入主动脉弓并连接到ECC回路。该导管在吻合期间将血液引流至LCA远端,并在ECC启动后用做灌注导管。
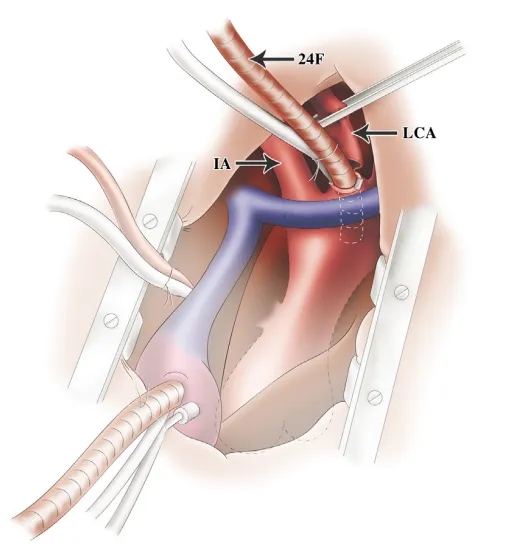
离断LCA,将24-F动脉插管插入主动脉弓
随后立即将12-F动脉插管插入LCA以维持远端血流,然后将LCA与第二臂吻合,24-F动脉插管在吻合过程中维持LCA远端血流。
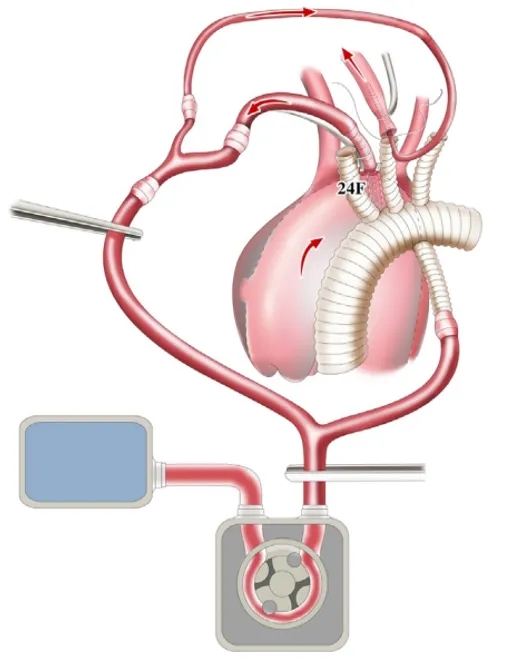
将12-F动脉插管插入离断的LCA以维持远端血流
完成后,取出12-F动脉插管,打结。松开移植物上的一个夹子,但穿过泵头的夹子保持原位,LCA血流通过导管-移植物-LCA环路恢复。
IA吻合
离断IA,插入12-F动脉插管以维持远端血流,随后将IA与第一臂吻合。完成后,取出12-F动脉插管,打结。IA血流通过导管-移植物-IA环路恢复。
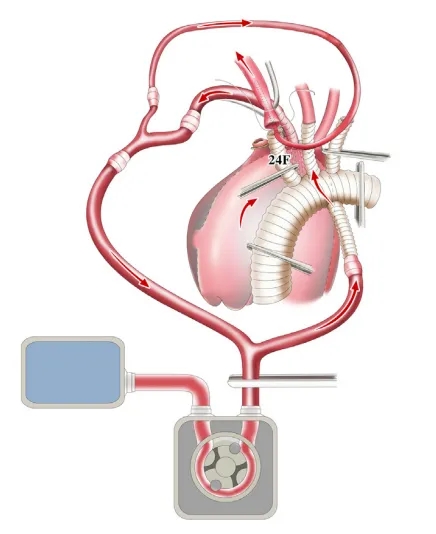
离断IA并插入12-F动脉插管
LSCA吻合
由于IA和LCA已灌注,因此在未插入12-F动脉插管的情况下,将LSCA与第三臂吻合。
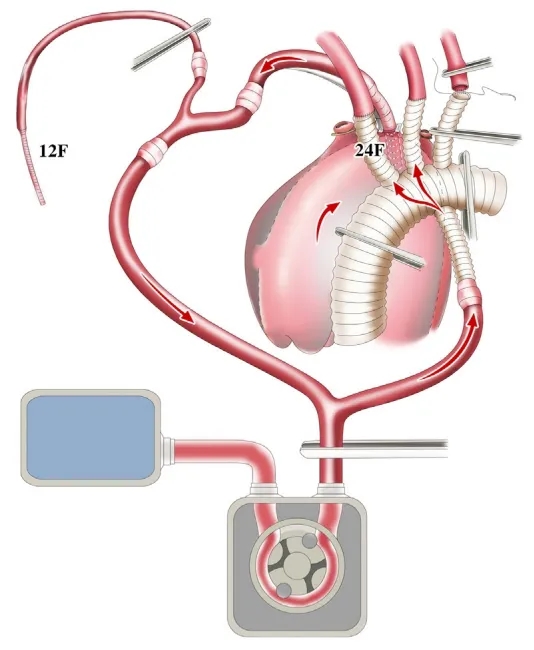
在不使用ECC情况下,将LSCA与第三臂吻合
在整个去分支的过程中,脑灌注由心脏泵血维持,无需ECC。在ECC启动前,于泵头前放置一个夹子。
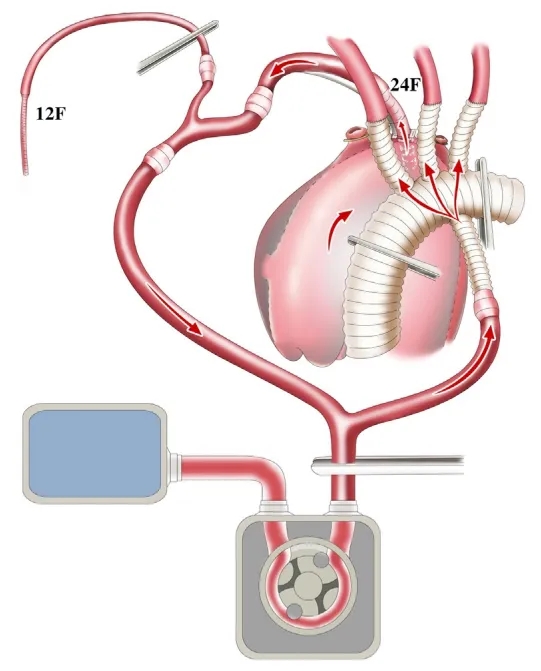
在阻断主动脉并启动ECC前
已完成主动脉弓上分支血管的重建
主动脉根部重建
完成去分支化操作后,撤除泵前夹子。启动ECC并进行全身降温,目标膀胱温度为28℃。采用24-F动脉插管为下半身供血,而移植血管灌注支,则供应上半身。随后阻断主动脉,经冠状动脉开口灌注组氨酸-色氨酸-酮戊二酸心脏停搏液,保留患者自体主动脉根部,并采用“三明治”夹层修复技术完成窦管交界处重建。
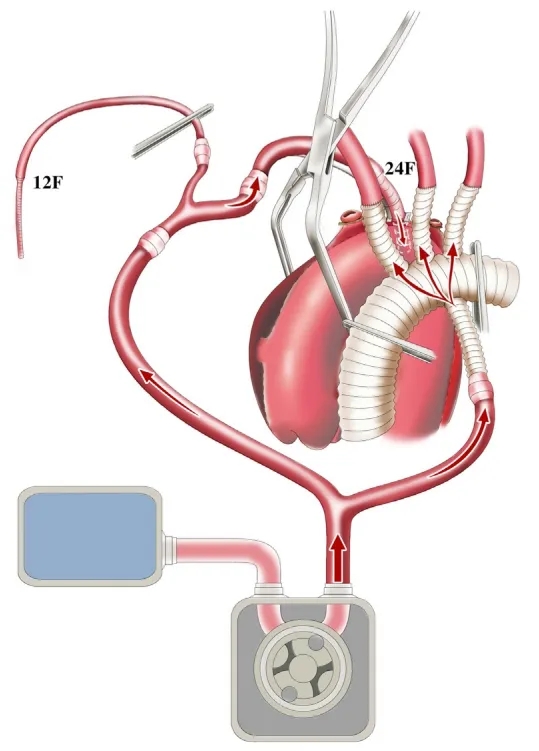
下半身停循环深低温期间,维持全身性脑灌注
采用冷冻象鼻技术行主动脉弓修复术
当膀胱温度降至28℃时,切开主动脉弓,在全身脑灌注条件下启动下半身深低温停循环(HCA)。灌注流量维持在5~8 mL/(kg·min),桡动脉平均压控制在30 mmHg左右,脑氧饱和度保持在60%以上。采用冷冻象鼻技术,将一枚直径28 mm的覆膜支架置入降主动脉。随后运用三明治技术(以覆膜支架上端作为内衬,毡条作为外层)将主动脉弓残端与分支人工血管进行吻合。
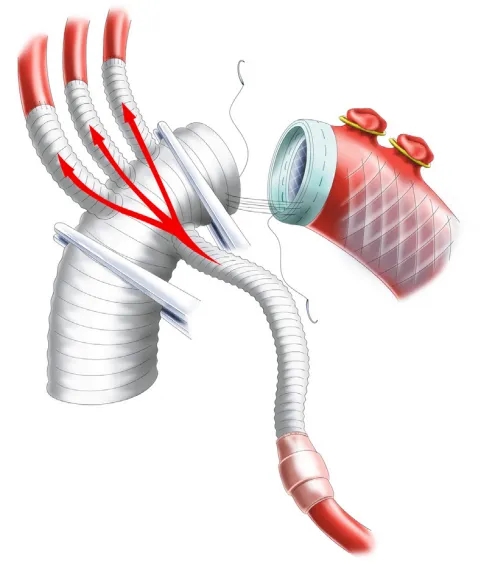
主动脉弓修复期间,保持全脑灌注
手术完成
完成主动脉弓吻合后,撤除分支人工血管远端的夹子,恢复下半身血流,随后开始复温。将分支人工血管近端修剪后,与近端管状人工血管吻合并排气。随后释放夹子,患者心脏恢复搏动,停止ECC。按常规方式关胸。
ECC、主动脉阻断及HCA时间分别为135分钟、92分钟和22分钟。患者于术后6小时意识恢复,次日拔除气管插管,7天后顺利出院,无任何并发症。术后随访3年,患者日常生活正常。手术全程见视频1。
视频1
TAR术后常并发脑、脊髓等重要器官缺血性损伤,导致较高的院内死亡率和并发症发生率。作为传统TAR的替代方案,分支优先重建技术已被引入。肖苍松教授团队在此基础上提出一种新型的CPFT技术,其关键改进在于:分支操作期间保持脑灌注不中断,并在HCA阶段实现全脑灌注。
该研究发现,(1)通过开放的LCA或IA起始部置入24-F动脉插管至主动脉弓真腔,具有操作合理、简便、耗时短(约1分钟)等优点。然而,若动脉存在夹层,置管则较为困难,研究排除了此类病例。(2)12-F动脉插管可通过提供持续性远端血流,避免因侧支循环不足或Willis环不完整所致的缺血风险。此时由患者自体心脏维持远端灌注,模拟生理性脑循环模式,无需依赖ECC。(3)CPFT技术可在HCA期间通过脊髓前动脉与脊髓后动脉维持脊髓血供。在在28℃低温下,22分钟的HCA时间对内脏缺血安全可控,使得采用浅低温停循环成为可行。(4)在ECC策略上,要求心肺旁路流量为5~8 mL/min,桡动脉压<30 mm Hg,以及脑血氧饱和度超过60%,此时,既可保障全脑灌注,又能避免灌注不平衡的潜在风险。
文献来源:
1.Xiao C, Chi H, Wang J, et al. Cerebral perfusion-first techniques in total arch replacement for Stanford A aortic dissection. JTCVS Tech. 2025 Apr 29;32:43-46. doi: 10.1016/j.xjtc.2025.04.005.
· END ·
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系


发表留言
暂无留言
输入您的留言参与专家互动