荣登ESMO IO大会LBA口头报告,安罗替尼联合免疫检查点抑制剂为晚期NSCLC提供新治疗策略
肺癌是我国发病率和死亡率最高的恶性肿瘤,每年新发病例超过781,000例[1],非小细胞肺癌(NSCLC)约占85%[2]。相对于驱动基因阳性NSCLC患者有精准的靶向治疗,驱动基因阴性NSCLC在治疗上存在很大的难点,尤其是后线的治疗。
由欧洲肿瘤内科学会(ESMO)组织召开的2021年ESMO免疫肿瘤学大会(ESMO IO)于近日召开,其中,由上海交通大学附属胸科医院韩宝惠教授和天津医科大学肿瘤医院李凯教授主导的安罗替尼联合TQ-B2450(PD-L1单抗)二线治疗驱动基因阴性晚期NSCLC的多中心、随机、双盲临床研究在大会上进行了口头报告,让我们看到了免疫联合抗血管生成治疗在驱动基因阴性晚期NSCLC治疗上的新突破。
二线联合方案是驱动基因阴性晚期NSCLC治疗的大势所趋
近年来,免疫单药治疗为PD-L1表达阳性的驱动基因阴性NSCLC患者带来更好的生存获益,而联合治疗模式更是起到了增效作用,成为所有驱动基因阴性晚期NSCLC患者(无论PD-L1阴性还是阳性)的治疗趋势。
韩宝惠教授表示,如何使PD-L1阴性的NSCLC患者适合于免疫治疗是最终需要解决的问题。未来驱动基因阴性NSCLC二线及以上的治疗,总生存期(OS)的提高需要借助于联合治疗,而联合治疗策略主要有以下几个方向:
一是在免疫治疗的基础上联合化疗,这种联合需要特别关注安全性。
二是免疫联合抗血管治疗,对于一线化疗耐药的患者,二线再联合化疗会使毒性增加且未必有效,这时需要变更治疗策略,而抗血管生成药物可能是免疫治疗最佳的搭档。
免疫和抗血管生成药物联合具备治疗上的协同作用:
- 首先,联合使用控制了肿瘤血管的生成,使得血管正常化,从而可以让更多的大分子PD-1/L1单抗进入肿瘤微环境,发挥作用;
- 其次,抗血管生成药物在抑制VEGF的同时,还可以上调PD-L1的表达,使免疫治疗药物发挥更大效力;
- 最后,抗血管生成药物阻断了VEGF,也解除了免疫细胞的抑制状态,增强了人体的免疫功能。
这种免疫联合抗血管生成药物的“去化疗”(Chemo-free)方案具有较好的发展前景。在抗血管生成药物的选择中,既有大分子单抗药物,又有小分子的酪氨酸激酶抑制剂。而小分子的酪氨酸激酶抑制剂可能会比大分子单抗药物(如,贝伐珠单抗)效果更好。
三是双免疫治疗,双免疫治疗的毒性比较大,可能有更大安全隐患,而且目前疗效并不比免疫联合抗血管生成药物更好。
基于以上观点,抗血管生成药物联合免疫是未来研究的重要方向。
包括NSCLC在内的几乎所有肿瘤中,二线治疗似乎都面临着一定的难点。这是因为二线治疗时,肿瘤已经产生不同程度的耐药,疗效相较于一线治疗大打折扣,所以二线治疗的要点在于克服耐药。
李凯教授表示,由于患者经过一线治疗,已经对化疗药物耐药,“chemo-free”模式可能是克服耐药的突破口。而在“chemo-free”模式当中,免疫联合抗血管生成药物似乎是最有希望的。然而,并不是所有的抗血管生成药物联合免疫治疗都尽如人意,例如IMpower150研究的最终分析结果显示,免疫+抗血管+化疗(A组)与免疫+化疗(B组)的中位OS仅有0.5个月的差异。
而安罗替尼既可以作用于肿瘤细胞本身,也可作用于肿瘤微环境,同时又是多靶点抗血管生成药物,从机制上来说,在联合免疫治疗时是最有可能起到协同增效作用的药物。
受到这个启示,韩宝惠教授和李凯教授发起了安罗替尼联合TQ-B2450二线治疗驱动基因阴性晚期NSCLC的多中心、随机、双盲临床研究,以挖掘最佳“chemo-free”治疗模式组合。
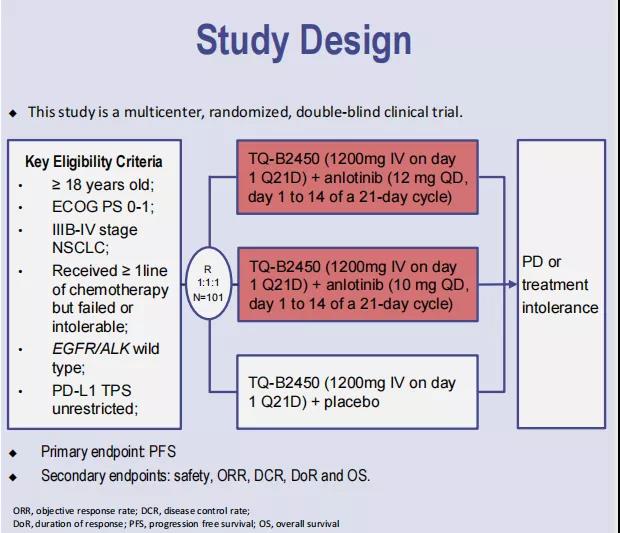
图1 研究设计
安罗替尼联合TQ-B2450二线治疗驱动基因阴性晚期NSCLC的多中心、随机、双盲临床研究共纳入101例患者,随机分为TQ-B2450+安罗替尼12mg QD(n=34)、TQ-B2450+安罗替尼10mg QD(n=34)以及TQ-B2450单药组(n=33)。
韩宝惠教授介绍道,截至2021年10月14日,中位随访11.1个月,TQ-B2450+安罗替尼(n=68)与TQ-B2450单药组(n=33)中位无进展生存期(PFS)分别为6.9个月vs 2.7个月(HR=0.43,0.25-0.73,P=0.0014 )。这意味着安罗替尼的加入,将中位PFS从2.7个月提高到6.9个月,获益幅度达到了4.2个月,结果非常令人满意。两组中位PFS的HR为0.43,相较于TQ-B2450单药,TQ-B2450+安罗替尼降低了57%的疾病进展或死亡风险。
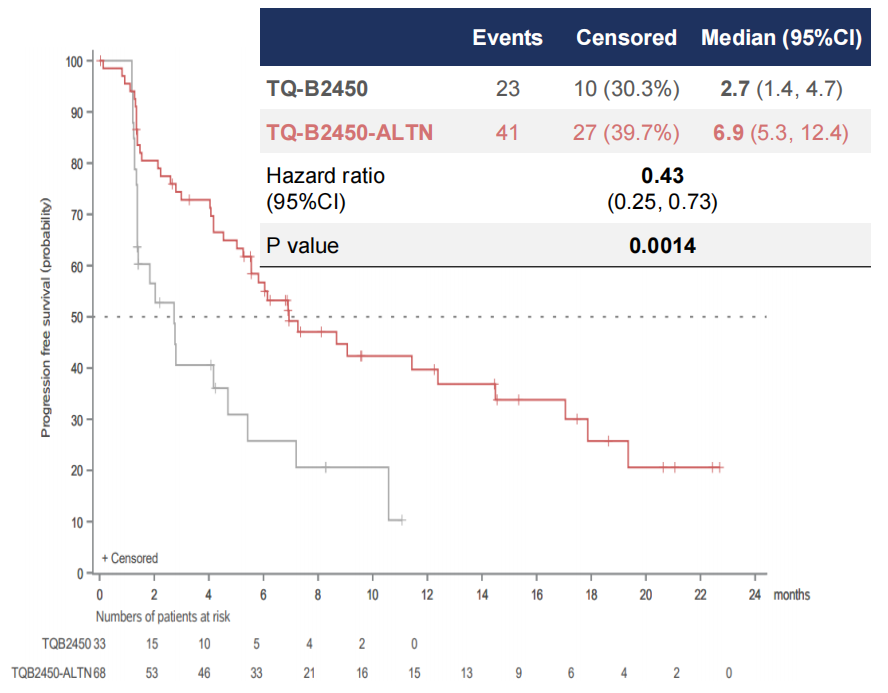
图2 PFS结果
该研究最终的OS数据,还有待长期随访。该组合能否将PFS获益转化为OS获益,值得期待。
安全性方面,大多数的不良反应均为1~2级,3级以上的不良反应包括高血压、高甘油三酯血症和疲乏等,而且是可逆可管理的,整体来说耐受性良好。
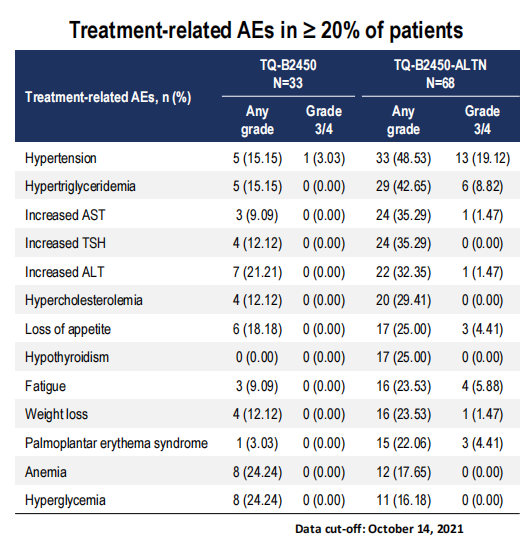
表1 安全性结果
步履不停,冲击一线;探索不止,未来可期
“好药用在一线上”已经成为不争的事实,安罗替尼联合TQ-B2450在二线治疗上已经取得较好的疗效,目前国内专家学者也积极布局其在一线治疗的临床试验。韩宝惠教授介绍,安罗替尼联合信迪利单抗一线治疗驱动基因阴性晚期NSCLC的探索性研究结果,在2019年和2020年世界肺癌大会(WCLC)上进行了口头报告,也同步发表在Journal of Thoracic Oncology(JTO)杂志上,结果显示[3],安罗替尼联合信迪利单抗一线治疗晚期NSCLC患者的PFS达15个月。在这样的研究结果基础上,相信安罗替尼联合TQ-B2450在一线上也能取得更好的效果。
目前,安罗替尼联合TQ-B2450对比帕博利珠单抗治疗PD-L1表达阳性的驱动基因阴性晚期NSCLC的III期临床研究已经启动,计划入组300余例患者,希望该组合能够为将来驱动基因阴性晚期NSCLC患者一线治疗提供一个新的循证医学证据。
李凯教授也指出,TQ-B2450与安罗替尼是正大天晴的两大拳头产品,正大天晴正广泛探究 TQ-B2450与安罗替尼联合疗法在各癌种中的疗效,目前已经启动多项 III 期临床研究,其中包括针对局部晚期(IIIB/IIIC 期)、转移性或复发性(IV 期)NSCLC以及广泛期SCLC、晚期肾细胞癌、晚期三阴性乳腺癌等研究,期待后续该组合在不同癌种中取得好的疗效。
除了疗效和安全性,药物的可及性也是患者非常关注的一点。根据近期国家医保局公布的《2021年版国家医保药品目录》的最终调整目录,安罗替尼治疗甲状腺髓样癌新适应症进入医保,目前在我国获批的4个适应症(非小细胞肺癌、小细胞肺癌、软组织肉瘤、甲状腺髓样癌)都进入了医保,让更多的老百姓用的起好药,凸显正大天晴的社会责任感。
李凯教授表示,“作为一个好药,需要满足以下几点要求,一是要能独当一面,即有确切的疗效;二是可作为良好的搭档,不仅独当一面,而且可以为其他药物增效;三要毒性可耐,毒性越小越好;四是应用宽广,在各个癌种都能展现很好的疗效;最后是物有所值,患者能负担得起。如果一个药物能同时具备独当一面、良好搭档,毒性可耐、应用宽广、物有所值,必然会众望所归。而安罗替尼有承担起这种责任的内涵和潜力。
安罗替尼是我国自主研发的小分子多靶点酪氨酸激酶抑制剂,能够全面、强效抑制多个血管生成相关激酶(VEGFR、PDGFR和FGFR)和肿瘤生长相关激酶的活性,从而显著抑制肿瘤血管新生的同时,阻断肿瘤细胞增殖、迁移,为此带来显著改善肿瘤免疫微环境的作用[5,6]。安罗替尼在2018年的上市是中国创新药物的骄傲,至今已经惠及许多国内肿瘤患者。
参考文献:
[1]Chen WQ, Sun KX, Zheng RS. Report of cancer incidence and mortality in different areas of China, 2014. China Cancer. 2018;27:1e14.
[2]Kilgoz HO, Bender G, Scandura JM, et al. KRAS and the reality of personalized medicine in non-small cell lung cancer. Mol Med. 2016;22:380e387.[3]https://doi.org/10.1016/j.jtho.2020.11.026.[4]《2021年版国家医保药品目录》[5]C Xie,X Wan,H Quan et al. Preclinical characterization of anlotinib, a highly potent and selective vascular endothelial growth factor receptor-2 inhibitor[J]. Cancer Sci,2018,109(4):1207-1219.[6]B Lin,X Song,D Yang et al. Anlotinib inhibits angiogenesis via suppressing the activation of VEGFR2, PDGFRβ and FGFR1[J]. Gene ,2018,654:77-86.
来源:医学界肿瘤频道,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。
