经导管缘对缘修复术对继发性二尖瓣反流患者接受以指南为导向的药物治疗上调的影响
继发性二尖瓣反流(SMR)是射血分数降低(HFrEF)的心力衰竭(HF)患者中最常见的瓣膜性心脏病,与患者不良预后相关。COAPT研究是第一项证明经导管边缘对边缘二尖瓣修复术(M-TEER)对慢性HFrEF患者症状和预后有益的前瞻性随机试验。欧洲心脏病学会当前关于HF患者管理的指南建议在与COAPT入组患者具有相似特征的患者中考虑M-TEER(IIa类推荐,证据水平:B)。尽管如此,在评估M-TEER之前,这些患者还必须接受优化的指南指导的药物治疗(GDMT)。事实上,GDMT可能会改善高达40%的HFrEF患者的二尖瓣反流(MR)严重程度,而尽管接受GDMT,SMR的持续存在与HF住院或死亡的相对风险增加近2倍相关。
近期几个注册研究证实,在高比例的HFrEF患者中,GDMT的使用和剂量仍然不足,这可能会对临床结果产生影响。低血压和肾功能不全是HFrEF患者治疗不足的主要原因。可以假设,M-TEER增加全身心输出量,可以改善血液动力学,对血压和肾功能产生有益影响,从而优化GDMT。目前M-TEER对GDMT的影响尚不清楚,因此,本研究目的是探究在SMR和HFrEF患者中,M-TEER后GDMT上调的比例,预后意义和预测因子。
1. 研究人群
这是一项对2008年11月至2021年1月从EuroSMR注册中心收集的前瞻性数据所进行的回顾性分析。所有患者均接受GDMT治疗,并在多学科心脏团队讨论后被认为适合接受M-TEER进一步治疗。根据本研究目的,只纳入HFrEF(左心室射血分数≤40%),并且在基线和6个月的随访中都有完整的GDMT数据的患者。
2. 指南指导的药物治疗(GDMT)
在纳入的患者中,检查是否使用以下3类药物:RAAS系统阻滞剂(RASI[ACEI/ARB/ARNI])、β受体阻滞剂、及醛固酮受体阻滞剂(MRA)。值得注意的是,在研究期间,钠-葡萄糖共转运体2抑制剂(SGLT2i)并未常规应用于临床。根据GDMT是否上调对患者进行分组,GDMT上调的定义是启用一种新的HF药物类别和/或增加先前使用的至少一种药物类别的剂量,而不下调任何其他药物类别。本研究对M-TEER后上调GDMT vs未上调的患者人群进行分析,并对于每一类药物,研究了上调与未调整的患者分层。药物剂量以当前指南中建议的目标剂量的百分比来衡量。
3. 随访及研究终点
对术后6个月的患者进行随访,包括生命状态、HF住院时间、药物治疗、纽约心脏协会(NYHA)功能分级和NT-proBNP测定。更长时间的随访通过门诊、电话或医院记录来评估。主要研究终点是全因死亡和全因死亡或HF住院的复合事件。
三、研究结果
共纳入810名患者。M-TEER后307名患者(38%)GDMT上调,503名患者(62%)无GDMT上调。
1. 基线信息分析
基线信息分析发现,M-TEER后GDMT升高的患者倾向于非男性,有心肌梗塞病史,平均动脉血压较高,肺动脉收缩压较低,肾功能较好或接受较低剂量的利尿剂,右心室收缩末期直径较小。(表1)

2. 随访结果
(1)与基线相比,接受3种药物类别(ACEI/ARB/ARNI、β受体阻滞剂和MRA)的患者比例均有所增加。在M-TEER后接受>50%目标剂量的ACEI/ARB/ARNI、β受体阻滞剂和MRA的患者比例仍然较低,尽管与基线相比有所增加。ACEI/ARB/ARNI的上调率为30.1%,β受体阻滞剂为24.8%,MRA为20.7%。(图1)
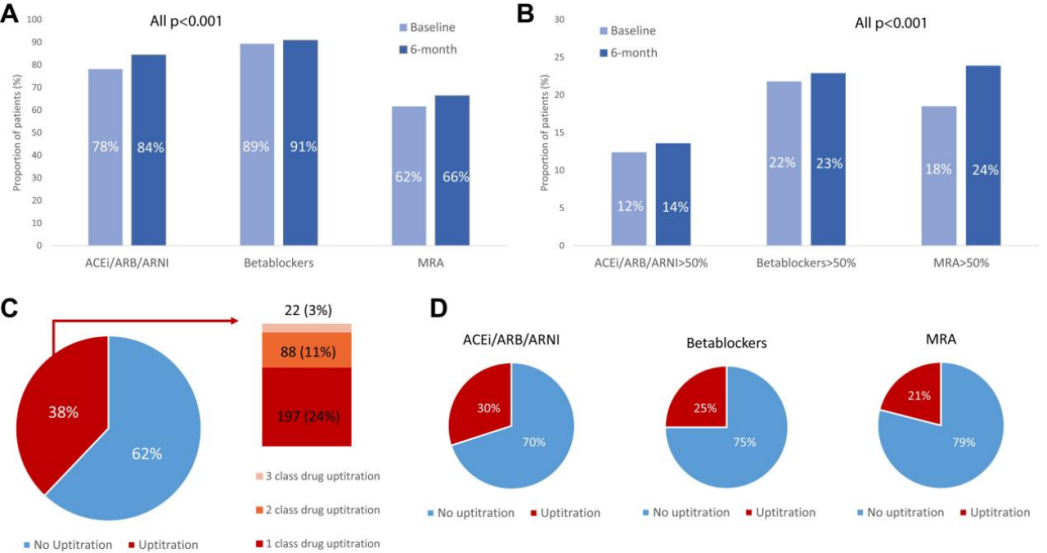
(2)与无GDMT上调的患者相比,GMDT上调的患者术后MR水平,NYHA分级及NT-proBNP下降程度更大(表2)。M-TEER后GDMT升高的患者与未升高的患者相比,3年随访时的无全因死亡生存率,无全因死亡或无HF住院复合事件的生存率更高。(图2)

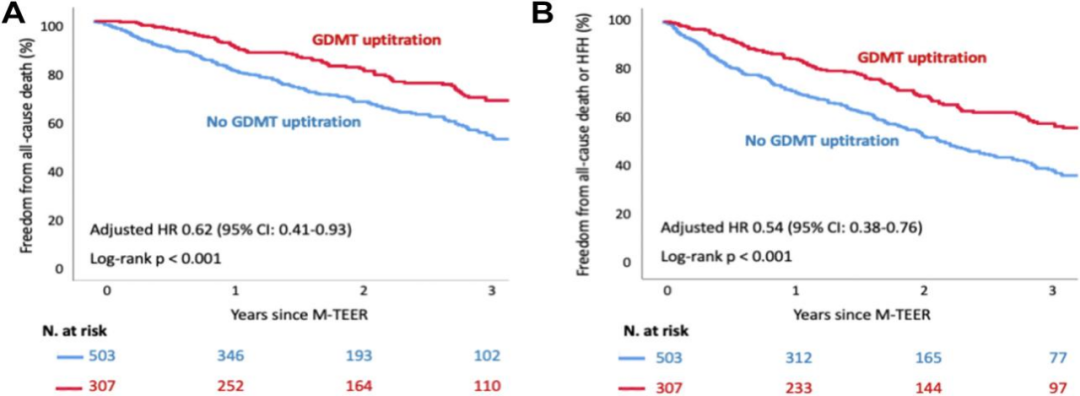
图2 3年随访生命曲线
(3)在多变量分析中调整其他变量后,GDMT升高患者的低全因死亡风险和低复合终点风险仍然显著。具体为:与GDMT未上调的患者相比,GDMT上调的患者全因死亡(调整后HR:0.62;95% CI:0.41-0.93;P = 0.020)和全因死亡或HF住院复合事件风险下降(调整后HR:0.54;95% CI:0.38-0.76;P < 0.001)。(补充表1)

3. 与GDMT上调相关的因素
从基线到6个月随访的MR降低程度(3或4度vs <3度)是唯一与M-TEER 后GDMT上调的可能性独立相关的变量(调整后的OR:1.71;95% CI:1.08-2.71;P=0.022)。(表3)

四、总结
在接受M-TEER的HFrEF和SMR患者中,超过三分之一的患者在手术后6个月观察到GDMT上调。M-TEER后GDMT的上调与临床事件风险降低独立相关。M-TEER后,MR严重程度的大幅下降是GDMT上调的一个主要相关因素。
经导管缘对缘修复(TEER)治疗二尖瓣反流是近年来结构性心脏病治疗邻域的热点领域,众多基于这一技术的临床研究结果表明了其在改善二尖瓣反流及患者预后中的作用,使其成为了目前指南唯一推荐的二尖瓣反流治疗介入技术。
相较于原发性二尖瓣反流(PMR),TEER技术在继发性二尖瓣反流(SMR)的应用效果起始于质疑。MITRA-FR研究结果未能得出阳性结论,但在研究设计、入选标准、执行程度等层面更为严格的COAPT研究得出了TEER在治疗SMR中的阳性结论,其结果也得到了更为广泛的认同。COAPT研究在2018年发表了的其主要结论,与单纯最大化指南推荐的药物治疗(GDMT)相比,TEER联合GDMT可减少外科手术高风险、左心室功能不全的中重度及重度SMR患者2年的心衰再住院及全因死亡发生率。2021年COAPT研究发表了3年的随访结果,TEER持续有助于改善患者二尖瓣反流严重程度、生活质量和能力。58例患者从单纯GDMT组转为接受TEER治疗,其死亡和心衰再住院复合重点发生率与继续单纯GDMT治疗的患者相比有明显的降低。基于COAPT研究结果,各大学术指南均提高了TEER治疗SMR中的应用推荐,对推广这一技术的临床应用也起到了巨大的作用。在2023年ACC会议上,COAPT研究公布了5年的随访结果,TEER技术的安全性得到了进一步验证。在5年的随访中,TEER组73.6%的患者发生死亡或心衰再住院,但仍明显优于对照组的91.5%。
临床上心功能不全患者数量巨大,多数长期心衰患者伴随着左心室重构,后者是导致SMR的重要原因。对于这部分患者的治疗,GDMT是目前公认的、改善患者预后的基石策略。需要指出的是,GDMT的落实不能仅停留在形式上,要真正改变患者预后,“最大化”是一个关键步骤。然而,合并心功能不全的严重二尖瓣反流患者往往伴随低血压等临床表现,包括药物类型和剂量最大化的GMDT很难被真正落实。本次介绍的研究另辟蹊径,回顾性分析了实施TEER治疗后患者GDMT的改善情况,并发现TEER治疗有助于上调对患者GDMT。也就是说,TEER治疗后可以更加规范和充分的对患者进行GDMT。毫无疑问,这将进一步有助于改善患者预后,也从另一个角度TEER治疗后患者预后改善的潜在原因。
基于此,我认为,在找到彻底解决心衰患者左室重构的治疗手段之前,对于解剖合适的严重SMR患者,TEER技术可安全、有效和快速的改善患者二尖瓣反流程度。在此基础上,患者也会获得更多机会接受“最大化”的GDMT,从而进一步改善其临床预后。与此同时,我们也应该清醒的认识到,TEER只是此类患者整体治疗中的一个步骤,绝非终点。在完成TEER治疗后,仍需要对患者进行严格的随访,并实施“最大化”GDMT。
采用指南推荐药物并滴定至最大耐受剂量,是对射血分数下降的心衰患者进行治疗并取得最大临床获益的基石。然后在临床实践中,多种原因导致了很大比例的患者没能接受GDMT及剂量上调。Savarese等人纳入2016年至2019年美国、英国和瑞典三国医疗信息系统中新开始使用药物治疗的心衰患者,12月后随访发现仅15~30%的患者达到了ACEi、ARB、倍他受体阻滞剂或ARNI药物的目标剂量,而且还有27~55%的患者停用了上述药物(Savarese G et al. Eur J Heart Fail. 2021;23:1499-1511. doi: 10.1002/ejhf.2271)。研究及临床实践经验都提示二尖瓣的不同程度反流、低血压和肾功能恶化等因素与GDMT不能上调相关。诚然,前期研究提示M-TEER增加全身心输出量,可以改善血液动力学,能改善患者低血压状态;此外,COPAT研究的事后分析也发现Mitraclip手术分别降低了66%和67%新发终末期肾病或需要肾脏替代治疗的风险(P≤0.011)。这些血流动力学参数的改善,很可能会增加患者对GDMT治疗的耐受性。然而,对SMR患者进行二尖瓣TEER治疗的大型随机对照研究——COAPT要求术前要对患者进行GDMT滴定并至最大耐受剂量,这一设定的理由很明确,因为部分SMR患者通过GDMT就能极大减少二尖瓣反流;但是,这一设定也使得COPAT研究实验组和对照组中都仅有极少数患者在入组后GDMT药物得到了进一步上调。那么,通过TEER治疗降低二尖瓣反流能否进一步促进GDMT上调并带来获益只能通过其他数据寻找端倪了。Adamo M新近通过回顾分析EuroSMR数据,结果给我们带来有益启示。
Adamo M等研究者从1159名合并HFrEF并进行了TEER治疗患者中,剔除数据不全的患者,最终分析了810名患者。TEER术前,98.5%的患者接受了GDMT治疗,但是仅有12.4~21.8%患者RAASi/ARNI、倍他受体阻滞剂或醛固酮受体拮抗剂达到目标剂量的一半以上。术后6个月时,38%患者上述药物剂量发生了上调。纳入基线时NT-proBNP水平、肺动脉收缩压、心梗病史、平均动脉压、eGFR水平、二尖瓣反流减少和MYHA心功能改善等多因素模型分析还发现,仅二尖瓣反流减少(减少3级以上)与术后6个月的GDMT上调相关。而且还发现,通过多因素矫正,GDMT上调都与全因死亡风险(HR: 0.62; 95% CI: 0.41-0.93; P=0.020)及全因死亡或心衰住院风险(HR: 0.54; 95% CI: 0.38-0.76; P < 0.001)下降相关。
当然,不可否认,这仅仅是对注册数据库进行的回顾性分析,我们无法确定是否存在其他伴随因素或者选择性偏倚的影响,更不能进行因果推断。但是这些发现仍具有临床及进一步研究意义:(1)对于明确不能通过药物治疗改善的SMR患者,是否可以不用等漫长的GDMT调整而尽早进行TEER治疗,TEER治疗是否可以让患者快速稳定并能更好的耐受GDMT上调?(2)术后再进行GDMT是否更简单并快捷并带来获益?(3)也就是说,对于心衰合并SMR患者,TEER与GDMT可能存在着协同作用,我们不应把TEER和GDMT看作是不同阶段患者的治疗方法。
文章来源:
JACC:Cardiovascular interventions.2023;16(8):896-905. DOI:10.1016/j.jcin.2023.01.362.
医谱app
扫码或者点击图片下载
微信公众号
扫码或点击图片关注
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。




发表留言
暂无留言
输入您的留言参与专家互动