汪宇鹏教授:小瓣环应用球扩瓣技术策略
瓣环较小患者的主动脉瓣狭窄(AS)治疗具有挑战性,可能导致假体-患者不匹配(PPM)。
在近期举行的“第二十届中国心脏大会(CHC)”上,北京大学第三医院汪宇鹏教授作“小瓣环应用球扩瓣技术策略”学术分享,医谱学术特将精华内容整理成文,供临床医生参考。
当正常功能的人工瓣膜的有效开口面积(EOA)与身体大小相比太小时,就会发生PPM,这导致瓣膜不能满足患者在休息和运动时的心输出量需求。此前有研究发现,PPM是远期死亡率的独立预测因子,与严重程度成比例,并与结构性瓣膜退化(SVD)的增加有关[1]。然而,后续的OCEAN-TAVI注册研究显示,Sapien 3和Evolut R治疗患者的全因死亡率相似,血液动力学表现在1年内没有临床差异,提示我们仍需要进行进一步的长期随访研究,以评估新一代瓣膜之间小瓣环主动脉瓣患者TAVR的真实血流动力学差异。
近期,球扩瓣与自膨瓣在小瓣环患者中的5年预后对比结果发布。Bern TAVI registry是一项前瞻性登记,纳入2012年1月至2021年6月期间,2769名连续接受TAVR治疗(CoreValve Evolut或SAPIEN THV) 的重度AS患者,共723名小瓣环患者(面积<430mm2)符合纳入标准。其中,389名患者接受了自膨瓣(环上游)THV治疗,334名患者使用了球扩瓣(环中瓣)治疗,排除VIV及纯反流的患者,最终倾向评分匹配结果为171对;研究主要终点基于VARC-3定义的器械成功率与技术成功率及5年内全因死亡率、卒中、出血等的复合终点[2]。

与球扩瓣相比,使用自膨瓣的患者在慢性肾脏疾病、外周动脉疾病和中度或重度二尖瓣反流中的发生率较低,但两组基线特征均无显著差异。
围术期情况
▪ 两者前扩无差异,自膨瓣比球扩瓣后扩占比更高(32.2% vs 19.9%;P>0.05);
▪ 总的来说,手术并发症很少,各组之间没有差异;
▪ 根据VARC-3定义,技术成功率均超过85%,且两组之间没有差异(87.1% vs 87.7%;P>0.05);器械成功率也无差异(79.5% vs 79.5%;P>0.05);
▪ 有效瓣口面积(EOA):自膨瓣 VS球扩瓣:1.81±0.46 cm2 vs 1.49±0.42 cm2;P<0.001;
▪ 平均跨瓣压差:自膨瓣 VS球扩瓣:8.0±4.8 mm Hg vs 12.5±4.5 mm Hg;P<0.001;
▪ PPM与中重度PPM:自膨瓣比球扩瓣发生率低(P<0.001);
▪ 两组中度或重度瓣周漏(PVL) (4.19% vs 1.2%;P=0.174)均罕见,轻度和中度PVL,自膨瓣发生率高于球扩瓣(P1/4=0.015)。
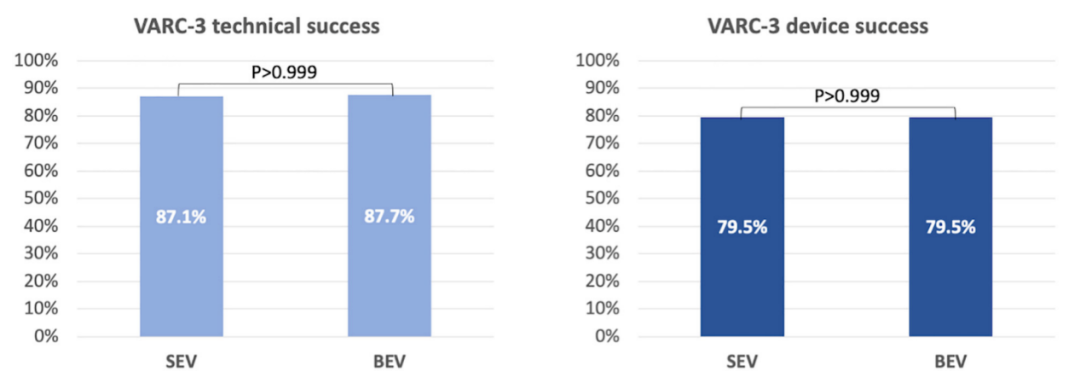
两组间相似的技术成功率和器械成功率
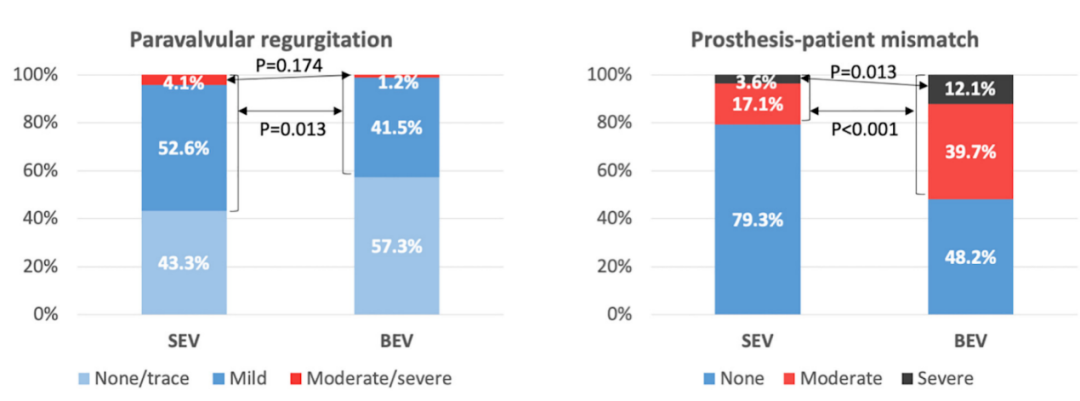
两组间PVR和PPM的差异
临床结局
30天随访:在死亡率、中风、严重或危及生命的出血、主要血管并发症和心力衰竭症状(NYHA功能分级)等方面无显著差异,自膨瓣患者比球扩瓣患者具有更高的永久性起搏器植入率(20.6% vs 8.3%,HR:2.68,P=0.002)。
1年和5年随访:在死亡率、任何中风、心肌梗死和严重或危及生命的出血的发生率、残余心力衰竭症状(NYHA功能III/IV级)等临床结果中,自膨瓣与球扩瓣的发生率无显著差异;致残性卒中,自膨瓣的发生率高于球扩瓣(1年 5.4% vs 0.6%,HR:9.07,p=0.038;5年 6.6% vs 0.6%,HR:10.01,P=0.030)。
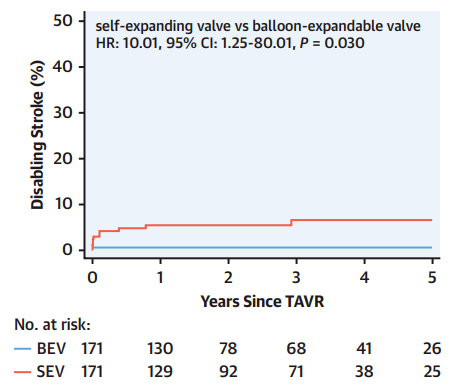
两组间致残性卒中的差异
IPTW分析:在1年和5年中,自膨瓣与球扩瓣相比临床结果没有差异,除了自膨瓣的致残性中风的发生率较高(5.3% vs 2.0%,HR:2.38)。
需要注意的是,这种差异在30天时就已经非常明显(2.8% vs 0.9%;HR:2.72;P=0.009)。30天及五年结果均表明,自膨瓣患者的任何中风发生率都高于球扩瓣患者(分别为4.2% vs 2.1%;HR:1.77;P=0.030和8.3% vs 5.8%;HR: 1.47;P=0.047)。
该研究在讨论部分提到,TAVR人群中PPM的发生率和其对临床的影响仍然是一个争论的主题,因为在记录PPM的方法上存在差异。早期在SAVR人群中的研究普遍表明,严重的PPM对临床结果有显著影响。这些研究中的PPM是基于Predict-EOA,而非Measured-EOA。在最近一项针对TAVR人群的研究中,与Measured-EOA相比,使用Predict-EOA降低了PPM的严重程度。在本研究中,两种器械中都没有记录严重的“预测”假体与患者不匹配的发生率。
此外,LVOT截面积呈椭圆形而非圆形,与心脏计算机断层扫描(CT)相比,使用TTE进行测量时,将LVOT截面当作是圆形,得到的LVOT面积会减少了17%。考虑到所有这些因素,使用多普勒超声心动图可能低估了这两种器械的血流动力学性能,即使是小瓣环患者使用环中瓣治疗,临床上有诊断意义的高压差和重度的PPM可能不太常见。
总之,PVL、起搏器、测量方式、卒中等都可能对预后产生影响,在长达5年小瓣环患者的研究中,自膨瓣超声心动图的血流动力学优势并没有转化为更高的VARC-3器械成功率或得到更好的临床获益,其自膨瓣组的致残性卒中发生率高于球扩瓣组(6.6% vs 0.6%;P=0.030)。因此,对于小瓣环患者,还是要根据其解剖结构和临床特征及患者全生命周期管理来选择合适的瓣膜。
1 随着TAVR术式的适应证逐渐向低手术风险和更年轻的患者拓展,进一步加强术后评估 (包括临床、心超和CT的评估)结果与长期预后间的关联性研究将是指导后续疗法发展的关键问题。
2 致残性卒中的发生率在两组间存在差异的原因值得探究。实际上,我们在其他研究(无论是否为小瓣环患者)中也可以看到类似的结果。
3 数据显示自膨瓣植入时需要更频繁的后扩,可能产生更多的微小脱落栓子,会造成短期(30天)卒中发生率升高。而且需要后扩的原因往往是由于瓣膜形态不好,由此导致的瓣叶工作不良可能在半年左右使得瓣叶周围发生血栓,导致术后长期(1年、5年)的卒中发生风险升高。
4 我们也需要注意到两组间基线的差异,自膨瓣组外周动脉疾病患病率较高,提示可能对卒中发生产生影响。
5 卒中的发生是否与术后抗凝治疗用药的个体化情况相关,也值得未来进一步探究。
TAVR术后PPM是否会影响临床结果目前仍不清楚,目前聚焦于小瓣环径患者的研究几乎都表明,具有更好的血流动力学表现的瓣膜并未带来更多的临床获益。
近年来,超声和导管测量压差带来的不一致越来越受到学界关注,如何定义“好的血流动力学”,是我们需要思考的问题。
参考文献
[1]Afonso B. Freitas-Ferraz, et al.Aortic Stenosis and Small Aortic Annulus--Clinical Challenges and Current Therapeutic Alternatives. Circulation 2019
[2]Okuno T, Tomii D, Lanz J, et al. 5-Year Outcomes with self-expanding vs balloon-expandable transcatheter aortic valve replacement in patients with small annuli[J]. Cardiovascular Interventions, 2023, 16(4): 429-440.
本文图片来自授课幻灯
本文为医谱学术原创文章,转载请标注来源
专家简介
- End -
关注我们
专业的心血管医生学术交流平台

医谱学术
扫码关注

医谱app
扫码下载
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。



发表留言
暂无留言
输入您的留言参与专家互动