学术分享丨丛洪良教授:《常用口服抗血小板药物不耐受及低反应性人群诊疗专家共识》解读
基于抗血小板治疗的疗效性和安全性呈现较大的个体差异,以及对于抗血小板药物不耐受高风险人群的识别、各类常规抗血小板治疗出现不耐受及低反应时的临床决策亟须具体指导性意见,《常用口服抗血小板药物不耐受及低反应性人群诊疗专家共识》应运而生,天津市胸科医院丛洪良教授在刚刚结束的武汉亚心国际心血管病论坛上对该共识进行了详细解读。

一、常用抗血小板药物不耐受类型及危险因素
(一)常用抗血小板药物不耐受类型
1.不耐受类型一:消化道损伤及出血
(1)阿司匹林通过局部和全身作用引起消化道黏膜损伤、出血
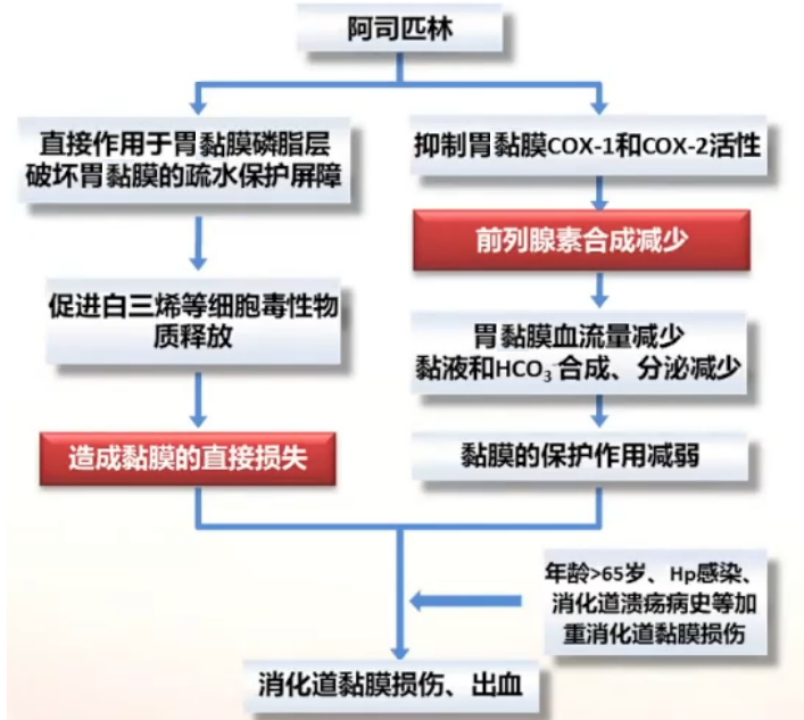
(2)氯吡格雷通过影响胃肠道黏膜损伤愈合导致修复受损、出血

(3)吲哚布芬胃肠反应少、出血发生率低
意大利多中心临床试验对5560例缺血性心脑血管疾病患者进行监测研究,每天服用吲哚布芬200-400mg,其中76%的患者至少连续治疗3个月。
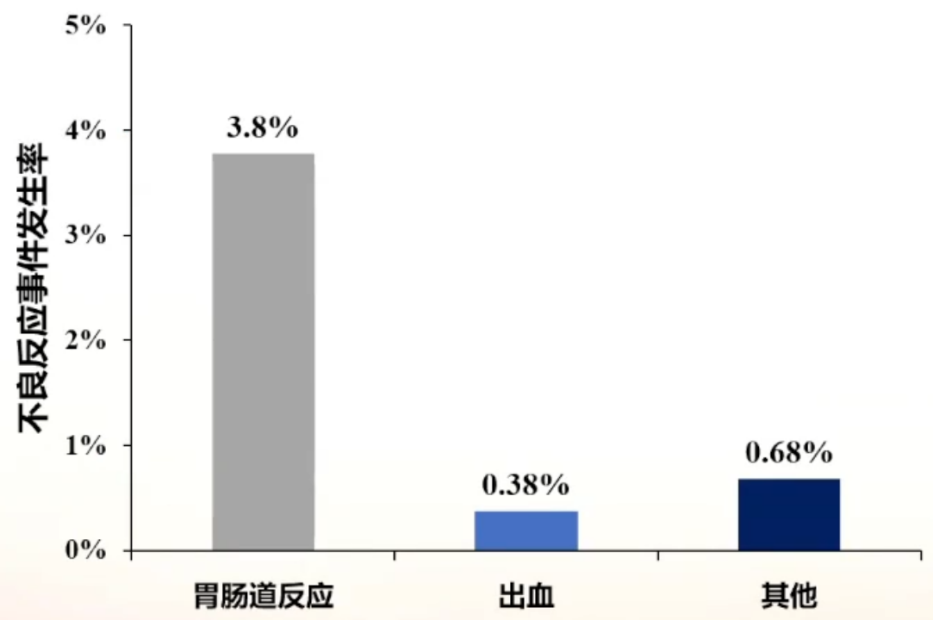
结果显示,仅3.9%患者出现不良反应,其中多为轻度胃肠道反应(3.8%),出血风险低(0.38%)。
2022年11月,复旦大学附属中山医院葛均波院士团队于Circulation发表关于OPTION试验(冠状动脉药物洗脱支架植入后吲哚布芬与阿司匹林的随机对照试验)的研究。结果显示,在接受药物洗脱支架植入术的心肌肌钙蛋白阴性的中国患者中,与阿司匹林+氯吡格雷DAPT相比,吲哚布芬+氯吡格雷DAPT可显著降低1年净临床结局风险。
一项纳入19项RCT,共5304名患者的荟萃分析得出的结论是吲哚布芬预防缺血性心脑血管病更安全。该研究结果显示,吲哚布芬对缺血性心脑血管疾病患者的心血管死亡、心肌梗死、卒中发生率等方面的作用与阿司匹林相当,但在总体出血、胃肠道反应等发生率则低于阿司匹林。
2.不耐受类型二:颅内出血
(1)荟萃分析:阿司匹林明显增加大出血和颅内出血发生率
15项随机对照试验,纳入165,502名受试者(阿司匹林组83,529例,对照组81,973例)进行分析。
与对照组相比,阿司匹林明显增加大出血风险(RR:1.5;95% CI:1.33-1.69)、颅内出血风险(RR:1.32;95% CI:1.12-1.55)和严重消化道出血风险(RR:1.52;95% CI:1.34-1.73)。
(2)替格瑞洛较氯吡格雷增加致命性颅内出血的发生率
PLATO研究:一项多中心、双盲、随机试验,比较了18,624名ACS住院患者分别服用替格瑞洛(90mg bid)和氯吡格雷(75mg qd)预防心血管事件的效果。
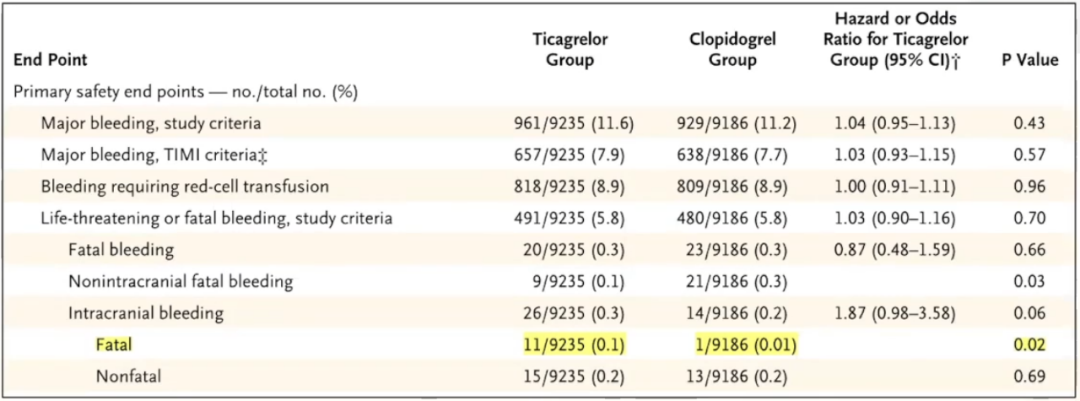
结果显示,替格瑞洛组与CABG无关的大出血发生率较高,包括致死性颅内出血的发生率。
3.不耐受类型三:其他部位出血
(1)氯吡格雷联合阿司匹林显著增加ACS患者的其他部位大出血发生率
CRUE研究:纳入12,562名NSTE-ACS患者,随机分为阿司匹林单药组或阿司匹林联合氯吡格雷用药组3-12个月。
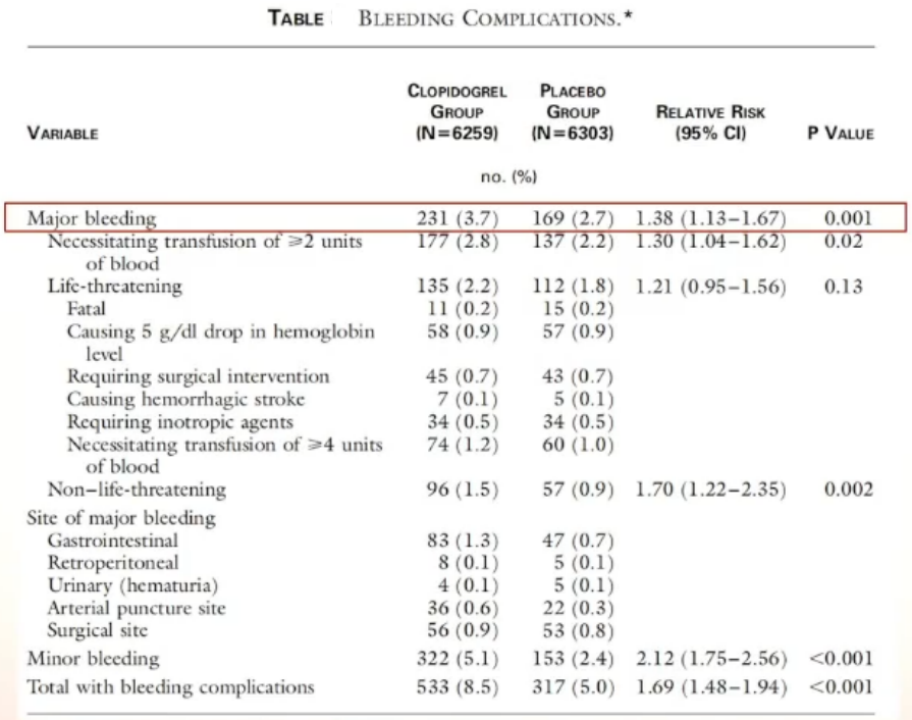
结果显示,对于ACS患者,氯吡格雷联合阿司匹林使大出血发生率从2.7%上升到3.7%(p=0.02)。
(2)替格瑞洛TIMI大出血风险明显高于氯吡格雷
KAMIR-NIH研究:纳入2011年11月至2015年6月期间8,010名接受成功血运重建的患者(1,377名患者服用替格瑞洛,6,633名患者服用氯吡格雷)。
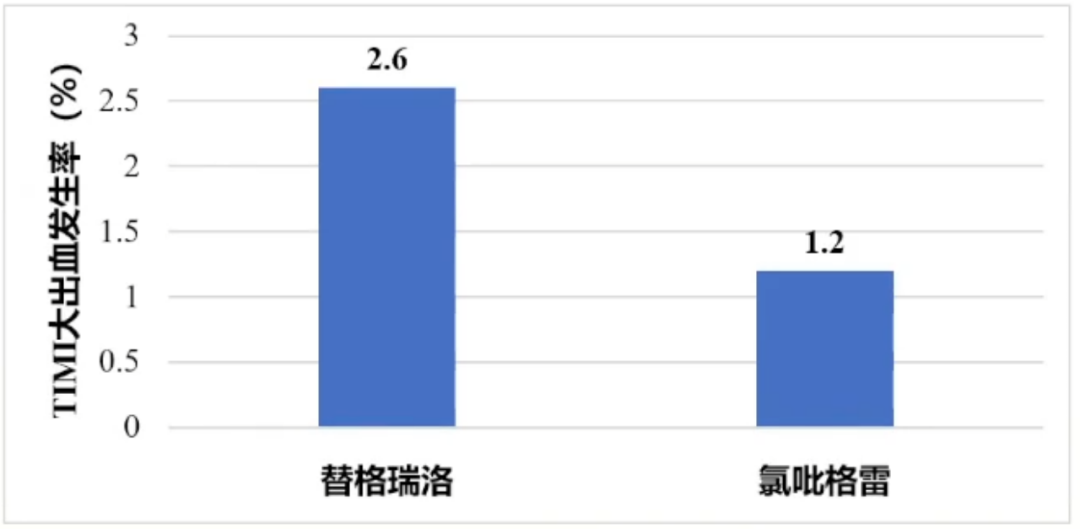
结果显示,替格瑞洛所致心肌梗死冠脉内溶栓(TIMI)大出血发生率明显高于氯吡格雷(2.6% vs 1.2%,p=0.008)。
4.不耐受类型四:痛风/高尿酸血症
(1)小剂量阿司匹林可引起血清尿酸水平增高和痛风复发
纳入49名老年住院患者(61-94岁),排除肾衰竭、高尿酸血症、痛风、出血史,或接受抗凝剂、阿司匹林或非甾体抗炎药的患者。阿司匹林用药如下:75mg/day(第1周)、150mg/day(第2周)、325mg/day(第3周)和0mg/day(第4周)。

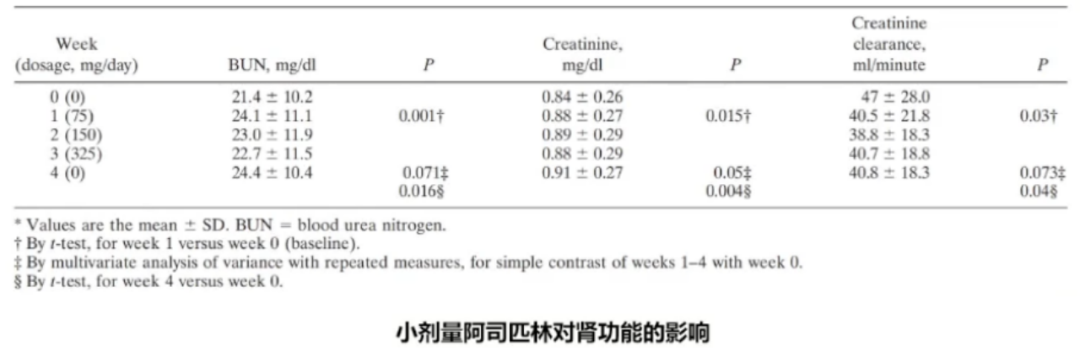
结果显示,①小剂量阿司匹林(75mg qd)能够显著升高老年人血尿酸水平,随着给药剂量增加,血尿酸水平可下降至接近基线水平。②小剂量阿司匹林能够显著升高老年人尿素氮,降低肌酐清除率。
(2)替格瑞洛显著增加既往MI患者痛风风险
PEGASUS-TIMI 54研究:一项随机、双盲、多中心对照临床研究,纳入1-3年前有过MI目伴有一项高危因素(65岁以上/糖尿病需要药物治疗/二次MI/多支冠状动脉病变慢性肾功能不全)的患者,按1∶1∶1随机分为3组,分别给予替格瑞洛90mg bid、60mg bid或安慰剂治疗,并同时给予包括阿司匹林<150mg/d在内的二级预防治疗。研究以心血管死亡、MI或卒中为主要疗效复合终点。
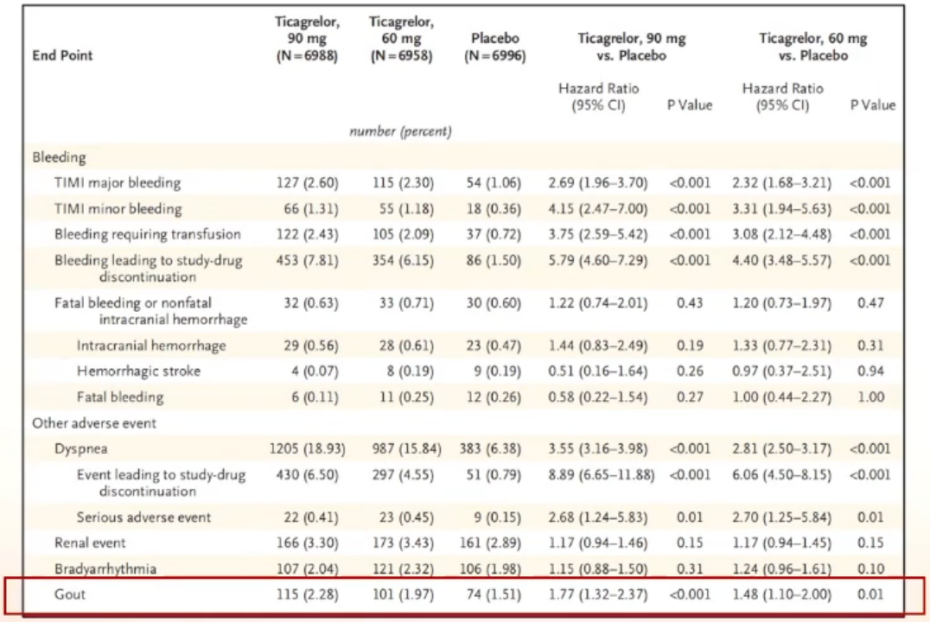
结果显示,替格瑞洛的痛风不良事件发生率明显高于安慰剂。
(二)导致不耐受风险增高的危险因素
1.导致不耐受风险增高的危险因素一:高龄
(1)≥70岁高龄患者使用阿司匹林时,严重消化道出血风险增加60%
一项ASPREE研究的亚组分析,纳入19,114例年龄≥70岁的高龄受试者,分为安慰剂组(n=9,589)和阿司匹林组(100mg qd,n=9,525)。
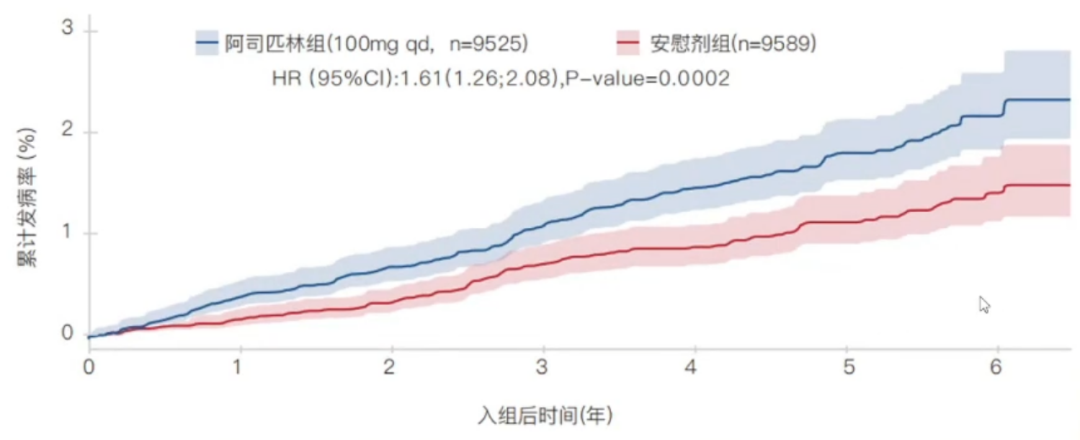
服用阿司匹林患者消化道出血事件显著增加了60%,其中上消化道出血增加87%,下消化道出血增加36%(P=0.0002)。
(2)阿司匹林所致消化道损伤风险将随年龄上升
一项人群队列研究,分为小剂量阿司匹林组(≤300mg/d,n=186,425)和安慰剂组(n=186,425),平均随访5.7年,主要终点是因为胃肠道大出血或脑出血住院。
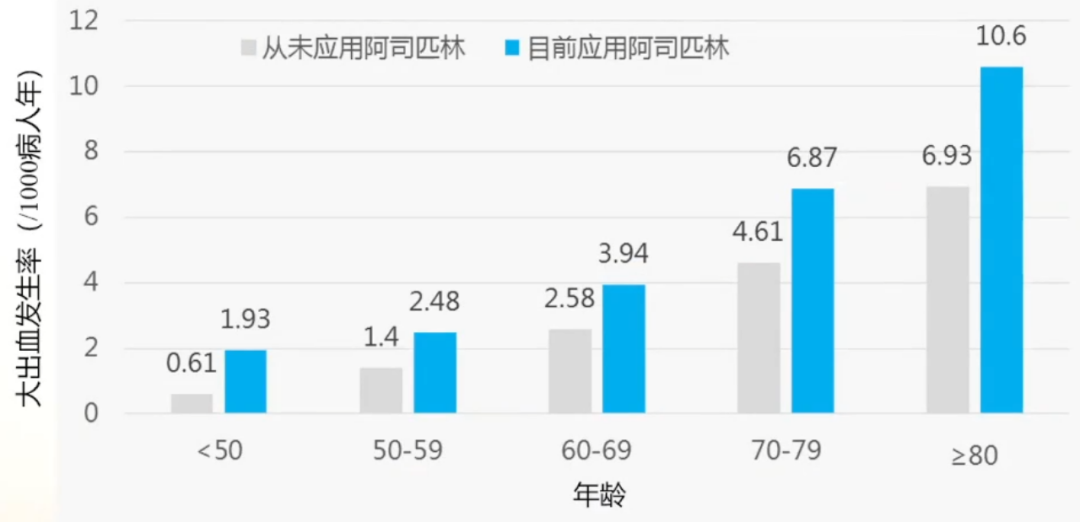
结果显示,在任一年龄段,服用阿司匹林均显著增加消化道出血风险,且消化道出血发生率随年龄升高逐步增加。
2.导致不耐受风险增高的危险因素二:高血压
(1)高血压患者脑出血风险增加
《2019中国脑出血诊治指南》:
-
高血压是脑出血复发的重要危险因素;
-
研究发现,服用阿司匹林人群中,每10,000人中脑出血增加12例;
-
老年人尤其是未经治疗的高血压患者中阿司匹林引起脑出血的风险进一步增加。
(2)高血压控制不佳患者使用阿司匹林出血风险进一步升高
高血压最佳治疗国际性(HOT)研究纳入18,790名高血压患者,分为安慰剂组和阿司匹林组(75mg qd)。
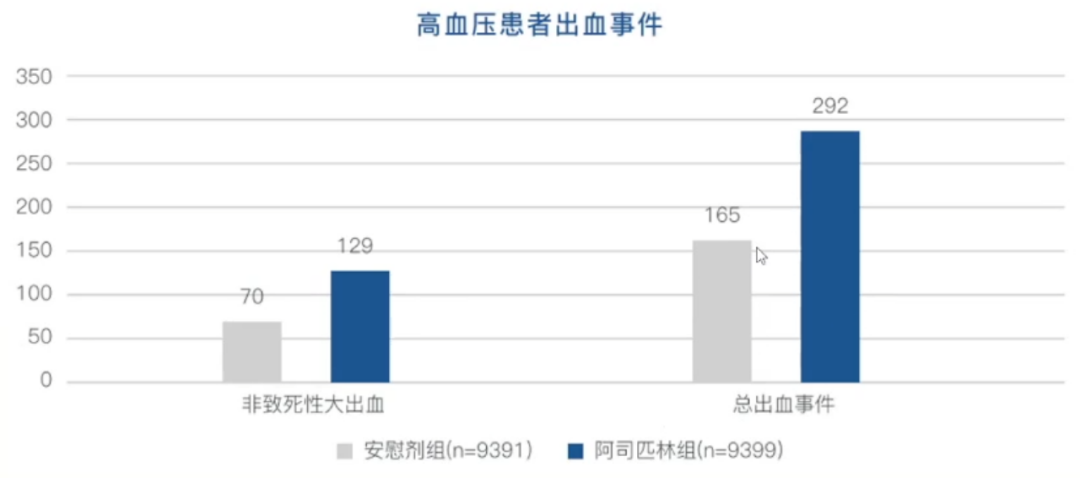
结果显示,①阿司匹林降低主要CVD事件15%(P=0.03),心肌梗死减少36%(P=0.002);②阿司匹林组和安慰剂组分别有129例与70例非致命性重大出血(p<0.001),服用阿司匹林的受试者非致死性大出血事件增加了84.3%,总出血事件增加了77.0%,主要与血压控制不良的基础上应用阿司匹林有关。
临床应用阿司匹林时,一定要注意患者血压的安全值,高值限定在160/100mmHg,急症高值限定在180/100mmHg,能够在一定程度上保证进行抗凝时不造成重要器官出血。
3.导致不耐受风险增高的危险因素三:肾功能不全
(1)肾功能不全患者缺血和出血风险均显著增加
纳入8,953名ACS患者,按慢性肾脏病分期:肾功能正常轻度(肌酐清除率>60ml/min);中等(肌酐清除率30-60ml/min);严重(肌酐清除率<30ml/min)。评估30个月内缺血性事件和出血性事件发生率。
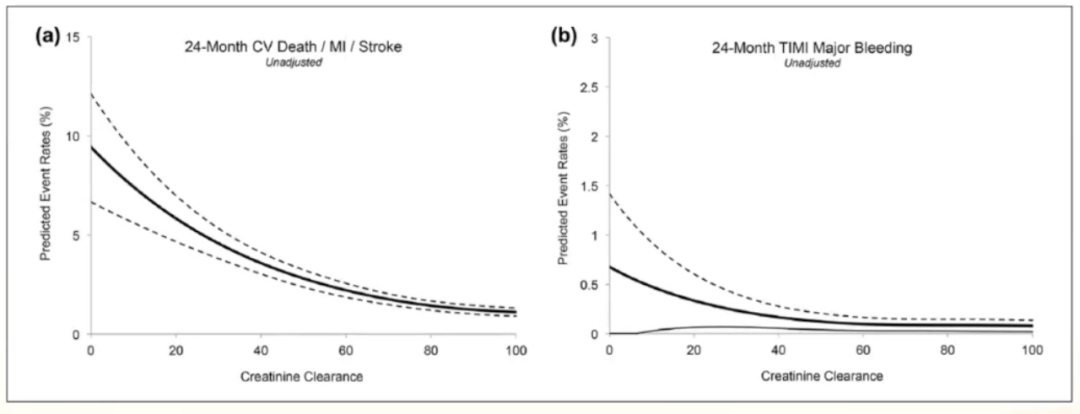
结果显示,在慢性肾脏病各个阶段,缺血和出血的发生率显著增加;在中度CrCl值(30-60ml/min)范围内,患者CrCl每降低5ml/min,其缺血和出血的风险将会增加20%-40%。
(2)经常使用阿司匹林使慢性肾衰风险显著增加
NEJM:瑞典一项基于人群的早期慢性肾功能衰竭病例对照研究共纳入926名肾衰竭患者和998名对照患者,两类患者中阿司匹林定期使用的比例分别为37%和19%。
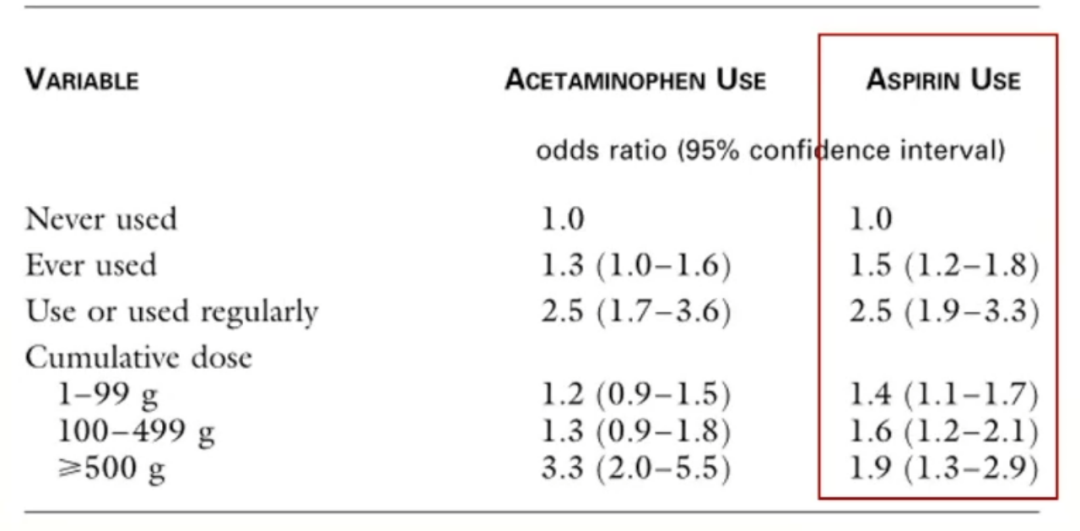
结果显示,在没有其他药物的情况下,经常使用阿司匹林所引起的慢性肾功能衰竭的风险增加2.5倍,且相对风险随着累积寿命剂量的增加而增加。
(3)替格瑞洛肾性不良事件发生率较氯吡格雷高
PLATO亚组分析:对于重度肾功能不全患者,替格瑞洛肾性不良事件发生率显著高于氯吡格雷。
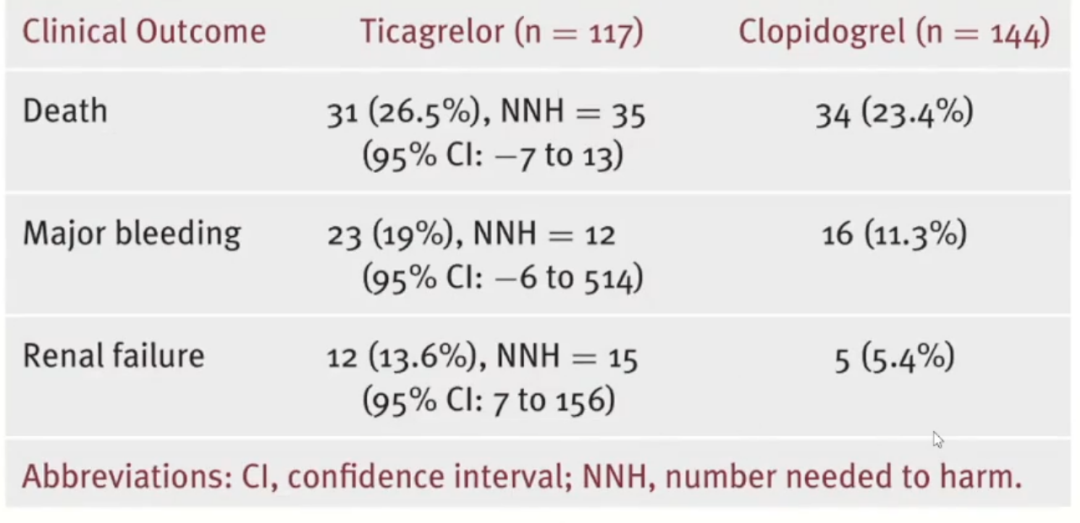
结果显示,与氯吡格雷组相比,在基线肾小球滤过率(eGFR)<30ml/min的住院患者中,替格瑞洛组的主要出血、死亡和肾功能衰竭风险增加。
二、抗血小板药物低反应性人群风险及机制
(一)阿司匹林低反应性
1.阿司匹林低反应性显著增加患者心血管事件发生风险
Meta研究:总共包括20项研究,涉及2930例心血管疾病患者,其中2120例患者确定为对阿司匹林敏感,810例患者为阿司匹林低反应性。
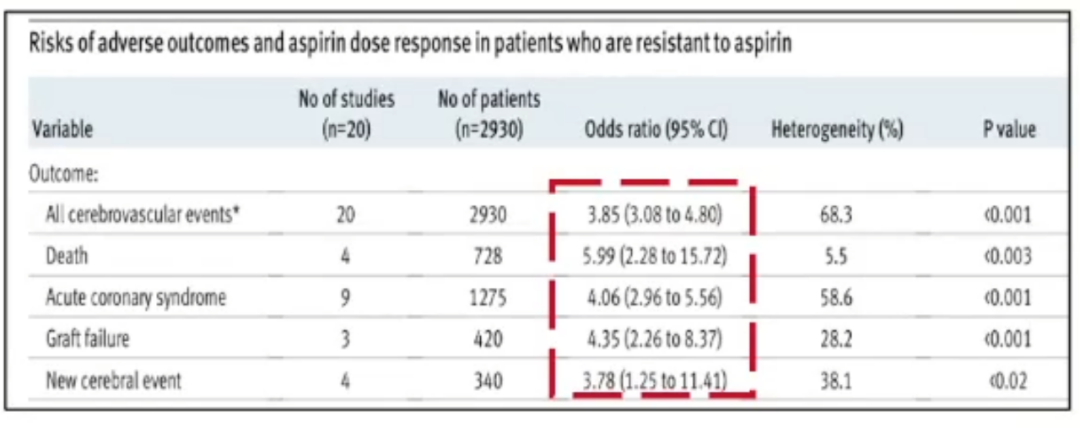
结果显示,阿司匹林低反应性患者心血管事件发生率明显高于阿司匹林敏感患者(39% vs 16%,OR 3.85,P<0.001)。与阿司匹林敏感者相比,阿司匹林低反应性患者非致命和致命性心血管、脑血管事件风险增加4-5倍(P<0.001)。
2.阿司匹林低反应性机制
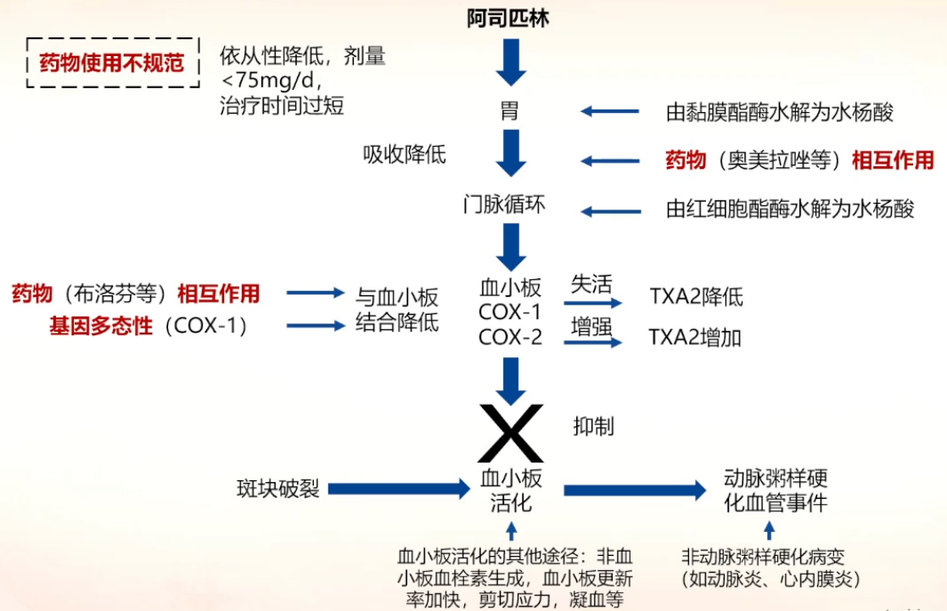
3.增加阿司匹林剂量并不能改善临床事件
CURRENT-OASIS 7研究:多中心、随机、双盲对照试验,对17,263名接受PCI的患者进行分析,8,624例患者服用高剂量阿司匹林(300-325mg),8,639例患者服用低剂量阿司匹林(75-100mg)。
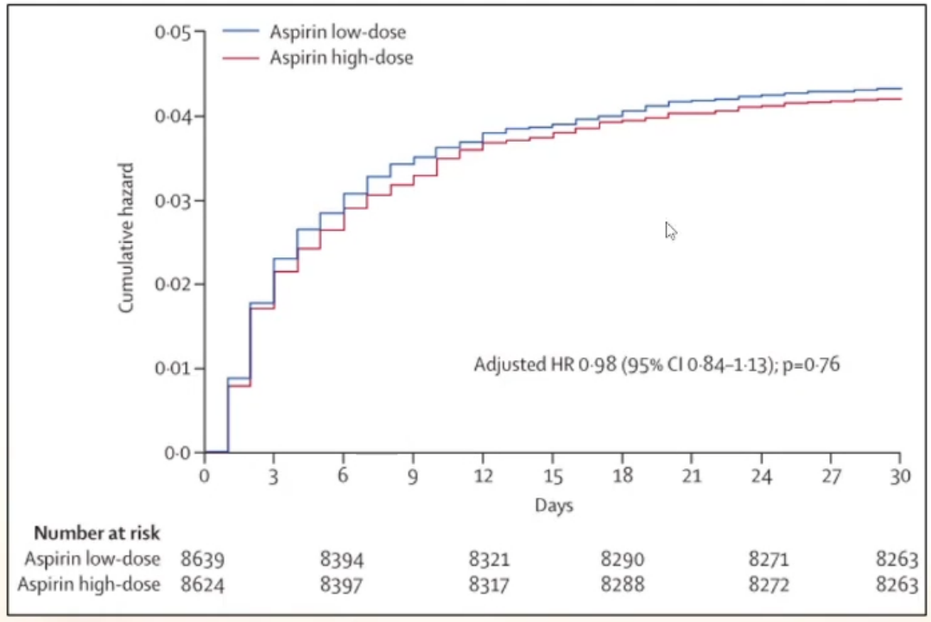
在高剂量和低剂量阿司匹林组中,心血管死亡、心肌梗死、中风或难治性缺血等主要复合结局方面没有差异,增加阿司匹林剂量并不能改善临床事件,反而增加出血风险。因此,在与P2Y12抑制剂合用时,即使血小板功能检测结果提示阿司匹林治疗反应不佳,也不推荐增加阿司匹林剂量。
(二)氯吡格雷低反应性
1.氯吡格雷的代谢:需通过肝脏P450酶系的活化
氯吡格雷代谢途径:
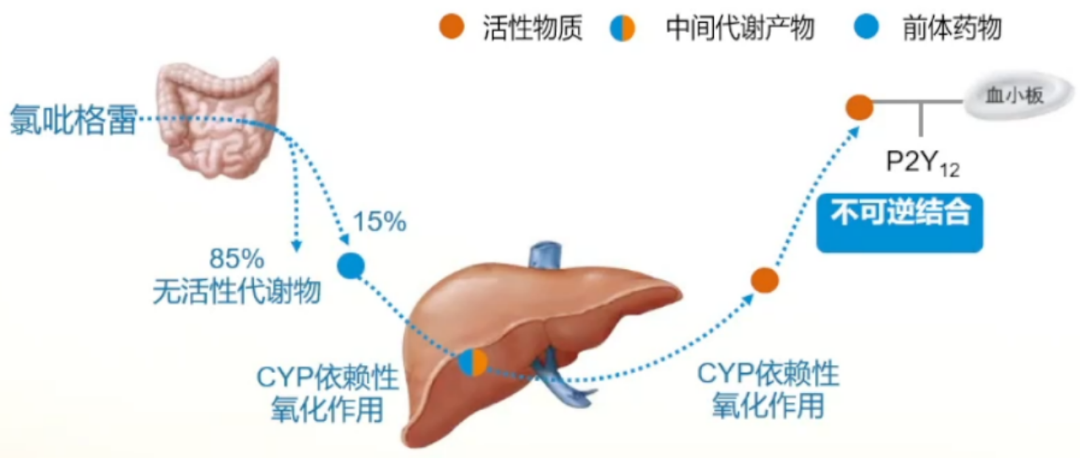
①85%经酯酶CES1水解成无活性产物,经肠道排出。
②15%经过肝CYP450酶(主要是CYP2C19和CYP3A4)两步代谢反应转化成活性产物:
-
CYP1A2、CYP2B6及CYP2C19酶参与调控第一步氧化反应,而CYP3A4、CYP2B6、CYP2C9 及CYP2C19酶催化第二步氧化反应。
-
CYP2C19在第一步氧化代谢中起到45%的作用,在第二步中起到21%的作用。
2.关于CYP2C19
(1)CYP2C19基因多态性与临床终点事件显著相关
TRITON-TIMI38研究:入选了1477例参加试验的行PCI手术的ACS患者,给予标准治疗,对影响氯吡格雷药效的多个基因进行了研究,随访15月。

与非携带者相比,CYP2C19功能缺失等位基因携带者主要复合终点事件(心血管性死亡、非致死性心肌梗死或非致死性卒中)发生风险增加了53%(12.1% vs 8.0%,图A),支架内血栓风险增加了3倍(2.6% vs 0.8%,图B)。
(2)CYP2C19失活等位基因携带者具有更高的缺血风险
Meta研究:总共包括9项研究,涉及9685例患者。
在接受氯吡格雷经皮冠状动脉介入治疗的患者中,与非携带者相比,携带1个和2个CYP2C19功能缺失等位基因患者出现支架血栓的风险增加2.67倍和3.97倍(P<0.001)。
(3)CYP2C19等位基因多态性(*2/*3/*17)基因分型
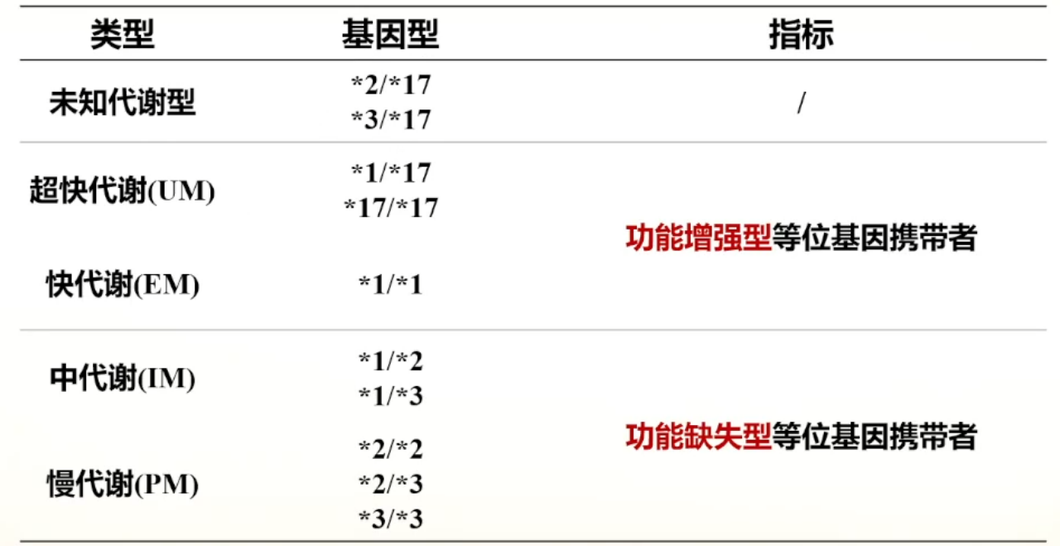
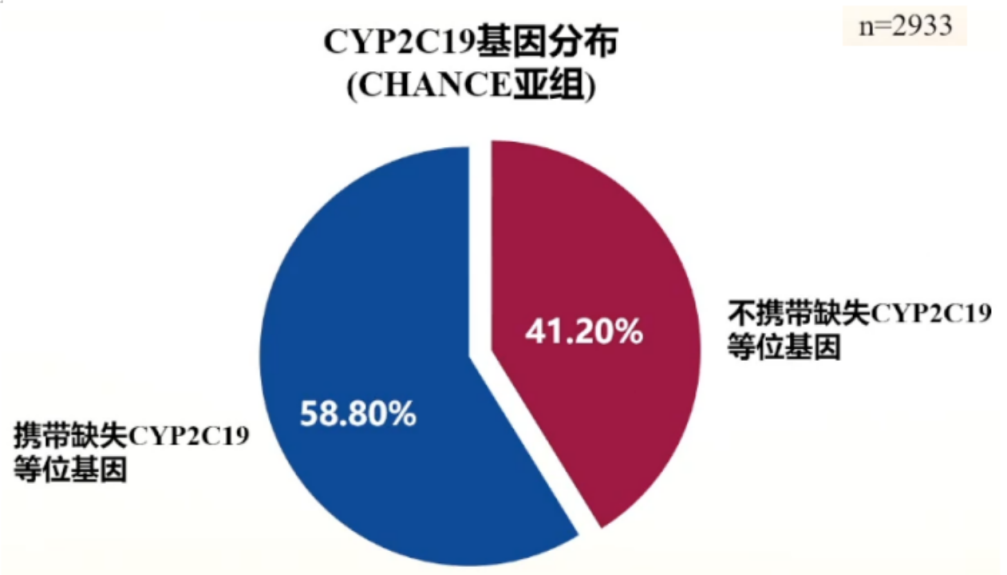
(4)CHANCE药物基因亚组研究:我国超过58%的人群携有CYP2C19变异基因(*2,*3)
3.氯吡格雷低反应性不推荐首选增加剂量
ELEVATE-TIMI56研究:多中心、随机、双盲试验,在32个地点登记并对333名心血管疾病患者进行基因分型。研究增加剂量(每天高达300mg)对CYP2C19功能缺失等位基因携带者血小板聚集抑制的改善作用,为CYP2C19基因多态性患者使用氯吡格雷提供参考。
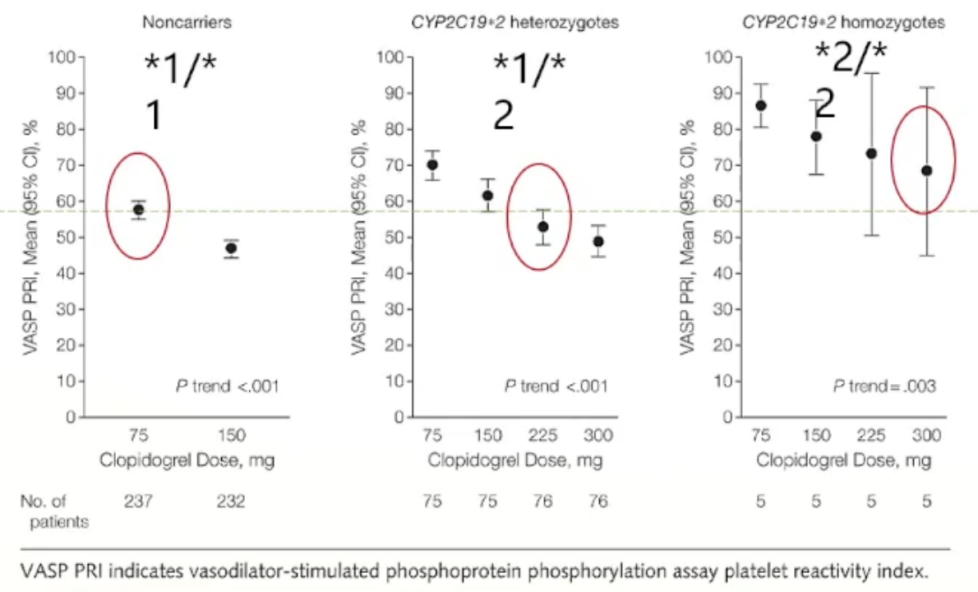
CYP2C19*1/*2型患者,维持剂量加倍(225mg),其对血小板活性的抑制程度方可达到非携带者患者的水平。而对于*2/*2型患者,即使维持剂量3倍(300mg),仍然难以达到相当的血小板抑制水平,需要更换药物。
(三)吲哚布芬
1.吲哚布芬:选择性、可逆抑制COX-1
目前尚无研究表明其存在低反应性的情况。
-
选择性:主要抑制血小板COX-1、血小板因子3和4,较低抑制前列环素的生成,因此胃肠反应更少。
-
可逆性:可逆抑制血小板聚集,24小时恢复血小板功能。
2.吲哚布芬通过AA途径抑制血小板聚集的作用不劣于阿司匹林
本研究共入选56例PCI术后稳定型冠心病患者,评估患者在使用标准的阿司匹林100mg qd联合氯吡格雷75mg qd双联抗血小板治疗达12个月后,分别使用单药吲哚布芬100mg bid、单药阿司匹林100mg qd治疗1个月后,花生四烯酸(AA)诱导的血小板聚集率的差异。
结果显示,吲哚布芬单药组聚集率低于阿司匹林单药组,有统计学差异(P=0.038)。与阿司匹林相比,吲哚布芬通过AA途径抑制血小板聚集的作用不劣于阿司匹林。
3.吲哚布芬胃肠反应少:对前列环素的影响少
(1)10名健康男性志愿者,随机分为两组:吲哚布芬200mg bid,阿司匹林300mg qd。连续给药7天。结果显示,吲哚布芬对前列环素PGI的抑制作用显著弱于阿司匹林。
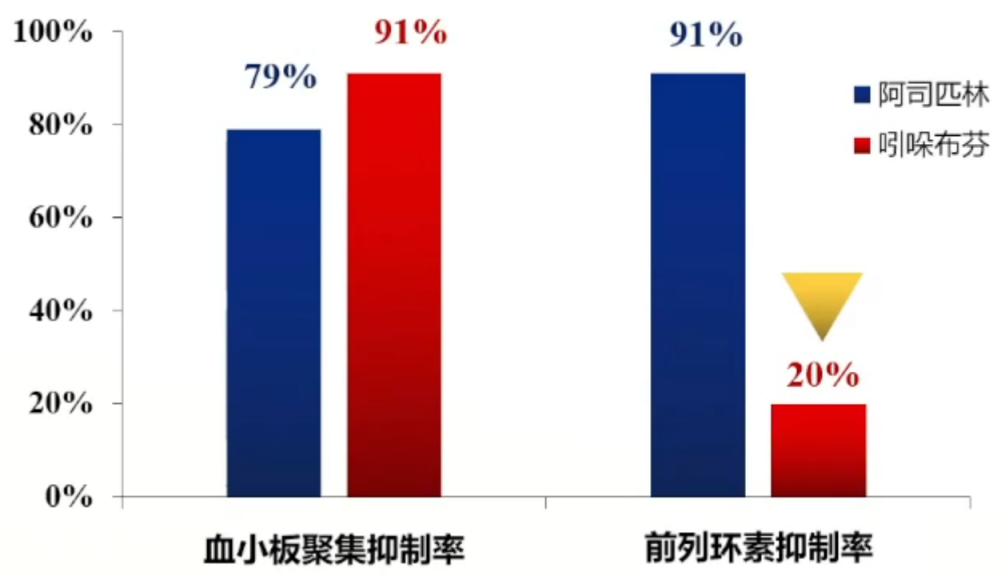
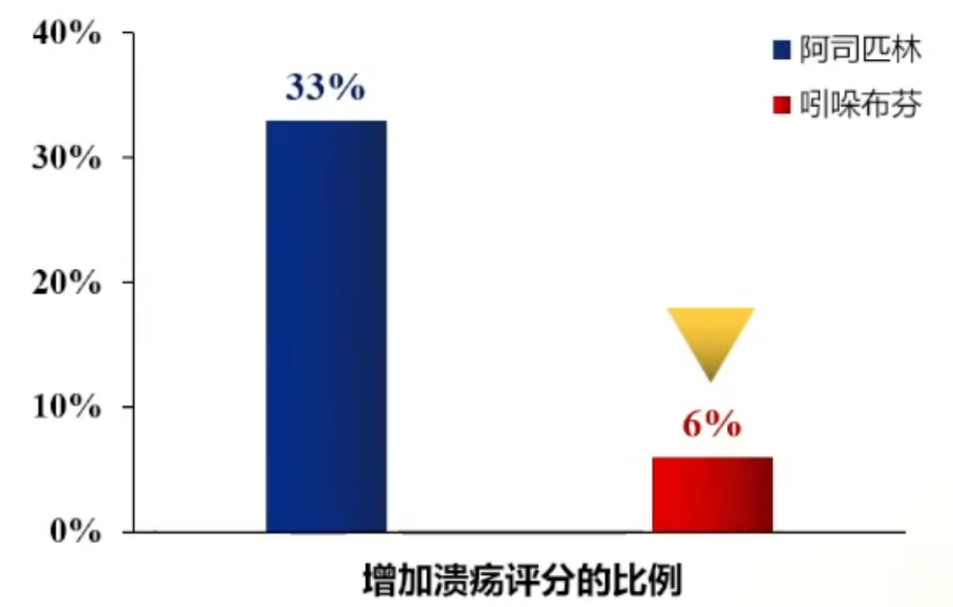
(2)共36例健康志愿者,18例口服阿司匹林vs 18例口服吲哚布芬;11天后用胃镜评估比较溃疡评分的变化。结果显示,吲哚布芬对胃溃疡的影响显著弱于阿司匹林。
三、高风险人群的临床筛查
(一)抗血小板不耐受高风险人群
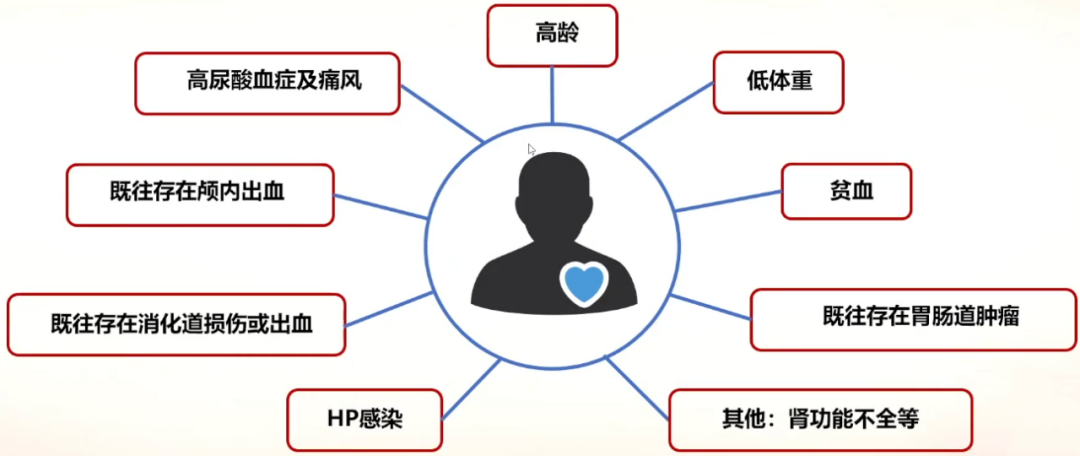
(二)低反应性人群临床筛查方法
1.血小板功能检测
患者主要包括复杂介入治疗;PCI术中出现夹层、无复流等;标准抗血小板治疗下再发血栓事件等。对需要更改抗血小板药物的患者,可检测血小板功能以指导P2Y12受体抑制剂的转换。
血小板功能检测——筛查血小板功能低反应性人群:

2.基因检测
对于高危缺血风险或者预后较差的动脉粥样硬化患者,可行氯吡格雷基因多态性检测,以作为P2Y12受体抑制剂的选择参考。
基因检测——筛查CYP2C19慢代谢及中间代谢人群:
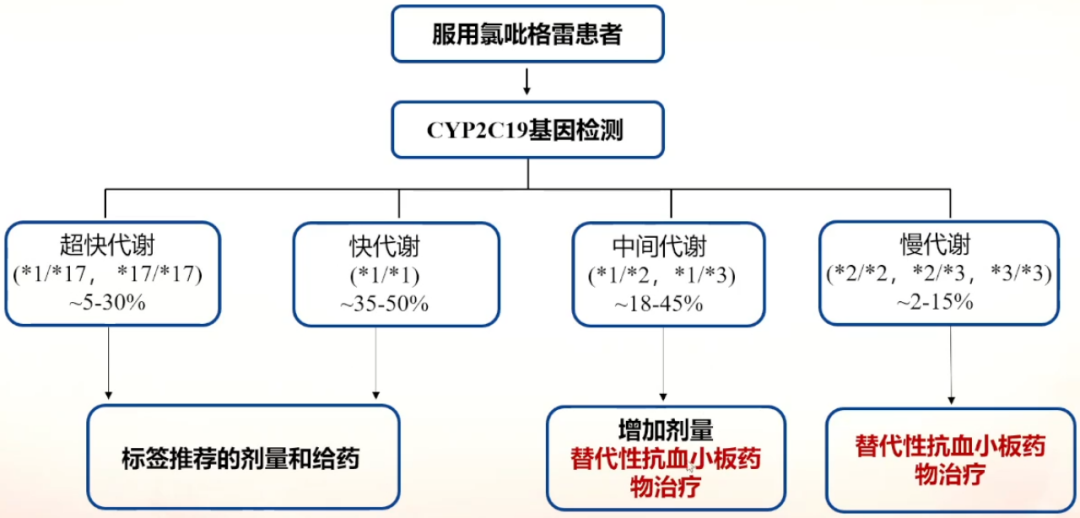
四、抗血小板药物不耐受及低反应性人群的治疗策略
(一)特殊人群抗血小板药物治疗临床建议
1.消化道溃疡及出血人群的抗血小板药物治疗临床建议
(1)冠心病
①阿司匹林产生消化道损伤症状:加抑酸用药或H2受体阻滞剂联合胃黏膜保护剂,也可改用其他抗血小板药。
②如患者发生活动性消化道出血,停用抗血小板药物直到出血情况稳定,症状稳定后可根据下述建议考虑改用合适的抗血小板方案:
-
SAPT:可选择长期服用阿司匹林、吲哚布芬、氯吡格雷、替格瑞洛、西洛他唑(心脏功能衰竭禁用、冠状动脉狭窄慎用,下同);如具有高危消化道出血风险的患者,可改用氯吡格雷/吲哚布芬等。
-
DAPT:既往有消化道出血史或具有高危消化道出血风险的患者(包括老年人,服用华法林、糖皮质激素或者NSAIDS者等),推荐服用PPI 1-3个月或H2受体阻滞剂联合胃黏膜保护剂,既往DAPT方案可改用氯吡格雷/吲哚布芬等治疗。
(2)DAPT期间发生消化道出血的患者
①积极治疗原发病。
②应权衡出血和缺血风险,再决定:
-
轻度出血无需停用DAPT。
-
如有明显出血(血红蛋白下降30g/L或需要住院治疗,但未引起血流动力学紊乱),可考虑首先停用阿司匹林,如出现危及生命的活动性出血,可停用所有抗血小板药物。
-
病情稳定后,在确保安全的情况下尽快恢复抗血小板治疗,一般3-5天后恢复氯吡格雷,5-7天后恢复阿司匹林或者更换为吲哚布芬等。
-
如服用替格瑞洛发生消化道出血的患者:停用替格瑞洛,如轻、中度出血可考虑换用氯吡格雷;重度出血需停用P2Y12受体抑制剂治疗者,在出血停止后换用氯吡格雷联用吲哚布芬等。
2.脑出血人群的抗血小板药物治疗临床建议
(1)抗血小板治疗时发生自发性脑出血患者:应立即停药;如有必要恢复抗栓治疗时,可于症状改善数天后,优先考虑抗血小板单药治疗,首选出血风险更低的抗血小板药物,如吲哚布芬、西洛他唑等。
(2)缺血性卒中伴有出血转化患者,可于症状性出血转化病情稳定后10天至数周后,酌情考虑开始抗栓治疗。
(3)75岁以上脑出血患者,建议影像评估出血吸收后重启抗栓治疗。
3.其他器官出血事件人群的抗血小板药物治疗临床建议
(1)轻微出血:建议持续抗血小板药物治疗,可换低强度抗血小板药。
(2)小出血:任何需要医疗照顾但无需住院的出血。建议持续抗血小板药物治疗,考虑缩短DAPT疗程/换低强度抗血小板药(降阶);识别与出血相关的并发症(如肾结石、痔疮、肿瘤)并进行可能的治疗。
(3)中度出血:任何导致血红蛋白丢失>30g/L和(或)需要住院治疗的出血,但血流动力学稳定,病情不会快速进展。尽量使用SAPT,优选P2Y12受体抑制剂,认为安全后可根据情况尽快恢复DAPT:选药原则同上。
(4)严重出血:任何导致血红蛋白丢失>50g/L并需要住院治疗的出血,但血液动力学稳定且病情不会快速进展。
-
停用DAPT,止血后再决定是否继续SAPT;
-
对于持续出血或无法治疗时,考虑停用所有抗栓药物;
-
一旦出血停止,再次评估需要DAPT还是SAPT治疗,考虑降阶;
-
再次启动DAPT后,考虑缩短DAPT疗程或降阶。
血红蛋白<70-80g/L时,考虑输注红细胞或血小板,如果可能,紧急手术或内镜治疗出血源。
(5)危及生命的出血:任何威胁患者生命的严重活动性出血。
-
停用所有抗栓药物;
-
一旦出血停止,再次评估需要DAPT还是SAPT,降阶。
低血压时给予补液,酌情及时考虑红细胞输注,酌情进行血小板输注;如果可能,紧急手术或内镜治疗出血源。
4.痛风/高尿酸人群的抗血小板药物治疗临床建议
(1)ACS合并痛风治疗,如果是阿司匹林导致痛风,立即停用,换用吲哚布芬+氯吡格雷等方案。
(2)支架后服用DAPT过程中发生痛风,应权衡缺血和痛风危害,可考虑合用抗痛风药物,或将阿司匹林换为吲哚布芬/西洛他唑。
(3)对于无需双联抗血小板治疗的稳定性冠心病、缺血性卒中或PAD患者,若合并高尿酸血症或痛风:
-
优先选择对嘌呤代谢影响小的抗血小板药物如氯吡格雷、吲哚布芬或西洛他唑;
-
若仍然使用阿司匹林,则建议碱化尿液、多饮水,同时监测血尿酸水平;
-
对于既往高尿酸血症或痛风性关节炎的患者应慎用替格瑞洛,不建议尿酸性肾病患者使用替格瑞洛。
5.高龄人群的抗血小板药物治疗临床建议
75岁以上冠心病患者:
(1)可首选阿司匹林、吲哚布芬、氯吡格雷、替格瑞洛等抗血小板药物作为二级预防用药;
(2)若出血风险较高,可以优先使用出血风险较低的吲哚布芬、氯吡格雷等;
(3)为预防支架内血栓,对于PCI术中成功置入DES的高龄患者,DAPT治疗期间可给予PPI防范消化道出血,或使用吲哚布芬联合氯吡格雷。
6.高血压人群的抗血小板药物治疗临床建议
(1)对于非急性期卒中或TIA高血压患者,降压达到目标值后再酌情使用抗血小板药物;对于皮层下小卒中患者长期使用抗血小板药物,可以考虑血压降到130/80mmHg以下。
(2)对于目前血压达标且合并冠心病、缺血性卒中或PAD患者,抗血小板药物的选择应根据病情决定,可选出血风险低的抗血小板药物,如吲哚布芬或西洛他唑。
7.肾功能不全人群的抗血小板药物治疗临床建议
(1)轻中度肾功能不全【eGFR:30-90ml/(min·1.73㎡)】
-
推荐阿司匹林、吲哚布芬或西洛他唑;服用阿司匹林期间需密切监测肾功能变化。
(2)重度肾功能不全【eGFR<30ml/(min·1.73㎡)】及透析患者
-
尽量避免使用阿司匹林及替格瑞洛:SAPT方案建议使用吲哚布芬或西洛他唑;对于ACS患者,可考虑吲哚布芬联合氯吡格雷。
(二)抗血小板药物低反应性人群的治疗临床建议
对于高危缺血风险或预后较差,高出血风险或已经发生出血的冠心病患者,以及缺血性卒中或PAD患者,可考虑行基因检测和血小板功能检测,作为抗血小板药物使用的参考。对需要更改抗血小板药物的患者,可检测血小板功能以指导P2Y12受体抑制剂的转换。对于高缺血风险同时又进行了复杂PCI手术的患者,在服用氯吡格雷前应进行相应基因检测。
1.阿司匹林低反应性人群专家建议
可考虑换用其他抗血小板药物,如吲哚布芬或氯吡格雷;当阿司匹林与P2Y12抑制剂合用时,即使血小板功能检测结果提示阿司匹林治疗反应不佳,也不推荐增加阿司匹林剂量(超过100mg/d)。
2.氯吡格雷低反应性人群专家建议
对于常规剂量氯吡格雷治疗无反应或低反应者,尤其是合并糖尿病的患者,不推荐首选增加氯吡格雷剂量,建议换用其他抗血小板药物,比如替格瑞洛等;如存在出血高危因素,或因其他原因不能接受P2Y12受体抑制剂治疗,可换用阿司匹林、吲哚布芬或西洛他唑(非心力衰竭或冠状动脉狭窄患者)。