俞飞成教授:单纯主动脉瓣反流的TAVR:操作技巧及挑战病例分享

近年来,随着技术经验的积累,TAVR在主动脉瓣反流(AR)患者中的应用逐渐被证实为一种安全、可行的外科手术替代方案。但AR特有的解剖特点使得TAVR治疗存在一定挑战。在2024中国结构周会议期间,浙江大学医学院附属邵逸夫医院俞飞成教授进行“单纯主动脉瓣反流的TAVR操作技巧及挑战病例”主题讲课,通过临床经验与病例分享,为AR患者TAVR治疗提供了重要参考。医谱学术特此整理,以供临床参考。
流行病学
AR患者的数量约为主动脉瓣狭窄(AS)患者的两倍,但在治疗方面仍面临诸多限制。根据国外心脏瓣膜病的相关调查显示,在重度AR患者中,仅约20%左心室射血分数(LVEF)介于30%-50%之间的患者接受了外科主动脉瓣置换术(SAVR),而当LVEF低于30%时,接受手术的比例不足3%。高龄和多种合并症是限制患者接受开胸手术的重要原因,这迫使部分患者选择保守治疗,病死率每年高达10%-20%。
为了应对AR患者未被满足的临床需求,进一步提升治疗的安全性、规范性,并为临床实践提供指导支持,2023年发布的《单纯主动脉瓣反流经股动脉主动脉瓣置换专家共识》总结了九大核心观点。这些观点从流行病学特点、适应证和器械选择,到术前CT评估及术中操作要点,为TAVR治疗AR提供了重要的理论支持和实践参考。
针对AR行TAVR时瓣膜锚定困难、容易移位等挑战,俞飞成教授从解剖结构和释放技巧两方面一一详细讲解。
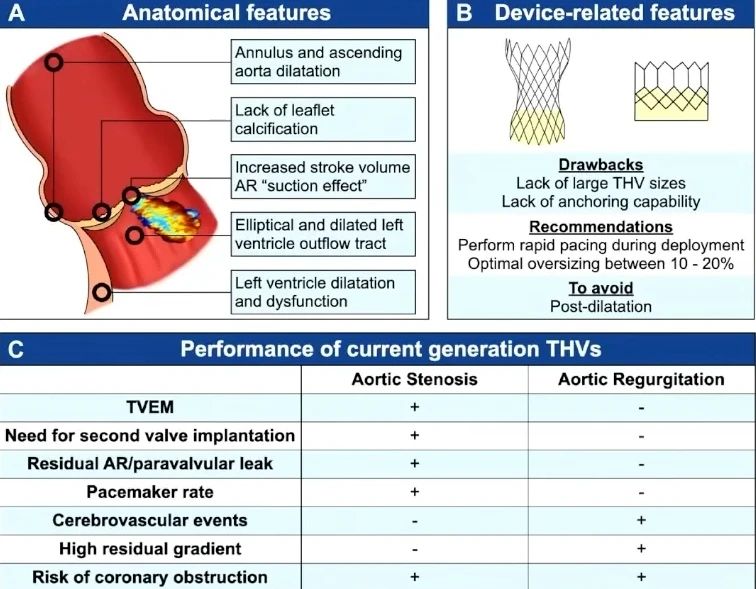
解剖因素
术前CTA多平面评估以及判断有利的锚定结构是提高TAVR治疗AR手术成功率的前提。
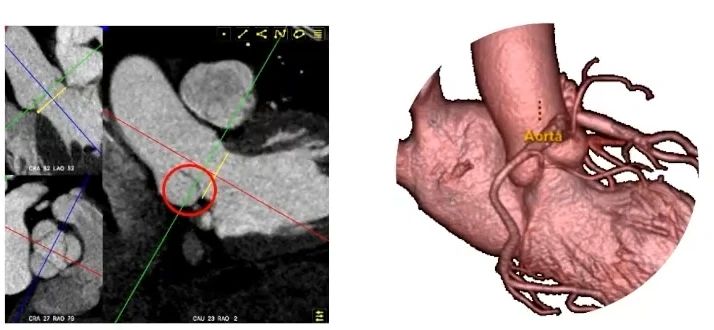
术前CTA多平面评估
术前CTA多平面评估解剖形态,为冠脉阻塞风险的评估提供了切实可行的方案,可指导瓣膜尺寸选择、高危复杂结构筛选、植入深度、释放策略,并对手术难易程度作出判断。
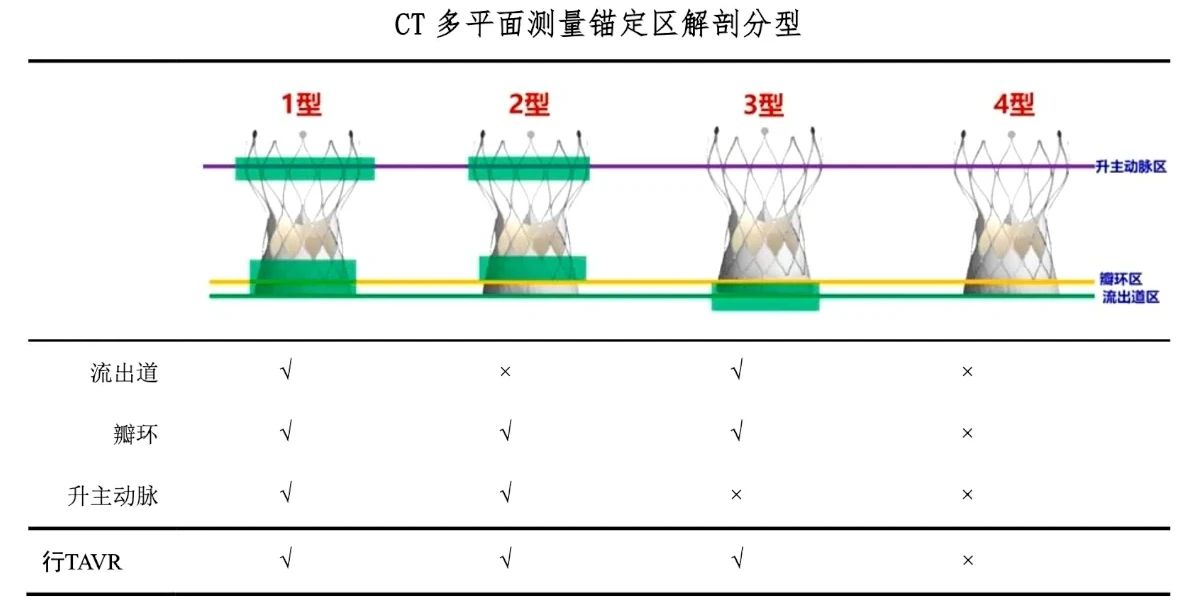
锚定因素
有利于锚定的解剖特征包括以下条件:
1、主动脉根部(AA)直径小于26mm;
2、左心室流出道(LVOT)呈收口型或至少为直筒型;
3、LVOT存在肌性台阶;
4、主动脉瓣二叶瓣畸形;
5、主动脉瓣钙化或瓣叶增厚;
6、窦管交界(STJ)直径小于35mm;
7、STJ与升主动脉(AAO)直径差大于5mm。
不利于锚定的解剖特征包括以下条件:
1、AA直径大于28mm;
2、LVOT呈敞口型;
3、瓣叶脱垂;
4、窦部(SOV)扩张;
5、STJ扩张;
6、AAO扩张;
7、主动脉瓣环呈横位(瓣环角度小于60度)。
解剖考虑
同时,解剖适应性也是关键考量因素,根据以下解剖学条件可评估患者是否合适行TAVR手术。

释放技巧
释放技巧可总结为无冠窦支点法(NCPI)、验证PASS原则和植入PHASE原则。
NCPI的定义
NCPI定义为:在瓣膜释放至可回收极限位且输送系统已无张力时,在DSA无冠窦切线位投照角度下,NCC侧植入深度-2mm≤DNCC≤2mm且无冠窦侧瓣架下缘呈微内收形态。
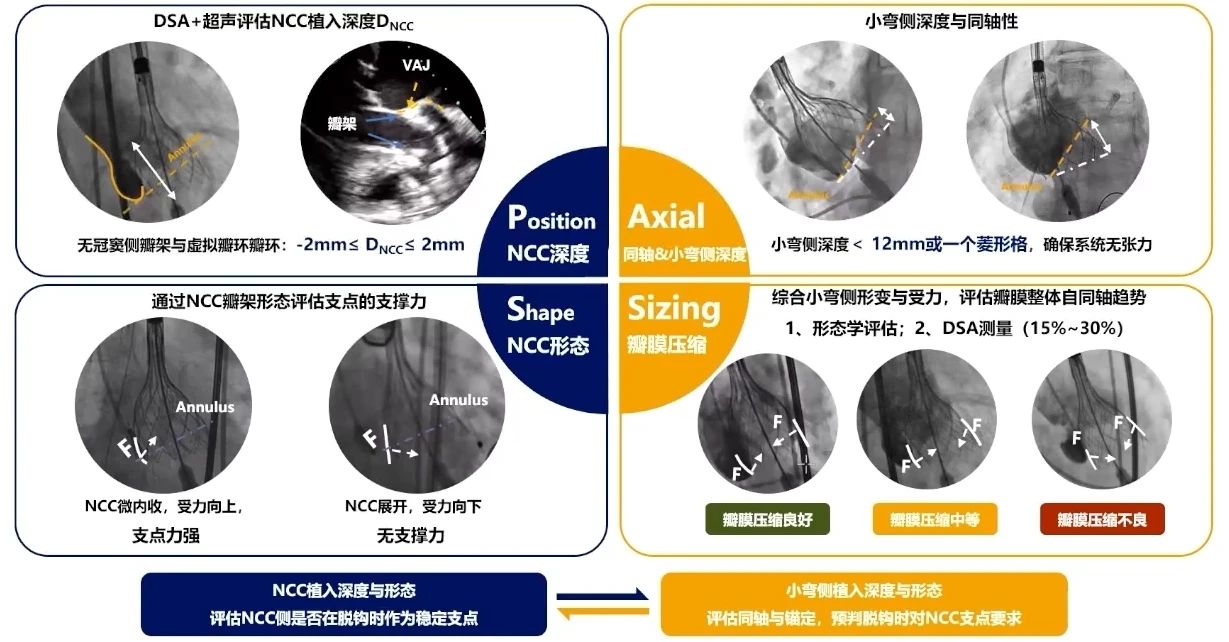
验证PASS原则
Position:术中需先将假体瓣膜瓣架对齐,DSA+超声评估NCC深度DNCC,无冠窦侧瓣架与虚拟瓣环之间-2mm≤DNCC≤2mm。
Axis:在评估小弯侧瓣架与虚拟瓣环的深度时,推荐不超过瓣膜的1个菱形格;若小弯侧超过1个菱形格,向下的受力会增大,从而增加移位的风险,需要回收并重新调整同轴。
Shape:通过NCC瓣架形态评估支点的支撑力。无冠窦内收,有向上力时,支撑力强;NCC展开,受力向下,无支撑力。
Sizing:通过压缩形变判断受力大小与受力点位置,综合无冠窦支点,可预估假体瓣膜工作位整体受力方向,预判脱钩自同轴趋势。在术中进行形态学评估时,根据小弯侧的压缩情况,评估整体受力;在DSA影像下测量,推荐压缩比为15%~30%。
植入PHASE原则
植入过程中遵循PHASE原则,以确保手术的安全性与成功率。
P(Pivot)指采用无冠窦支点法,以室间隔或无冠窦作为支点进行瓣膜释放;
H(High speed)强调快速稳定释放,在瓣膜即将锚定及锚定后快速释放到可回收极限位置,避免释放过程中发生移位;
A(Anatomy)要求术前通过CT全面评估解剖结构,包括瓣环、LVOT、窦管结合部、瓦氏窦、升主动脉及瓣环角度的分析,尤其关注瓣环大小及室间隔突出点;
S(Slow)在脱钩及系统撤出时需缓慢进行,特别是高位植入时避免上移;
E(Echo)则强调术中经食管超声(TEE)的细致评估,术前确认有无室间隔突出点,术后验证植入深度,确保瓣架完全位于窦内侧,无压迫室间隔突出点的情况。
基于不同自膨式瓣膜设计特点考量
VitaFlow LibertyTM自膨式瓣膜基于其独特的设计特点,提供了良好的使用体验和临床效果,在释放过程中的精准性方面表现突出。其设计确保了在整个释放过程中(包括前1/3和脱钩阶段)支架无位移或窜动,从而提高了手术的稳定性和安全性。
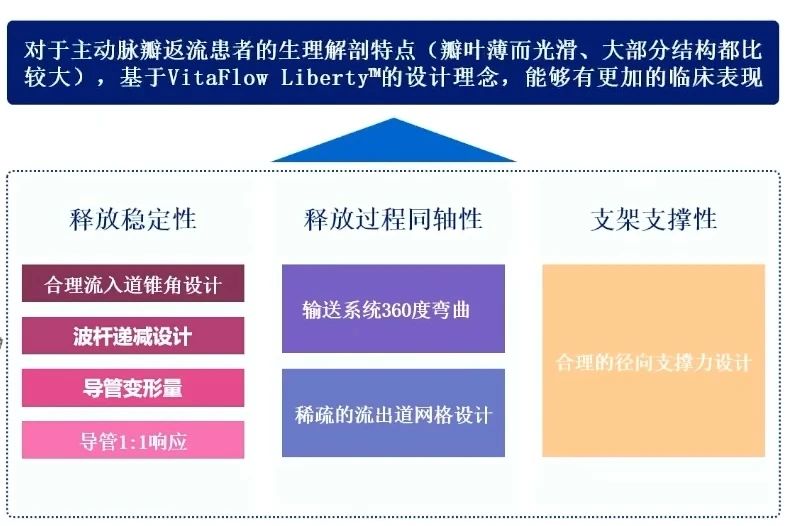
启明瓣膜流出端设有3个T头(2长1短),实现轴向锚定,可提供平稳的力学支持,确保瓣膜的稳定释放。此外,瓣膜流入端的3个射线下标记点在DSA下清晰可见,能帮助医生精准定位并实现精准释放,进一步提升了手术的成功率和疗效。

病例分享
患者男性,79岁,身高162cm,体重55kg,BMI为21kg/m2。因胸闷、气促持续半月前来就诊。既往有高血压病史10余年。辅助检查显示:血红蛋白128 g/L,肌酐95 μmol/L,估算肾小球滤过率(eGFR)65.3 mL/min,NT-proBNP水平显著升高(7669 pg/mL)。心电图提示窦性心律伴频发房性早搏。头颅MRI显示双侧基底节区陈旧性脑梗死。
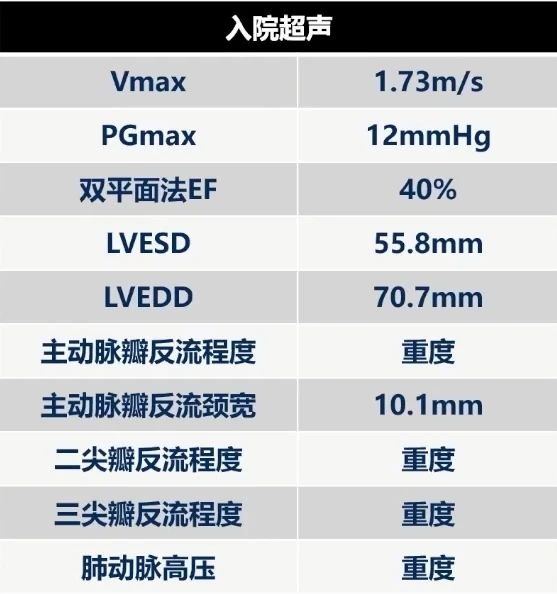
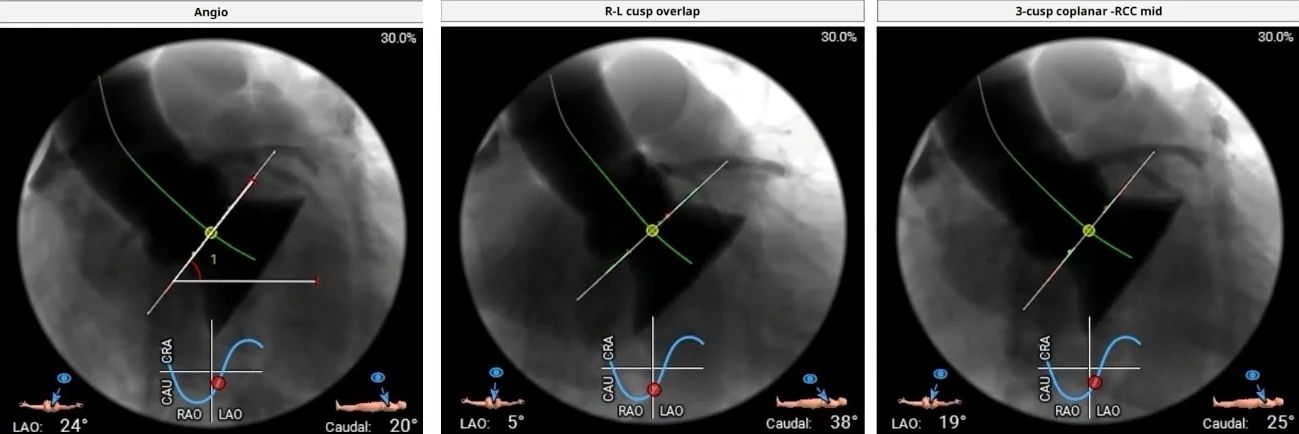
患者非横位心,瓣环略有增厚,相对来说可以提供一定的锚定力,外周入路粗,选择22F大鞘,术中从无冠窦切线位造影,发现主动脉瓣反流量较大,无明显压差,瓣膜缓慢释放后效果理想。术后超声显示瓣架形态良好、稳定。

释放策略个人经验
瓣膜起始定位应选择高位,释放体位则为无冠窦的最低点。初步释放时应缓慢进行,根据瓣膜移动情况调整位置。当瓣膜释放时,可采用180bpm的临时起搏,配合停呼吸,逐步将瓣膜释放至功能位。功能位评估时,将起搏频率调整至120bpm左右,确保瓣膜位置稳定(人工瓣膜低端内收),轻轻推压,观察瓣膜移动情况,并通过DSA多角度成像和心脏超声进一步评估。
在最后的释放脱钩过程中,重新使用180bpm起搏器,轻推并缓慢释放,需根据具体瓣膜类型来判断撤导丝回时的操作。回撤导丝时,应释放张力,注意避免tip头带出瓣膜。若需要依赖STJ和AAO作为锚定点,可在稳定后快速起搏并一次性释放到底。
瓣膜完全释放后,将临时起搏器频率调整至100bpm,并观察20至30分钟以评估瓣膜稳定性。如果循环稳定且回收超过三次,可更换瓣膜。
总结
AR患者在制定TAVR手术策略时,应对锚定结构进行详细评估,合理选择瓣膜类型,掌握释放策略的技巧,妥善处理可能出现的并发症,并通过不断更新的医疗器械,确保手术的成功和患者的良好预后。相信未来,随着技术的进一步发展和治疗方案的不断完善,TAVR有望为AR患者提供更加精准、安全的治疗,提高患者的生活质量。

长按识别二维码 看本次授课精彩回放
专家简介
医谱app
扫码或者点击图片下载
微信公众号
扫码或点击图片关注
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、上载、下载、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。





发表留言
暂无留言
输入您的留言参与专家互动