2022 CCHC丨陶凌教授:TAVR术后瓣周瘘
TAVR(经导管主动脉瓣置换术)术后瓣周瘘(PVL)作为临床常见并发症之一,严重影响着患者的长期预后。对于术后瓣周瘘的问题,临床有多种方法来处理。近日,空军军医大学西京医院陶凌教授在2022中国心血管健康大会上对“TAVR术后PVL”的处理作详细汇报,她提到首先需要选择合适的评估方法,AR index是其中一种方法,现在主动脉根部造影采用软件的方法既可以达到标准化造影的流程,同时又可以借助软件法计算出反流百分比,并且提供一个介质便于我们识别中-重度反流,从而及时进行处理。

SAVR(外科主动脉瓣置换术)PVL的机制:SAVR首先切除严重钙化的瓣膜,然后将人工瓣膜直接缝合到主动脉瓣环上。由于在去除自身瓣膜后产生的空间不是规则的圆形,因此在人工瓣膜缝合环和患者瓣环之间可能会存在不完全密封。
TAVR(经导管主动脉置换术)PVL的机制:
1.没有切除自身瓣膜、且并非缝合固定。因此,钙化组织会影响介入瓣的局部膨胀,导致瓣膜与瓣环结构不能完全贴合。
2.瓣膜位置不佳,植入过深、过浅导致裙边封闭作用丧失。
术中评估包括:侵入性血流动力学监测、不典型的瓣膜形态(椭圆形瓣环、二叶瓣)、主动脉造影、心脏超声(TTE TEE)。
术后评估包括:查体、心脏超声、CT。
急性主动脉瓣反流血流动力学:
1.心动过速。
2.左心室舒张末期压力升高。
3.舒张压降低(舒张末期主动脉和左心室压力相等)。

严重返流对血流动力学影响:
A.TAVR术后正常压力曲线:舒张末期主动脉与心室压差;
B.TAVR术后存在重度返流患者的舒张末期主动脉与心室压差很小(13 mmHg) AR index 6.1%;
C.快速起搏对重度PVL患者血流动力学的影响:主动脉收缩压变化不大,但是主动脉舒张压增加。

在PVR判断中,AR index与ECHO(超声心动图)良好联合。

心脏超声:用于评估主动脉瓣反流严重程度的超声心动图参数主要包括射流长度和面积。超声评估可以从以下几个方面进行:半定量参数(降主动脉脉冲舒张期血流逆转、人工瓣膜周长反流占比),定量参数(反流量、反流分数、有效反流口面积)。

主动脉根部造影:
-
轻度反流(1+)仅少量造影剂进入左心室而未充满;
-
中度反流(2+)造影剂微弱地充满整个心室且不能迅速清除;
-
中度至严重(3+)心室造影剂的密度等于升主动脉;
-
严重(4+)当心室造影剂密度大于主动脉。
整体来说,主动脉根部造影是主观的和半定量的;几乎不可能仅通过主动脉造影评估来将瓣膜内反流与PVL区分;为了通过主动脉造影术正确评估PVL的严重性,需要遵循以下几条规则:
1.至少5F猪尾导管,位置不超过人工瓣叶2cm,造影前撤出导丝。
2.造影剂不应低于8ml,12到20ml之间最佳,主动脉非选择性造影参数为20ml/s,压力1200 psi。
3.图像投影应很好地可视化主动脉近端以及整个左心室,左室流出道或主动脉根部不应有器械与之重叠。
4.图像记录应当持续直到造影剂从主动脉根部排出(造影剂注射后至少3个心搏)。
5.主动脉非选择性造影参数为20ml/s,压力1200 psi。
定量评估主动脉根部造影反流:采用单主动脉造影和视频密度测量技术,从参考区域(主动脉根部)和ROI区域得到两条时间-密度曲线,时间-密度曲线下两个面积的比值转换为反流的百分比。
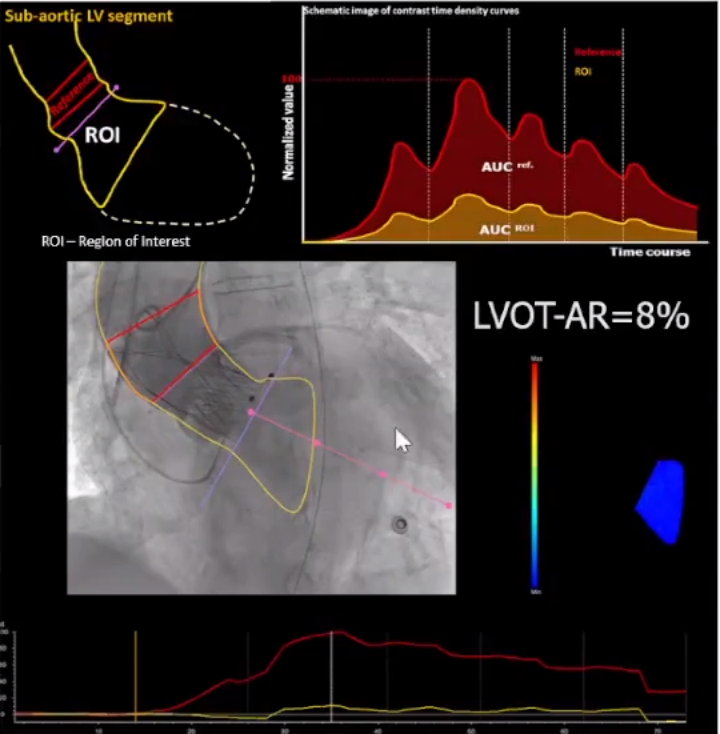
视频密度测量评估以量化TAVI后的AR严重程度。
qRA指数的理论范围【0.0-4.0】
-
0.0 无反流
-
1.0轻度反流
-
2.0中度反流
-
3.0中重度反流
-
4.0严重反流
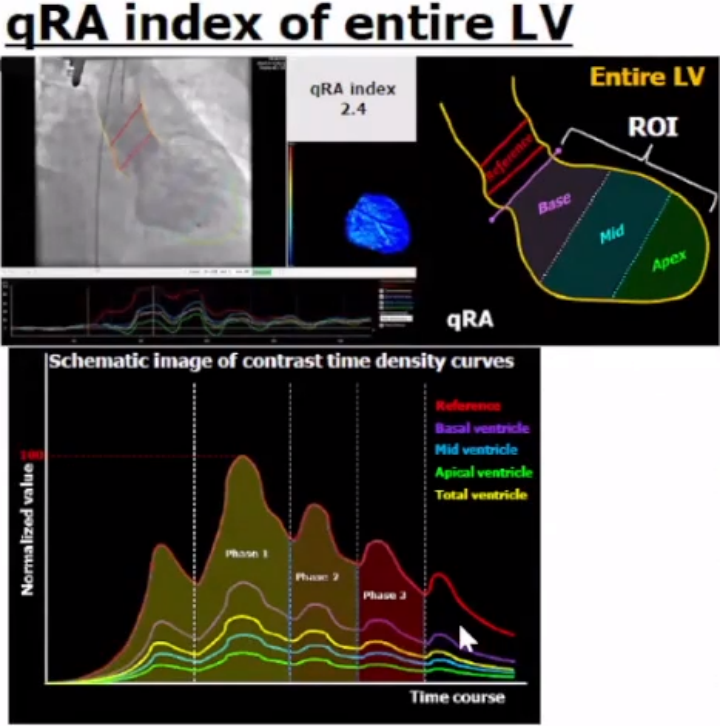
RAUC的理论范围【0.0-1.0】
-
0.0 LV中没有对比
-
1.0 LV中的对比度与参考区域相同

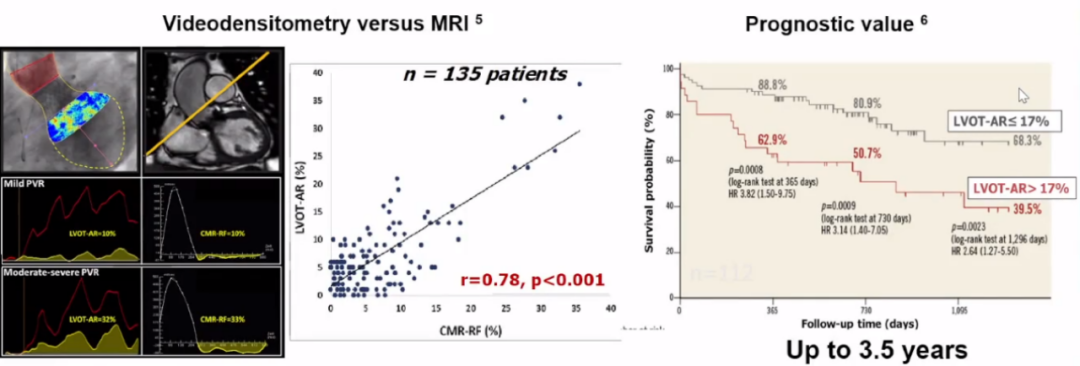
以下研究以MRI作为金标准,与主动脉根部造影相对应,结果发现两者对应度较高。另外,通过长期随访观察,借用主动脉根部造影的软件计算反流量和事件的关系,结果发现软件计算LVOT-AR>17%时,患者预后明显变差;LVOT-AR≤17%时基本上跟造影显示少量反流或没有反流的患者一致。由此,也可以判断,若术后LVOT-AR>17%时,一定需要干预后在结束手术;若≤6%,则完全不需要干预;若6%≤LVOT-AR≤17%时,属于灰色地带,由术者判断是否需要干预。
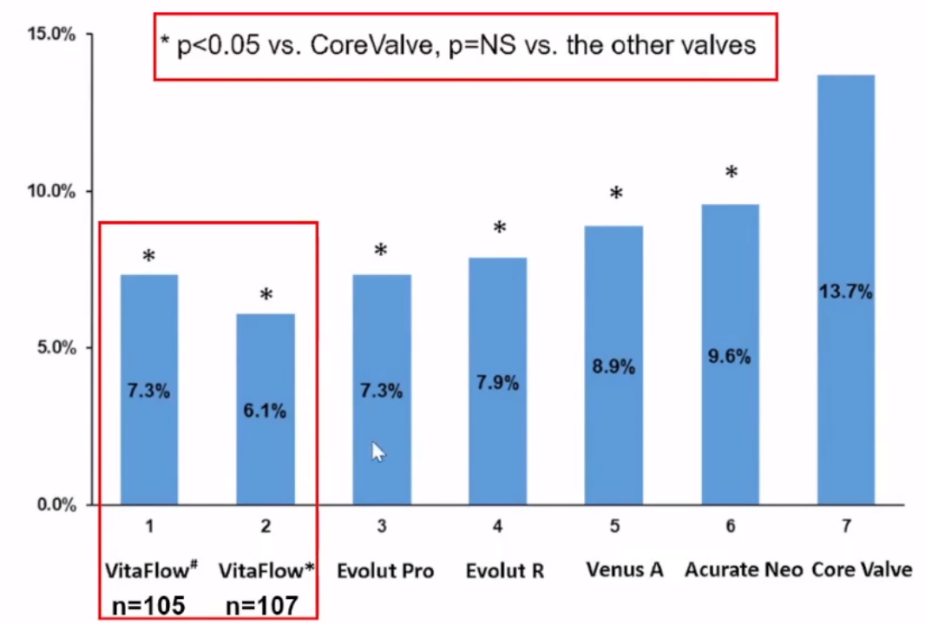
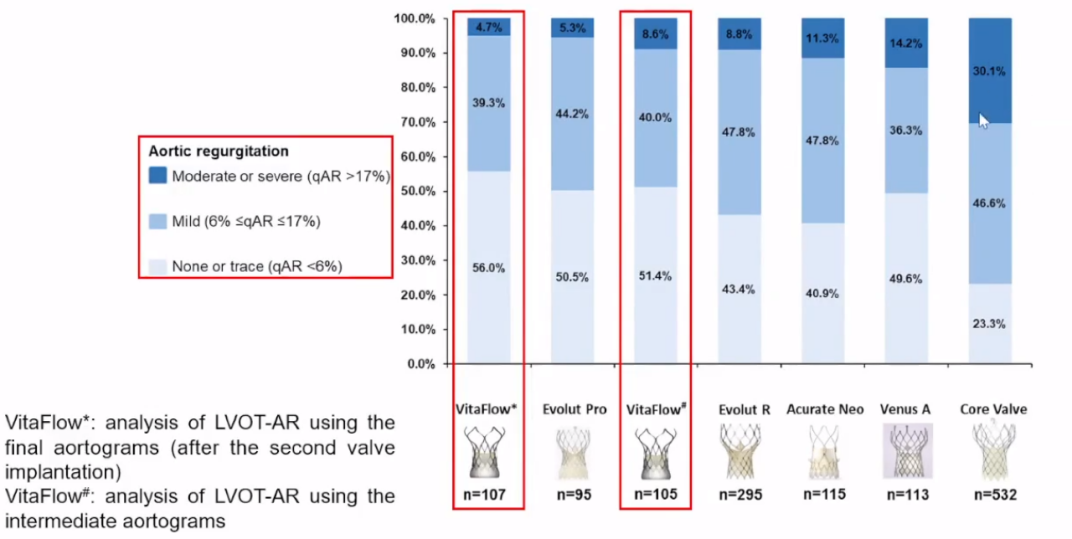
通过分析国外很多核心实验室的数据,对比国内外6个经导管心脏瓣膜(THVs)器械植入后,比较TAVR术后平均软件计算LVOT-AR结果,可以看出国产VitaFlow的LVOT-AR值是7.3%,在进行后扩或其他干预后降低到6.1%,相对其他几个器械表现相对不错。
通过视频密度法评估TAVR术后不同程度AR的累积百分比。统计患者在不同瓣膜结束手术时,出现中量或大量PVL的比例。在国内外的临床研究中,一部分患者在结束手术时,PVL的标准没有达到,这也影响着患者的临床预后。通过软件计算LVOT-AR结果可以帮助找出不达标的部分患者,从而采取进一步的干预措施。
PVL的严重程度与患者的预后密切相关。研究发现患者出现中/重度periAR和没有反流或轻度PVL两者之间生存率(36.4% vs 79.8%)相差较大,故术后要减少反流,干预意义重大。

1.PVL的危险因素
-
解剖因素:瓣叶的钙化程度(尤其是瓣叶与主动脉壁接合处);不典型的瓣膜形态(椭圆形瓣环、二叶瓣);极小的瓣膜面积;过大的主动脉成角。
-
手术因素:瓣膜型号不匹配(人工瓣膜小于自身瓣环);瓣膜移位(太低或抬高);不充分的预扩张。
2.PVL的预防及处置
预防手段:
-
仔细的评估主动脉根部解剖(瓣环大小、形态、钙化程度及分布);
-
充分的预扩张(尤其是瓣环面积小且钙化严重);
-
精准的瓣膜定位。
处置方法:
-
血流动力学稳定:保守治疗、严密随访;
-
血流动力学不稳定:血管升压药、快速起搏(120 beat/min);
-
瓣膜位置不佳:回收、抓捕器、V-IN-V;
-
人工瓣膜膨胀不充分:球囊后扩张;
-
顽固性瓣膜返流:外科手术、经皮治疗。

TAVR术后球囊后扩

TAVR术后瓣中瓣

1.评估PVL的方法很多,包括有创血流动力学监测(AR index)及影像学方法,往往需要综合多种结果判断。
2.中-大量PVL可能影响患者预后,精准的定量PVL可以辨别出需要处理的人群。
3.术前通过仔细的影像学评估,可以评估患者发生PVL的风险。
4.根据PVL产生机制可以采用后扩张、SANRE、瓣中瓣、介入等方法处理。

发表留言
暂无留言
输入您的留言参与专家互动