免开胸!经导管机械抽吸终末期肾病患者右心室导线巨型赘生物

引言
在临床工作中,对于伴有大型导线赘生物(长度超过 20 毫米)的全身性植入式电子设备感染的管理,往往颇具挑战性[1]。以往,当患者出现大型导线赘生物时,开胸手术并拔除导线是较为常见的考虑方案。不过,究竟是选择开放手术移除导线,还是采用血管内导线拔除的方式,这并非一概而论,而是需要根据患者的具体情况进行个体化决策[2]。需要注意的是,针对带有大型赘生物的导线实施血管内拔除操作时,由于存在导致血流动力学不稳定的肺栓塞风险增加的问题,所以临床医生往往会有所顾虑。而开放手术移除导线的方式,不仅会使患者承受较高的发病率和死亡率,而且术后恢复时间也相对较长。值得一提的是,在相关文献中,已经介绍了在导线拔除之前,运用特定设备对大型赘生物进行经导管抽吸的非手术方法,并且研究发现这种方法具有较好的效果[3]。
病例详情
在此,我们为大家介绍一位 54 岁男性患者的病例。该患者因耐甲氧西林敏感金黄色葡萄球菌(MSSA)菌血症入院治疗,检查中发现其植入式心律转复除颤器(ICD)导线存在较大赘生物。之后,我们采用 Inari FlowTriever 装置对赘生物进行了抽吸处理,并通过血管内激光技术将导线移除。
发病情况
一位 54 岁男性患者,因出现呼吸急促、发热症状前来我院就诊。患者入院时,生命体征基本正常。体格检查发现,患者活动后有气促表现,双下肢存在非凹陷性水肿(+)。
既往病史
该患者既往有多种疾病史。患有终末期肾病(ESRD),需长期接受血液透析治疗;存在非缺血性心肌病,左心室射血分数仅为 23%。因预防心源性猝死一级预防,曾植入自动化植入式心律转复除颤器(AICD)。此外,还患有阵发性心房颤动,日常服用阿哌沙班进行抗凝治疗。
鉴别诊断
综合考虑患者症状及病史,初步将肺炎、感染性心内膜炎、肺栓塞、急性心肌炎、急性心包炎以及急性心力衰竭加重等疾病纳入鉴别诊断范围。
辅助检查
1. 实验室检查:检查结果提示,患者脑钠肽(BNP)水平大幅升高,达到 2775 pg/ml;白细胞计数也有所升高,为 15.4×10⁹/L;降钙素原显著上升,数值为 39.83 ng/ml。血培养结果显示,患者存在耐甲氧西林敏感金黄色葡萄球菌菌血症。
2. 影像学检查:胸部平扫 CT 显示,患者双肺存在多个局灶性浸润影。考虑到患者处于慢性肾脏病(CKD)第 5 期,且仍保留部分残余肾功能,我们未立即进行胸部 CT 血管造影检查。鉴于高度怀疑感染性心内膜炎,我们进一步为患者进行了经胸超声心动图(TTE)检查。检查发现,三尖瓣上可见一长 2.1 cm、宽 0.5 cm 的条索状结构,高度怀疑为赘生物。同时,超声心动图还提示患者存在重度三尖瓣反流,双心室心力衰竭,右心室(RV)功能中度受损(通过目测评估),以及右心室中度扩张(右心室舒张末期基底段直径:4.7 cm [正常范围 2.5 - 4.1 cm])。
治疗措施
首先,我们给予患者静脉注射头孢唑林进行抗感染治疗。随后,为更精准地评估赘生物情况,我们为患者进行了经食管超声心动图(TEE)检查。检查结果清晰显示,源于 AICD 导线的一处大型赘生物,大小约为 2.5 cm×1.5 cm,呈丝状且活动度极高。在心脏收缩和舒张过程中,该赘生物可脱入右心房和右心室(图 1,视频 1),并引发了随后的重度三尖瓣反流(视频 2)。
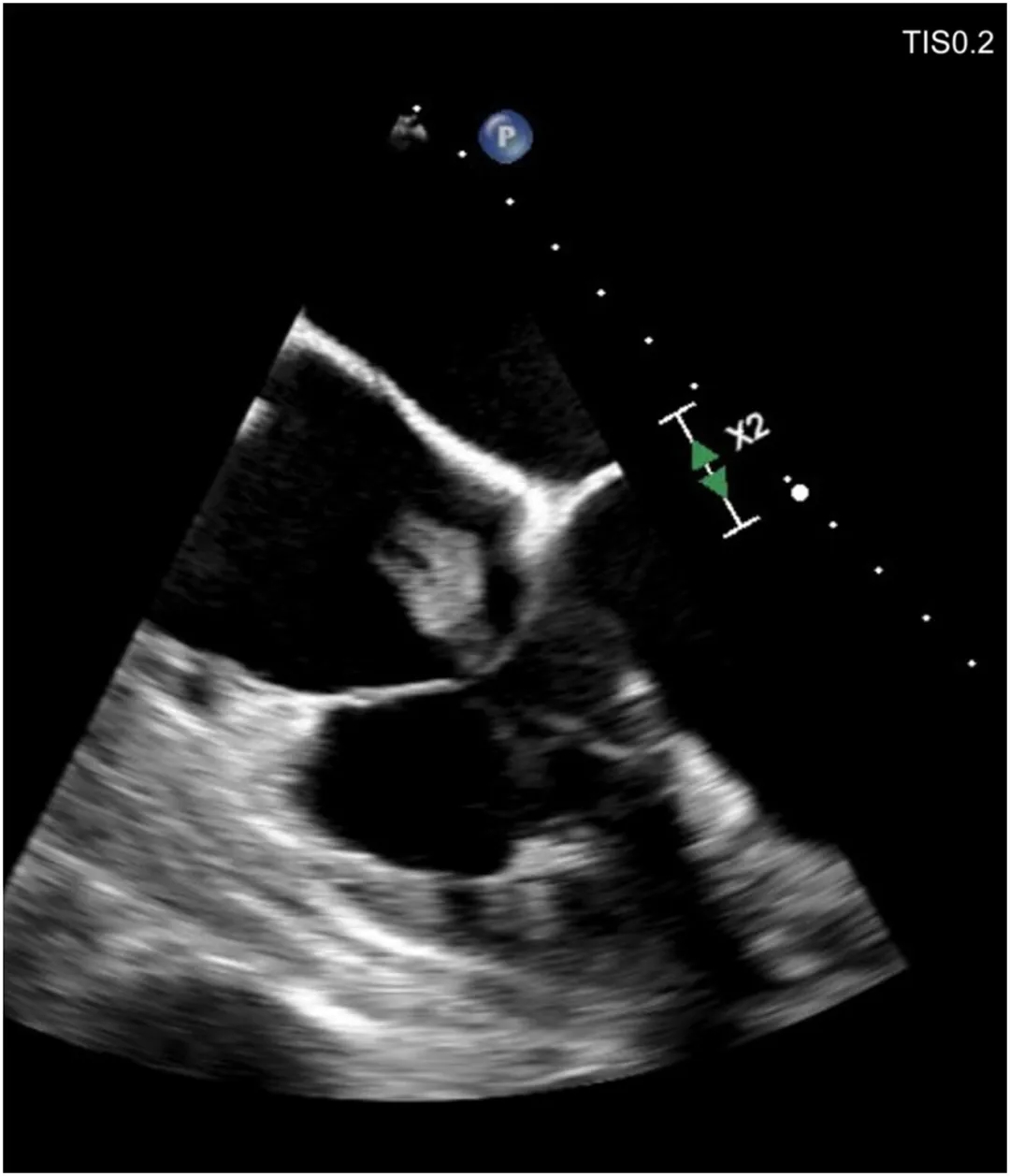
图1
经食道超声心动图(TEE)显示右心导线赘生物
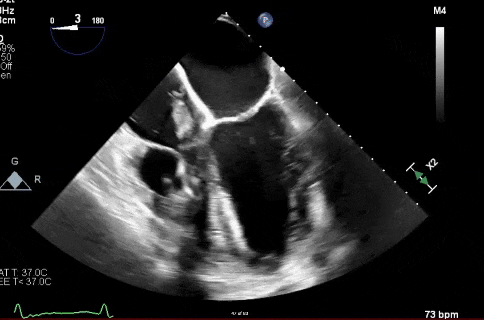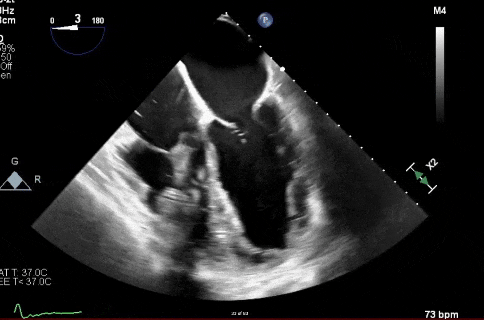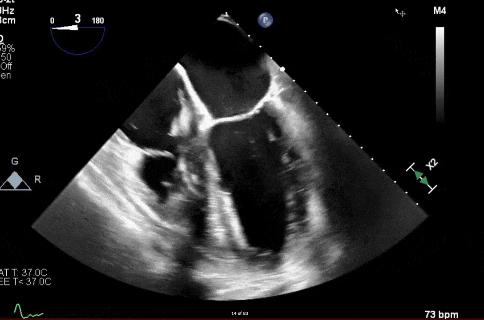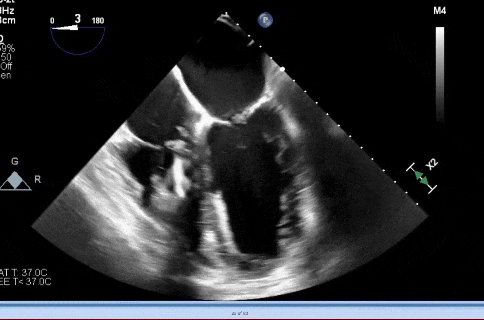
视频1
经食道超声心动图(TEE)显示右心导线附着赘生物
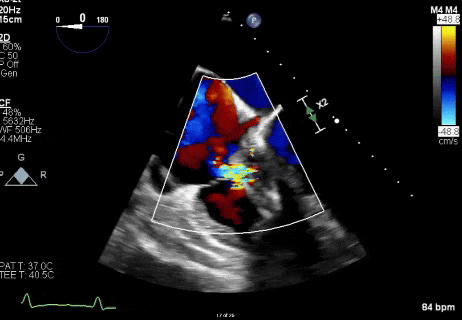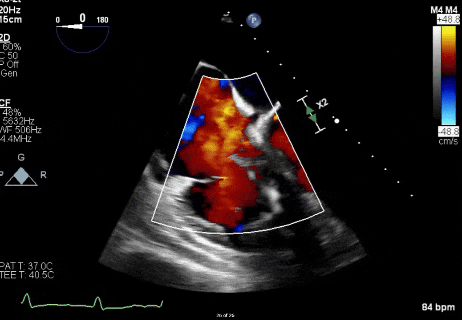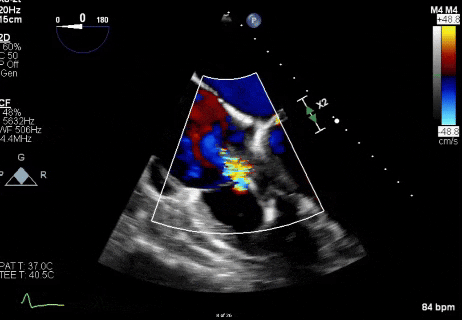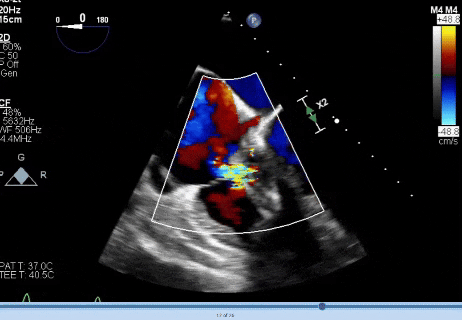
视频2
心外科团队评估了开放手术清除赘生物及拔除导线的方案,但鉴于患者存在多种高危合并症,被判定为极高危手术对象。考虑到激光血管内拔除导线可能导致脓毒性栓塞及持续菌血症风险,且患者存在右心室功能不全可能引发血流动力学不稳定的肺栓塞,故未采用该方案。
经心脏介入团队综合评估患者双心室功能障碍后,决定分阶段实施经皮介入治疗:首日采用FlowTriever导管行右心室导线赘生物机械抽吸,次日由电生理团队行心律转复除颤器导线拔除。
在芬太尼联合咪达唑仑静脉镇静下,经右颈内静脉入路,在X线及超声引导下使用FlowTriever血栓抽吸导管成功清除三尖瓣及ICD导线赘生物(视频3、4)。

视频3
FlowTriever装置经右心房进入右心室
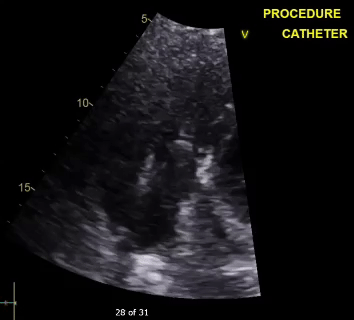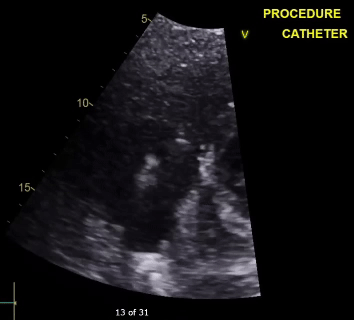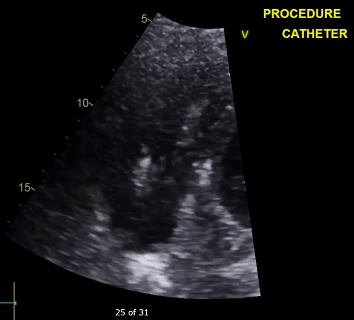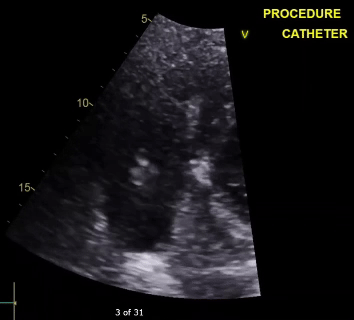
视频4
经胸超声心动图(TTE)显示FlowTriever装置位于右心房(RA)及右心室(RV)
针对患者慢性贫血,采用配备40μm滤网的Flowsaver系统将抽吸血液回输。手术过程中,医生团队首先尝试使用 24F Inari FlowTriever 导管进行多次抽吸,但仅吸出血液,未能成功清除赘生物。之后,改用 20F 弯头 FlowTriever 导管,仅经过单次操作,便顺利清除了三尖瓣赘生物(图2),这一过程通过术中超声得到了确认(超声图像详见视频 5)。术后,对清除的赘生物进行病理检测,结果显示其为两个大小分别为 2.5×0.6×0.6cm 及 3.8×0.5×0.1cm 的组织(图3),经鉴定为纤维坏死组织,伴发急性炎症反应,且存在可疑菌落(图 4 )。
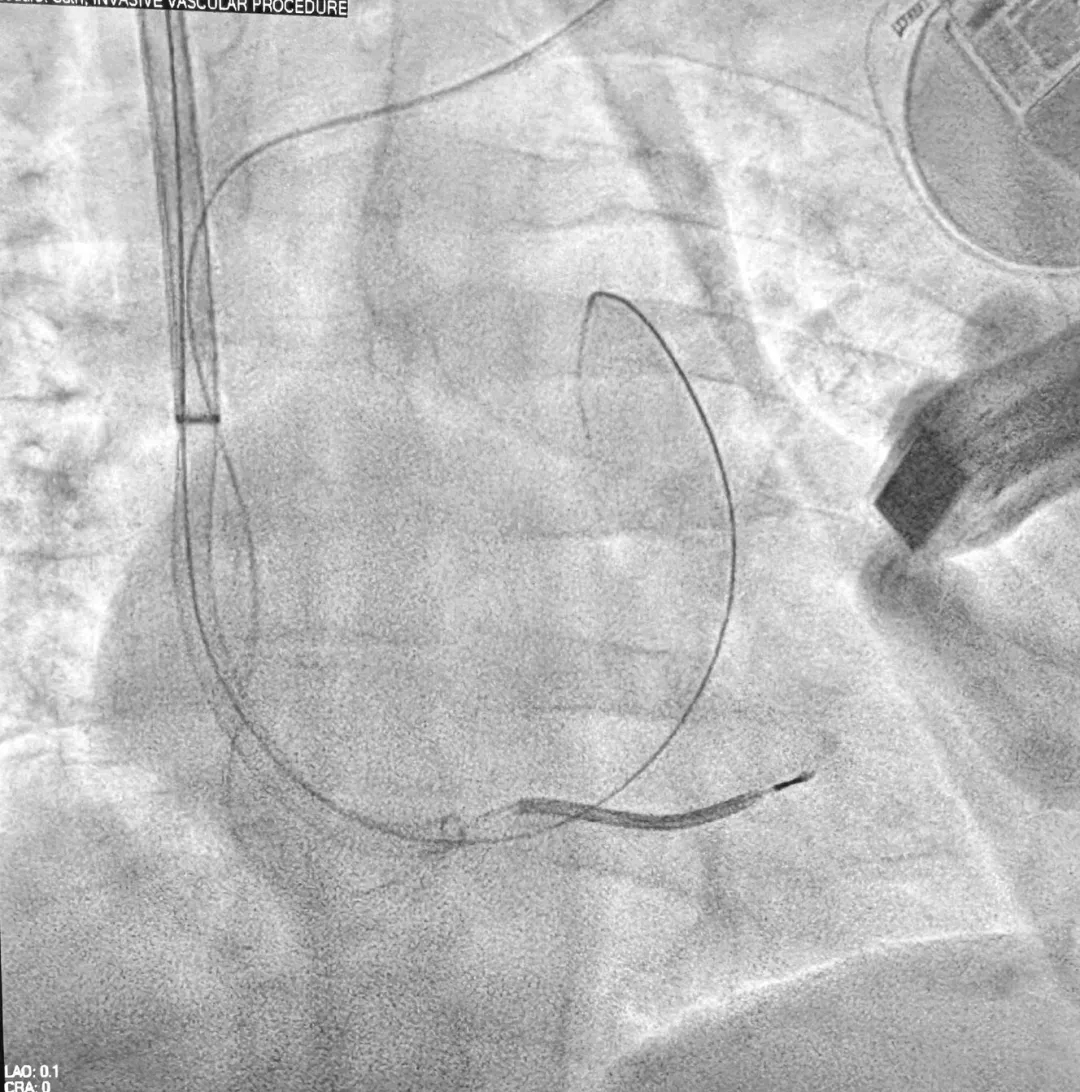
图2
24F导管引导20F导管进入右心室心尖部(使用Inari FlowTriever系统)
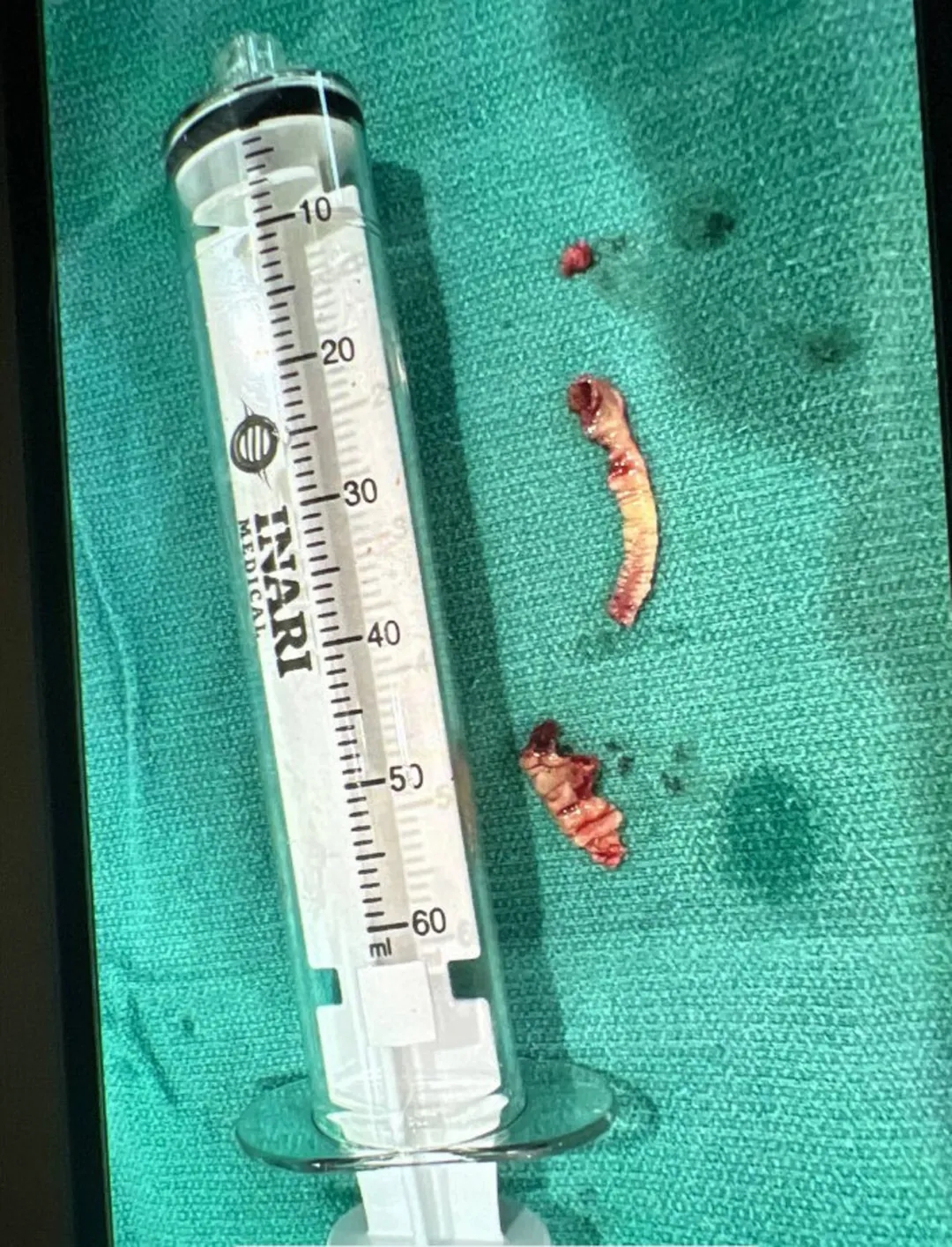
图3
赘生物标本
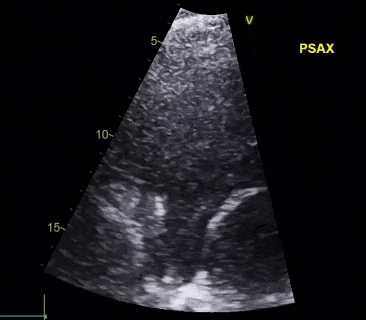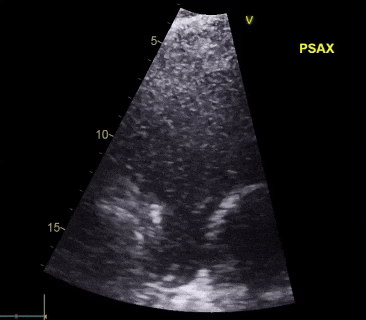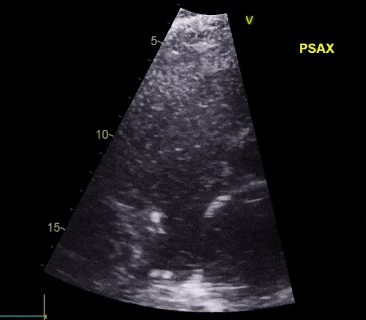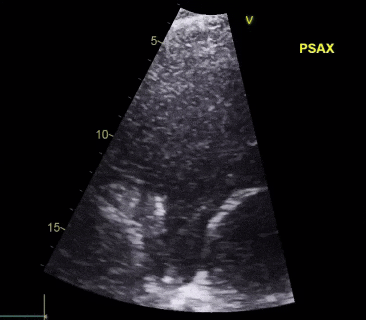
视频5
经食道超声心动图(TEE)显示右心导线赘生物
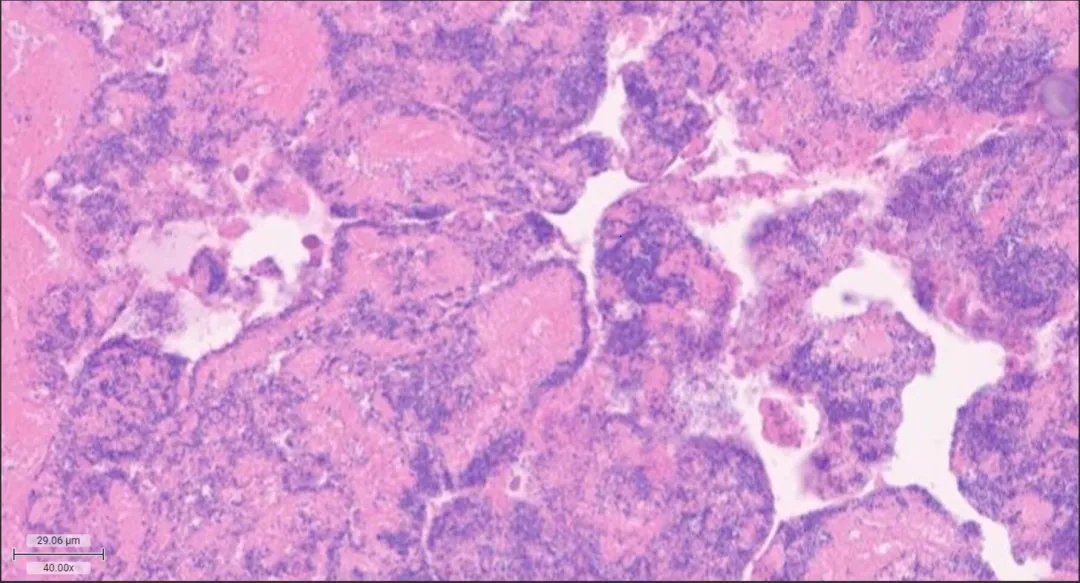
图4
病理切片显示大量无细胞纤维蛋白坏死碎屑伴极少量炎性细胞浸润,可见显著钙化碎屑,部分区域提示细菌菌落形成。
次日,患者成功接受右心室导线血管内激光拔除术,术中耐受良好。患者拒绝佩戴体外除颤器进行心源性猝死一级预防,经静脉抗生素治疗后病情稳定出院,拟在菌血症控制后门诊植入AICD。
讨论
本病例展示了使用Inari FlowTriever系统清除大型ICD导线赘生物的方法。处理器械相关感染性心内膜炎的关键在于彻底移除器械系统(理想情况下3日内完成)并延长抗生素疗程。一项大型心脏器械感染队列研究显示,未移除器械仅行抗菌治疗的患者死亡率增加7倍[4]。大型赘生物在导线拔除过程中存在栓塞风险,可能导致严重肺栓塞[5]。
2020年欧洲心律协会关于心脏器械感染的共识文件指出,对于>20mm的赘生物,在导线拔除术前或术中行经皮抽吸可作为替代方案。Inari FlowTriever作为快速血栓清除装置,其在肺栓塞中的应用已证实具有良好安全性和有效性[6]。其他用于赘生物清除的血栓切除系统包括Penumbra Indigo和AngioVac,后者虽可清除大血栓但需建立静脉-静脉旁路[7]。FlowTriever的优势在于提供多种导管规格,并配备40μm滤网的Flowsaver组件实现血液回输,这对本合并V期慢性肾病所致重度贫血的患者尤为重要。首篇FlowTriever系统用于大型赘生物清除的报道发表于2023年[8]。
心脏植入式电子装置(CIED)心内膜炎死亡率较高,尤其合并肾功能衰竭和心力衰竭患者[9]。CIED感染危险因素包括糖尿病、终末期肾病(ESRD)、COPD、糖皮质激素使用、既往装置感染史、心力衰竭及皮肤疾病。ESRD患者发生CIED感染的风险最高(OR 8.73,95%CI 3.42-22.31)[10]。本例患者兼具ESRD、心力衰竭和糖尿病多重危险因素,因预测死亡率过高不宜手术。
最终采用20F弯头FlowTriever导管成功清除赘生物,未发生手术并发症。
结论
本案例表明在血管内导线拔除前行经皮赘生物清除可降低栓塞风险,对于无需建立静脉旁路的大赘生物清除更具优势。该方法能减少开放手术需求,为高危手术患者提供救治机会。未来需大规模研究进一步评估心脏赘生物清除术的安全性和有效性。
参考文献:<滑动查看>
医谱app
扫码或者点击图片下载
微信公众号
扫码或点击图片关注
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、上载、下载、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。



发表留言
暂无留言
输入您的留言参与专家互动