超越“易损斑块”:JACC高危冠状动脉斑块立场综述
近期,JACC影像学子刊发布了一份立场综述:Vulnerable or High-Risk Plaque: A JACC: Cardiovascular Imaging Position Statement,系统性总结了高危斑块的概念和特征,扩展了关于高危斑块的观念。

数十年来,我们对急性冠脉综合征(ACS)发病机制的理解,一直被“易损斑块”(Vulnerable Plaque)——即以薄纤维帽粥样硬化斑块(TCFA)为代表的、随时可能破裂的病变——这一概念所主导。近期,《JACC: Cardiovascular Imaging》发布的立场文件指出,在有效降脂疗法普及、患者风险图谱演进的今天,这一传统观点已显狭隘。
近十年的研究成果提示,心血管医生和研究者应进行思维转变:由TCFA破裂导致的血栓形成,仅是冠脉事件的多种途径之一。一个常被忽视的关键机制是斑块侵蚀(Plaque Erosion),目前被认为是高达40%ACS的罪魁祸首,且其过程不涉及斑块帽的破裂,且目前还难以早期检测其前驱病变。此外,爆发性钙化结节(Eruptive Calcified Nodule)同样是引发血栓的重要原因。
实际上,动脉粥样硬化是一种动态的泛血管疾病。斑块表型可能会随着时间的推移而变化,并且斑块可能会在强化药物治疗后消退,但通常只在一个时间点进行评估。并且,大多数斑块破裂或侵蚀在可能是隐匿性发生的,但会导致斑块的快速进展。
因此,文章重新定义了“易损斑块”的概念,提出了更具包容性的术语——“高危斑块”(High-Risk Plaque)。
高危斑块的核心决定因素
三种斑块特征(易破裂斑块TCFA,易侵蚀斑块,爆发性钙化结节)描述了高危斑块的基本病理形态。
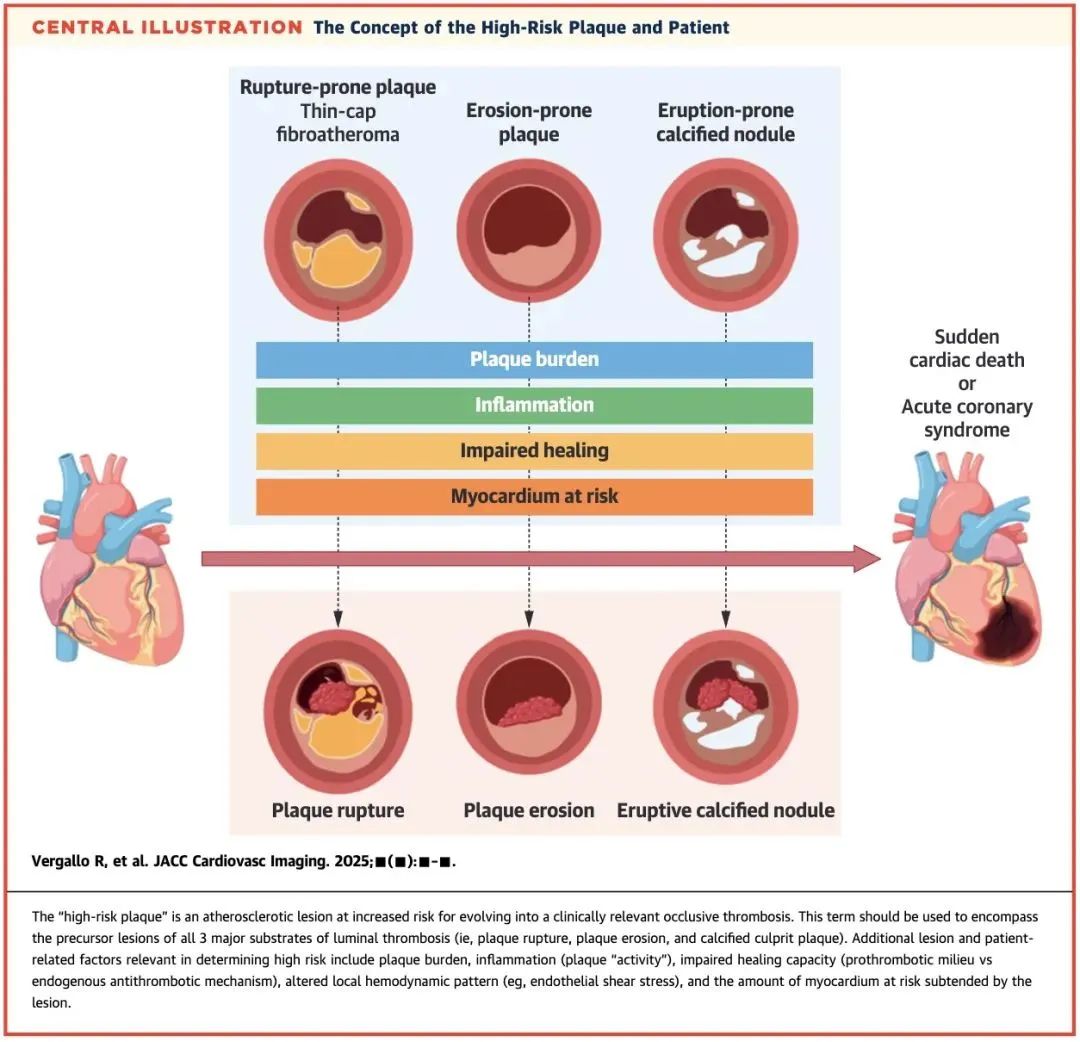
然而,斑块破裂产生血栓,其病理形态并非唯一决定因素。高危斑块的风险评估是一个多维度的综合过程,其最终是否导致心肌梗死或心脏性猝死等硬终点事件,也取决于以下几大关键因素的相互作用:
-
斑块负荷(Plaque Burden): 斑块的总体积,是预测不良事件的基石和强有力的独立因素。
-
炎症状态(Inflammation): 无论是斑块局部的微环境炎症,还是系统性的炎症反应,都对斑块的稳定性起着至关重要的作用。
-
斑块愈合(Healing Mechanisms): 人体存在着强大的斑块愈合机制。许多斑块的微小破裂或侵蚀在临床上是“静默”的,并能够自行愈合,但这一过程也可能导致斑块的进展和管腔的狭窄。促血栓与抗血栓因素的失衡,最终决定了事件的走向。
-
血流动力学(Hemodynamics): 局部血流环境,特别是内皮剪切力(Endothelial Shear Stress)的异常,是斑块发生、进展和失稳的关键诱因。
-
心肌危险区(Myocardium at Risk): 病变血管所供血的心肌范围,直接决定了事件发生后的临床严重程度。
因此,综述建议一种综合性的评估方式,即将"高风险斑块 "定义为:基于综合考虑斑块形态、负荷、生物活性、内在血栓形成性和位置,有更高倾向演变为临床相关血栓并导致ACS(主要是STEMI或1型NSTEMI)或心源性死亡的斑块。我们的关注点也应从孤立的“易损斑块”转向综合评估下的“高危患者”。
基于此,提出了一套更全面的高危斑块评估标准:
主要标准:纤维帽薄、脂质/坏死核心大、斑块负荷高、斑块内活动性炎症(巨噬细胞浸润)、内皮损伤/剥脱
次要标准:浅表突出的钙化结节、斑块内出血、新生血管形成、胆固醇结晶、正性重构、缺乏愈合痕迹、局部血流动力学紊乱、位于冠脉近中段(心肌危险区域大)
冠脉血栓的三大前期病变
-
易破裂斑块 (Rupture-Prone Plaque / TCFA): 这是典型的富含脂质的斑块,其薄而脆弱的纤维帽在炎症和机械应力下破裂,将促血栓的坏死核心内容物释放入血流。
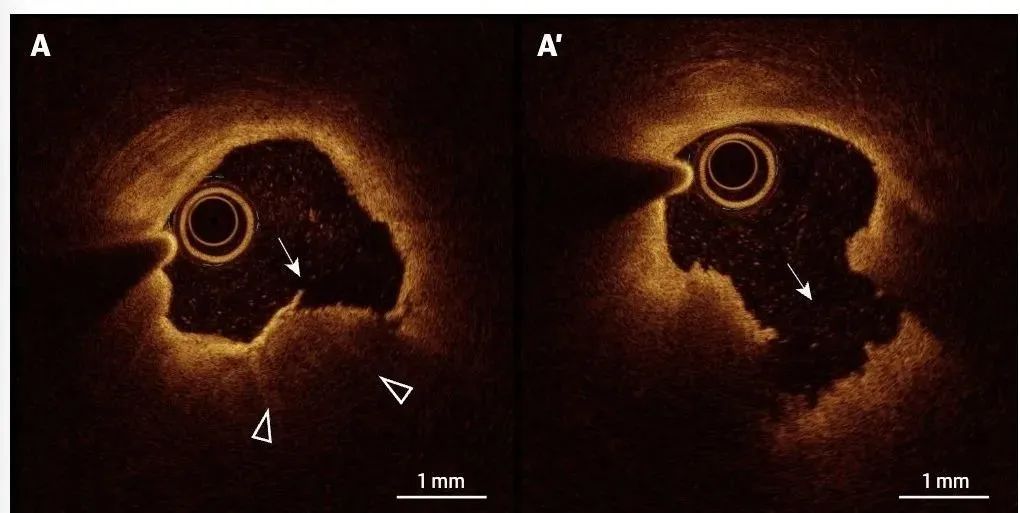
(A) 薄纤维帽粥样斑块,斑块内有一大块富含脂质的核心(低信号区,箭头所示为弥漫边界),表面覆盖着一层薄薄的纤维状箭头所示的高信号组织边缘(厚度小于 65 毫米),其断裂导致斑块破裂。(A’)脂质/坏死核心被排入管腔后,留下一个巨大的斑块空腔(箭头)。
斑块内出血(Intraplaque Hemorrhage, IPH) 是加速此类斑块恶化的一个关键因素。高危斑块内的新生血管(Vasa Vasorum)通常结构不成熟且容易破裂,导致血液进入斑块内部。这些出血不仅带来了大量富含胆固醇的红细胞膜,从而急剧扩张了坏死核心的体积,还引入了大量炎症细胞,进一步加剧了斑块的不稳定性。因此,IPH被认为是连接新生血管、炎症和坏死核心扩大的核心环节,显著增加了斑块破裂的风险。
-
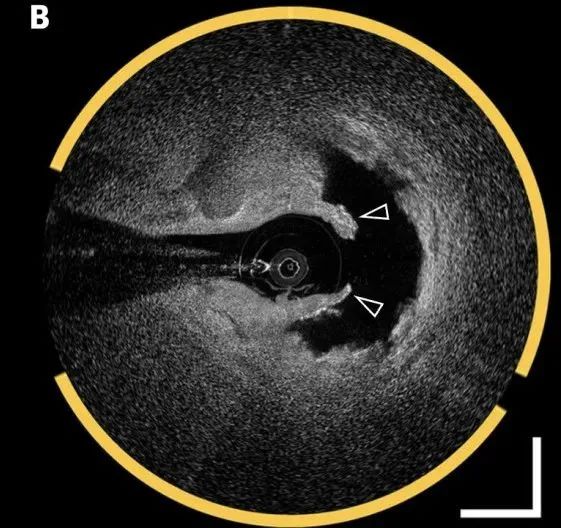
易侵蚀斑块 (Erosion-Prone Plaque): 这类病变通常富含平滑肌细胞和细胞外基质,其表面的内皮细胞层发生剥脱,导致血小板直接暴露于内皮下基质而形成血栓,但斑块帽本身保持完整。
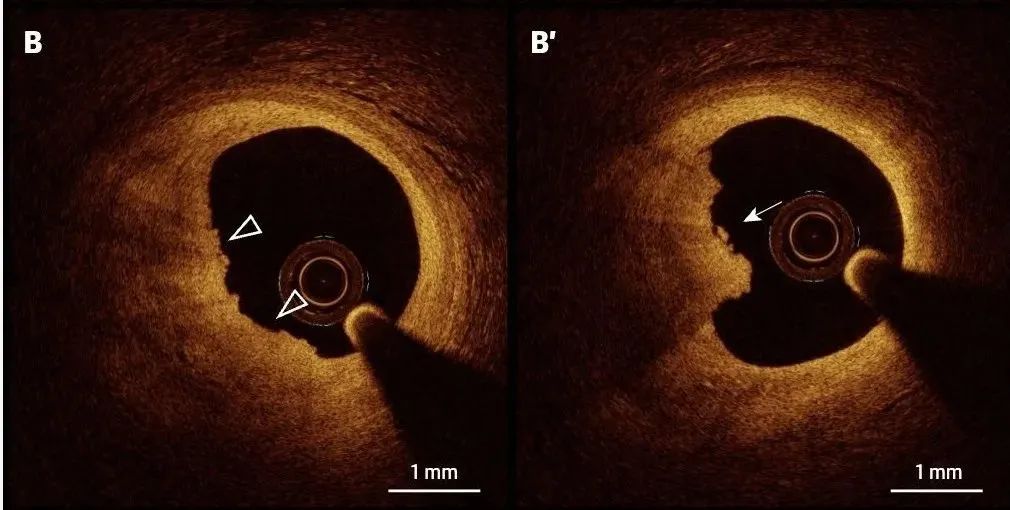
(B) 偏心斑块,主要为纤维斑块,表面不规则(箭头),将演变为斑块侵蚀(B’),其中血栓明显,表现为不规则的肿块附着在血管壁上并突出到管腔内(箭头),但没有内皮连续性破坏的迹象。
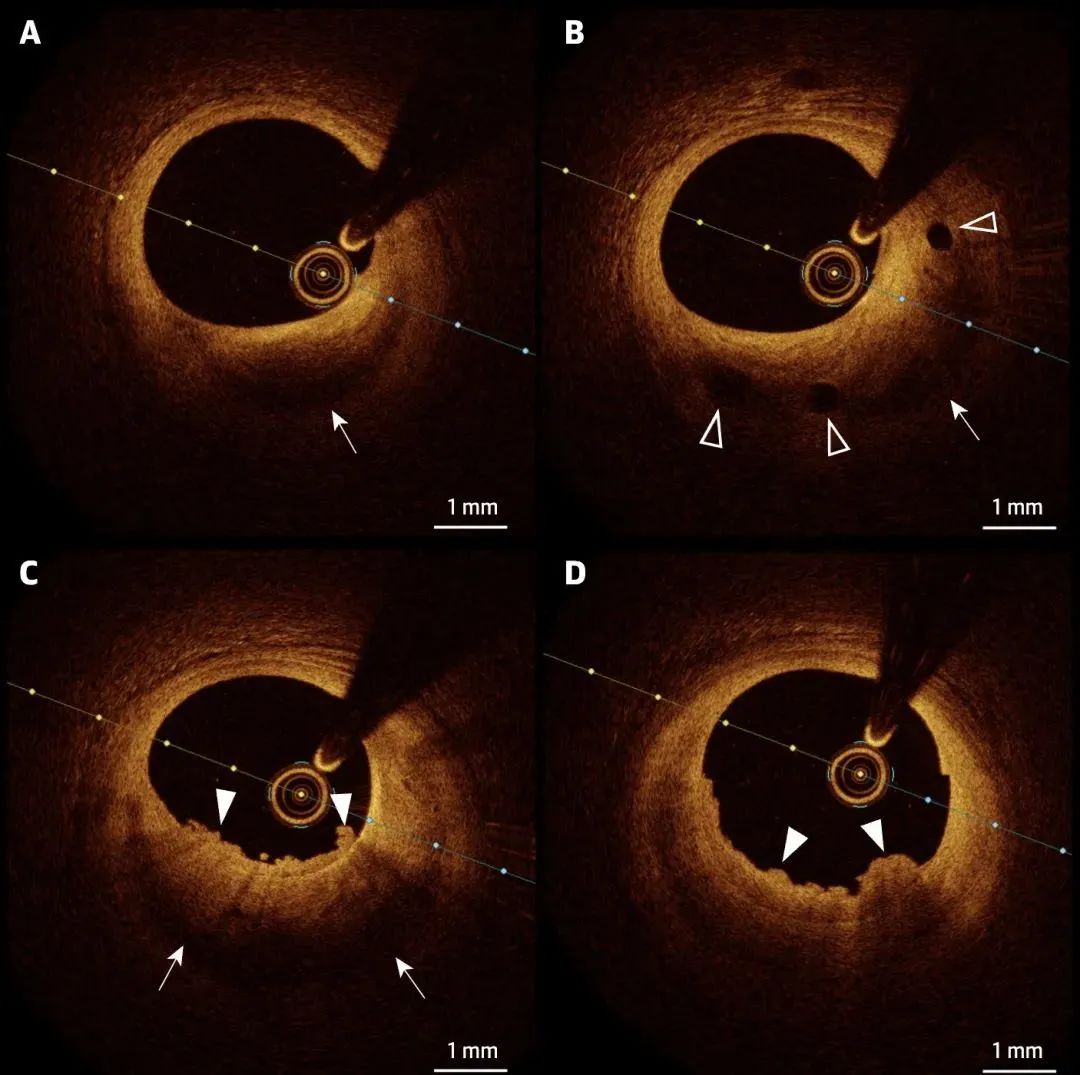
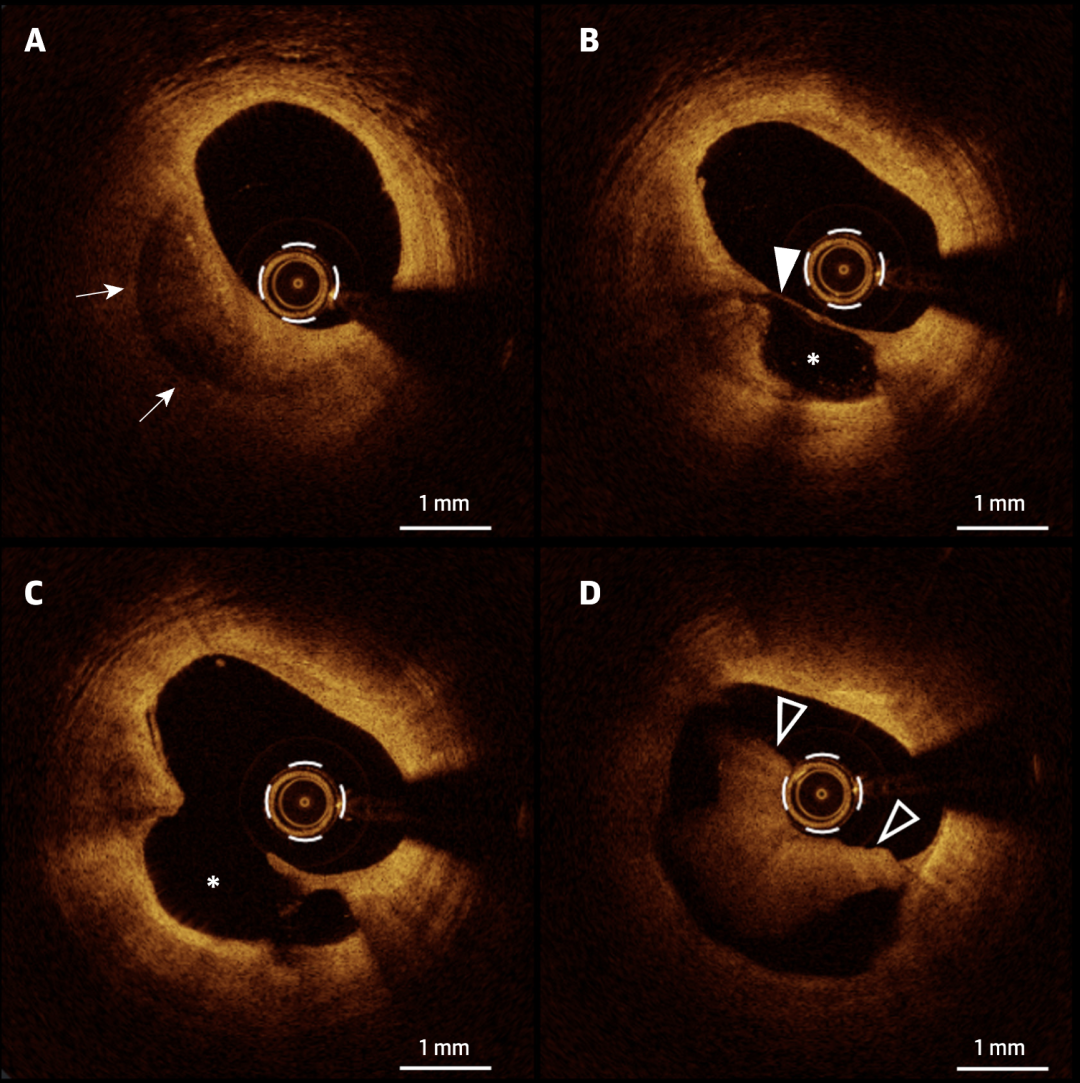
斑块内出血与斑块侵蚀
(A、B)厚盖纤维斑块,中央为新月形低信号区(箭头),提示 IPH,通常发生在扩大的内膜新生血管附近(B 中为箭头)。(C、D)IPH(箭头)部位出现侵蚀,并伴有白色血栓(白色箭头)。
-
爆发性钙化结节 (Eruptive Calcified Nodule): 坚硬的钙化结节穿透纤维帽并突入管腔,其不规则的表面可直接激活凝血系统。这种情况常见于血管扭曲和机械应力集中的部位。
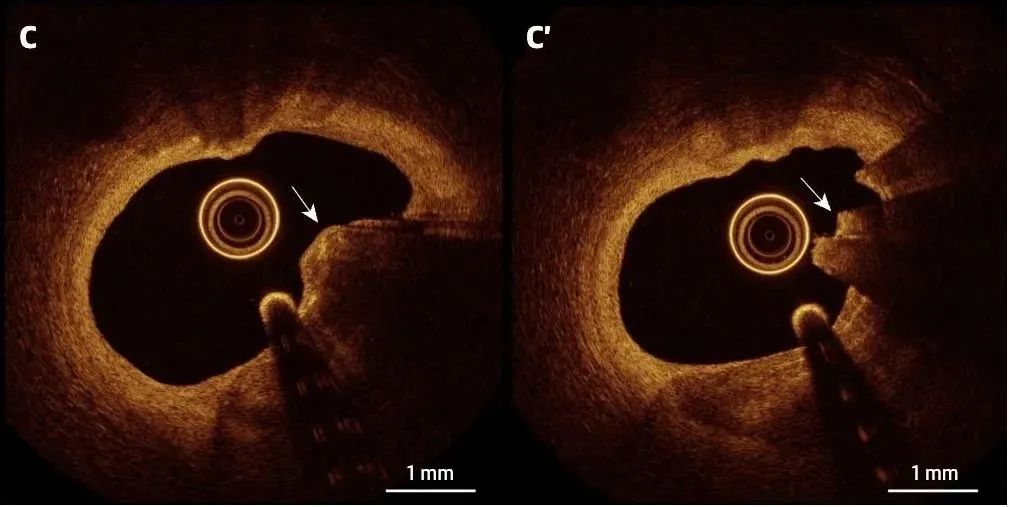
(C) 偏心结节性钙化斑块突入管腔,由薄薄的组织边缘覆盖。爆发性钙化结节(C’)显示不规则、低信号结节突出,伴有背影(箭头)和少量附着的红色血栓。
斑块的动态演变:愈合与稳定
动脉粥样硬化是一个动态过程。许多斑块失稳事件在临床上并无症状,机体通过形成新的内膜层将其“覆盖”并愈合。这些愈合后的分层斑块,在慢性稳定型冠心病患者中极为常见,但在反复发生ACS的患者中则较为少见。这提示我们,斑块的内源性愈合能力,或许是区分“高危患者”与“稳定患者”的关键生物学特征。
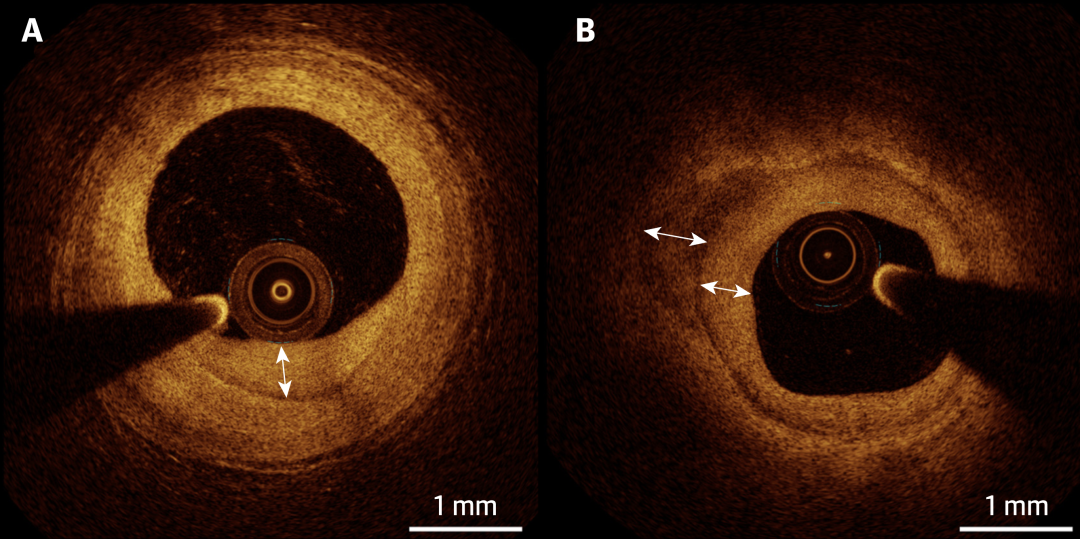
斑块愈合,(A) 典型的斑块 "分层 "模式,纤维斑块上覆盖着愈合组织边缘(双箭头)。(B)"多层 "斑块,两层不同的光学强度(双箭头)。
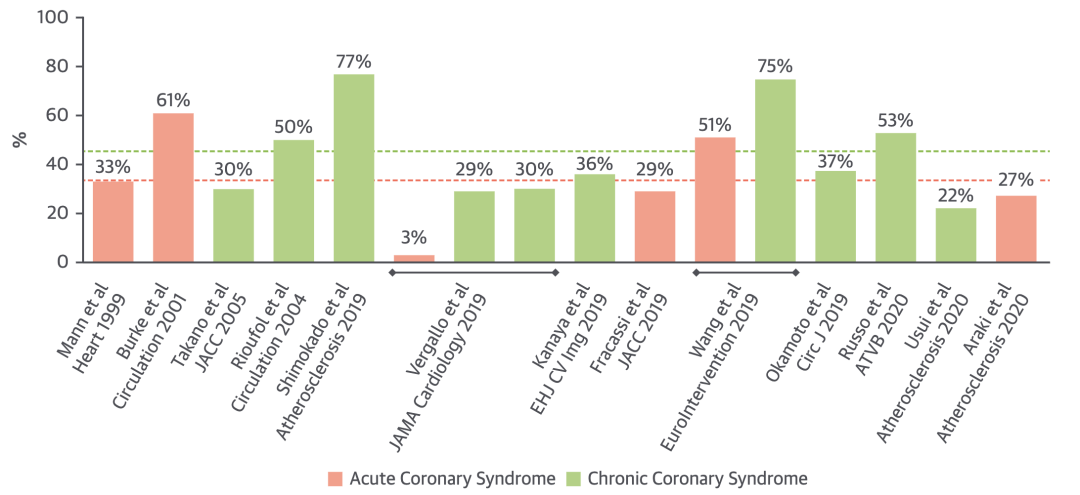
愈合斑块的发生率。平均而言,CCS患者(绿色虚线)的斑块愈合率高于ACS患者(红色虚线)。
高危斑块分布的偏好区域
高危斑块在冠状动脉内的分布并非随机,而是有明显的位置“偏好”,这主要与血流动力学和解剖结构相关。
-
血流动力学决定的“热点区域”:尽管动脉粥样硬化是全身性疾病,但斑块倾向于在血流紊乱的区域形成,例如血管的分叉处、内弯侧等。在这些区域,低的内皮剪切力(Low Endothelial Shear Stress) 是一个关键的致病因素,它会促进斑块向高危特征(如富含脂质、薄纤维帽)发展。
-
冠脉近、中段是高危斑块高发区:大量病理学和腔内影像学研究一致证实,高危斑块,特别是薄纤维帽粥样硬化斑块(TCFA),绝大多数位于冠状动脉的近段和中段。其中,左前降支(LAD)的近段是最为经典的“高危地带”。
-
不同斑块类型的共同偏好区域:不仅是经典的斑块破裂,斑块侵蚀也同样好发于冠脉近段,尤其是LAD和邻近分叉的部位,这进一步印证了紊乱的血流动力学在驱动不同类型斑块失稳中的共同作用。
-
临床意义:这种位置偏好具有重大的临床意义。因为近中段病变一旦发生血栓事件,其所波及的心肌危险区(Myocardium at Risk)范围更大,从而更有可能导致严重的临床事件,如大面积心肌梗死或心脏性猝死。
多模态影像精准构建冠状动脉斑块风险画像
In vivo检测高危斑块必须依赖于先进的无创和有创影像学技术。
无创影像学手段
|
|
|
|
|
|
|
|
|
|
|
|
有创影像学手段
| IVUS |
|
|
| OCT |
|
|
| NIRS |
|
|
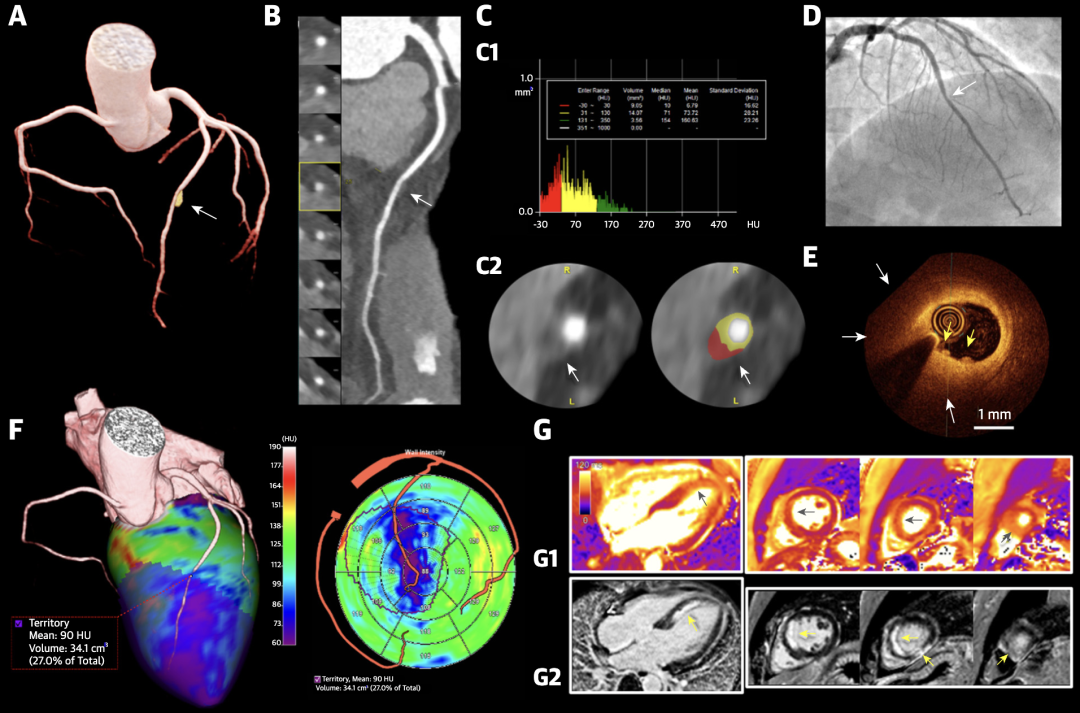
多模态影像:无已知心血管危险因素,中度冠状动脉阻塞的 44 岁女性,因斑块侵蚀引发ACS。CTA(图C)显示纤维脂肪为主(黄色),伴坏死核心(红色)。OCT(图E)显示一个小的白色血栓(黄色箭头)覆盖在纤维血斑块的内皮表面(白色箭头),没有破裂迹象。MRI(图G)显示透壁心肌水肿伴LGE。
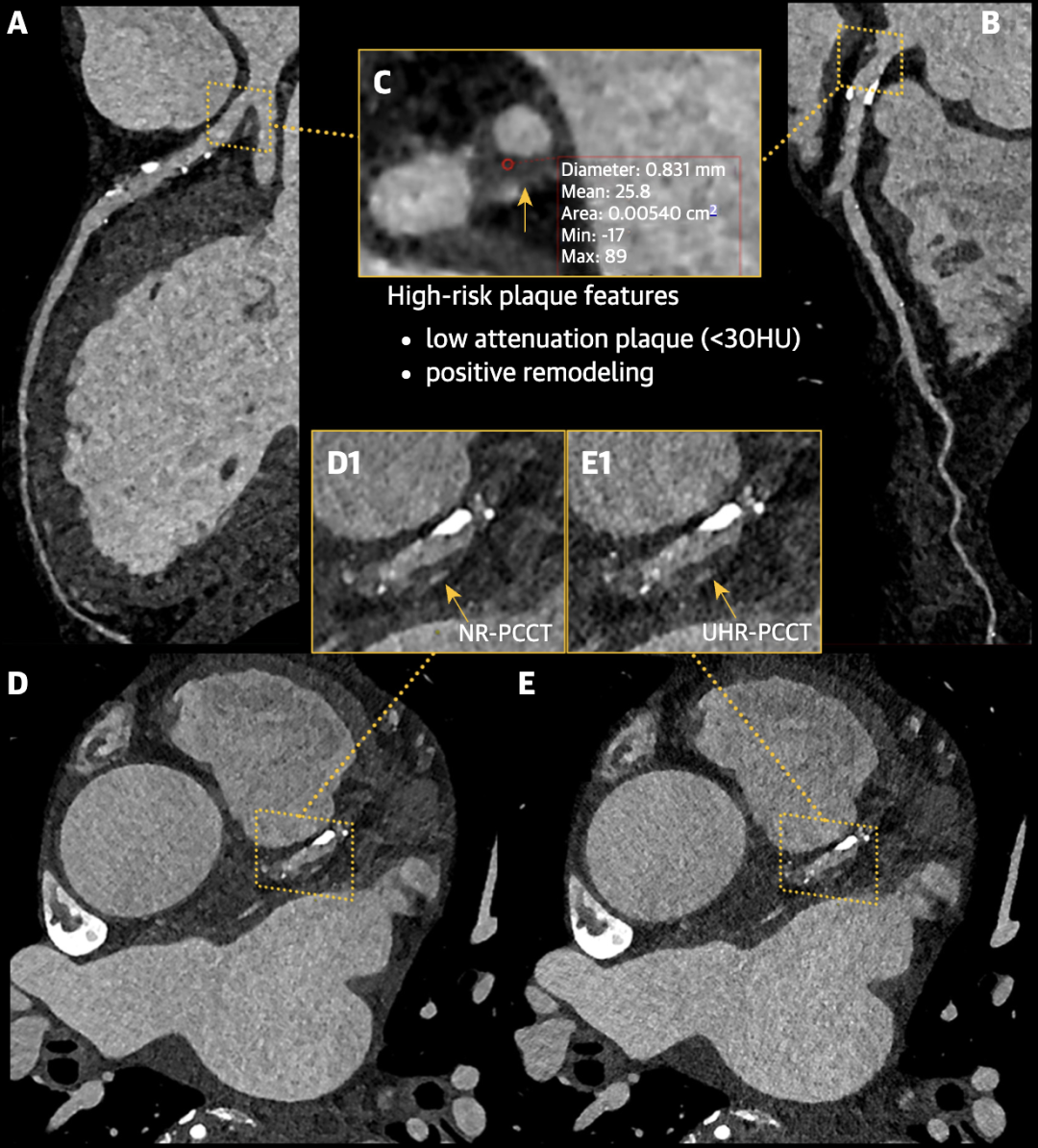
光子计数CT(PCCT)的超高分辨率影像(UHR,ultra high resolution)
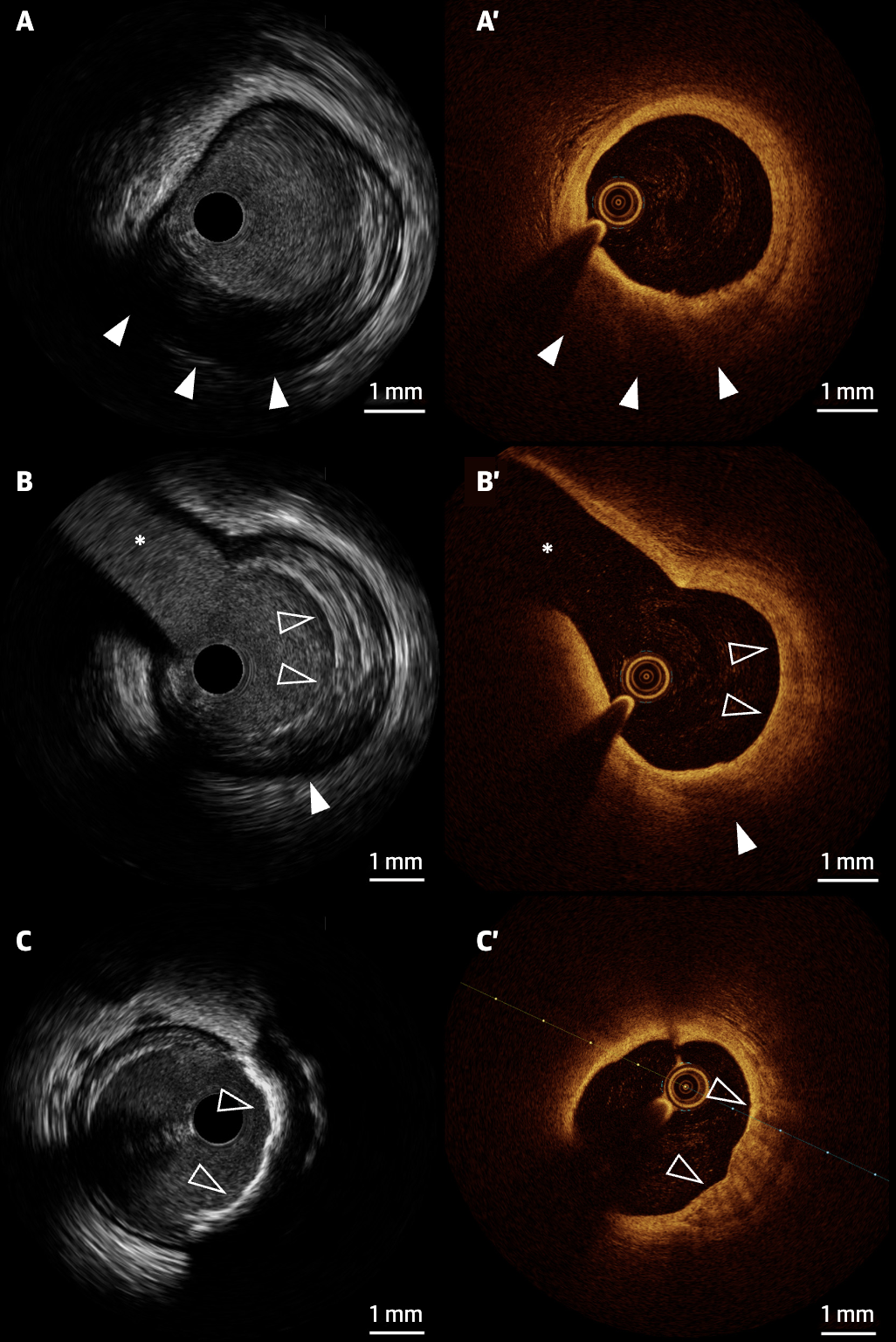
IVUS 和 OCT 冠脉成像的比较
(A) 脂质斑块:IVUS 可观察到衰减斑块,即回声衰减,无高回声前缘;OCT 成像可观察到低反向散射、低信号区域,其弥漫边界被高反向散射纤维帽覆盖。
(B)纤维斑块:IVUS 上可以看到纤维化组织普遍存在的斑块,表现为具有中等回声的区域(空箭头);在斑块内还可以看到一个小的、局部的、回声衰减区域(白色箭头);OCT 上,同一斑块表现为高反向散射、信号丰富的区域(空箭头),以及一个小的、具有弥散边界的低信号区(白色箭头)。
(C)钙化斑块:IVUS 上可以看到一个带声影的高回声偏心斑块(C,空箭头);在 OCT 成像上,钙质显示为一个低反向散射的异质区域,边界清晰。
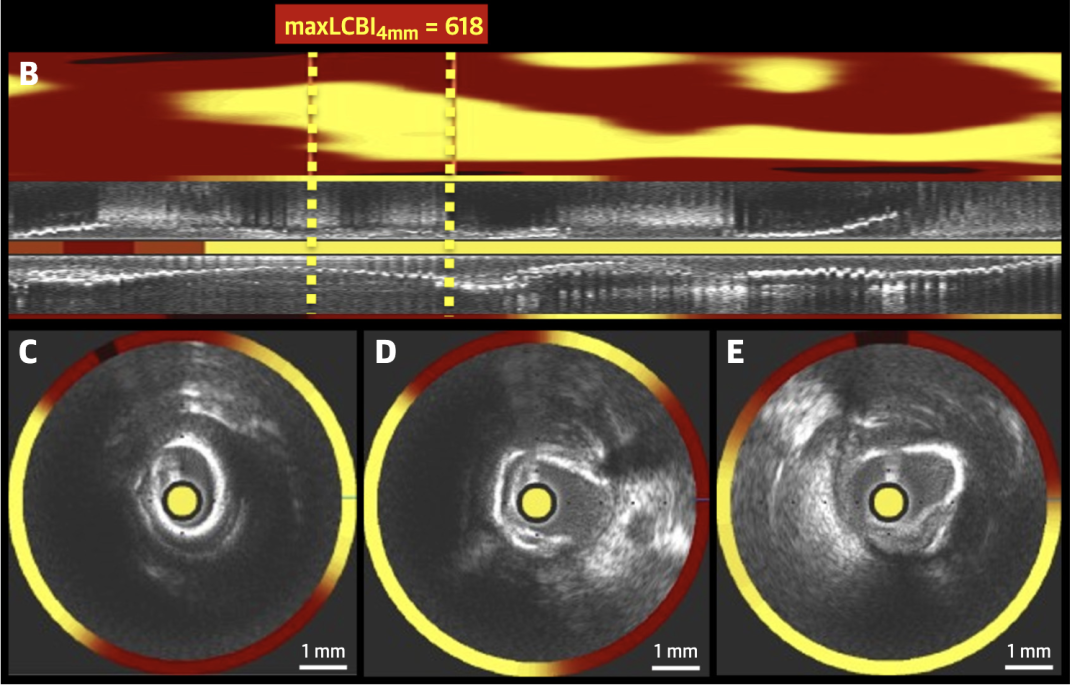
OCT-NIRS显示破裂斑块周围脂质(黄色弧线)
原文:Vergallo, R, Park, S, Stone, G. et al. Vulnerable or High-Risk Plaque: A JACC: Cardiovascular Imaging Position Statement. J Am Coll Cardiol Img. 2025 Jun, 18 (6) 709–740.
- End -
关注我们
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。

发表留言
暂无留言
输入您的留言参与专家互动