国际动态:Circulation:肠道菌群与亚临床动脉粥样硬化有关
 背景
背景动脉粥样硬化性心血管疾病(CVD)是导致患者死亡和残疾的主要原因。胃肠道的微生物群落(亦称为肠道微生物群)与动脉粥样硬化疾病有关,其被推测以三种潜在机制影响动脉粥样硬化的进展。第一种,通过微生物代谢产物来干扰宿主代谢,包括脂质代谢。第二种,活细菌或细菌结构成分(如内毒素)进入血液导致全身低度炎症,从而加剧动脉粥样硬化发展。第三种,动脉粥样硬化斑块内细菌DNA的发现提示细菌可能通过直接感染斑块并加速动脉粥样硬化进展。
肠道和口腔的微生物群不是两个独立的群落,而是相互联系的。据报道,在颈动脉粥样硬化斑块中发现的细小杆菌和链球菌等与口腔细菌有所重叠。肠道可能是口腔致病菌进入血液的生态位点或进入途径。然而,动脉粥样硬化相关肠道细菌种类与口腔中相应细菌种类的丰度之间的关系尚不清楚。
本研究旨在确定肠道微生物组与基于计算机断层扫描的冠状动脉粥样硬化测量之间的关系,并探讨相关的临床相关性。
在基于人群的SCAPIS(瑞典心肺生物影像研究,主要关注心血管和呼吸系统疾病,纳入了来自瑞典6个地点的30154名年龄在50至64岁之间的参与者)中,对8973例无明显动脉粥样硬化症状的参与者进行横断面研究。冠状动脉粥样硬化采用冠状动脉钙化评分和冠状动脉CT血管造影。通过粪便样本的霰弹枪宏基因组测序评估肠道微生物群物种丰度和功能潜力,并通过调整心血管危险因素的多变量回归模型评估菌群与冠状动脉粥样硬化的相关性。评估有所相关的物种与炎症标志物、代谢物和唾液中相应物种的关联。
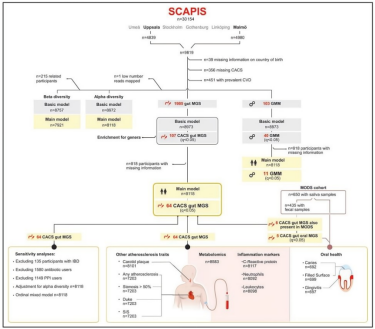
图1 总研究设计流程图
研究样本的平均年龄为57.4岁,其中53.7%为女性。40.3%的患者有冠状动脉钙化,5.4%的患者至少1处冠脉狭窄,且闭塞50%。
64种微生物物种与冠状动脉钙化积分(CACS)相关,与心血管危险因素无关。其中51种与CACS呈正相关,13种与CACS负相关(图2和3)。其中观察到的咽峡炎链球菌和口腔链球菌口腔亚种的关联性最强(P<1×10-5)。
基于冠状动脉计算机断层造影的测量结果大致相似。在64个菌种中,19个菌种(包括链球菌和其他常见于口腔的菌种)与高敏感性C反应蛋白血浆浓度有关,16个菌种与中性粒细胞计数有关。
口腔中常见的肠道微生物种类与血浆吲哚丙酸呈负相关,与血浆次级胆汁酸和丙酸咪唑呈正相关。在Malmö后代牙科研究中,包括3种链球菌在内的5种细菌与唾液中的同一种细菌相关,并与较差的牙齿健康有关。硝酸异化还原、厌氧脂肪酸β-氧化和氨基酸降解的微生物功能电位与冠状动脉钙评分相关。

图2 研究中所调查物种的枝状图
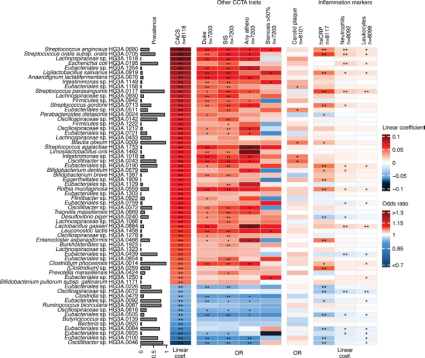
图3 冠状动脉钙评分相关肠道物种与动脉粥样硬化、炎症和感染标志物的替代测量之间的关系图
肠道细菌被认为通过局部或远端动脉粥样硬化斑块感染,或通过产生致动脉粥样硬化代谢物来影响动脉粥样硬化的形成和进展。之前,肠道微生物群与冠状动脉粥样硬化的关系仅在常接受治疗的有动脉粥样硬化症状的患者中进行过研究,由于药物可能导致菌群组成成分发生极大变化,因此这些研究存在很高的偏倚风险。本研究的研究对象为SCAPIS队列中无早期心血管疾病的大规模人群,采用影像手段详细评估冠状动脉粥样硬化,通过霰弹枪宏基因组学对个体的肠道微生物组进行深入表征,鉴定64种与CACS相关的独立于危险因素的微生物物种。其中一些细菌与炎症及感染的循环标志物有关,也与唾液样本中相应的细菌种类有关,而这些细菌又与口腔健康状况恶化有关。因此,值得继续研究这64种微生物物种在动脉粥样硬化形成中的作用。
本研究提供了证明肠道微生物群组成与冠状动脉粥样硬化和全身炎症标志物之间存在关联的相关证据,关联性的特征是链球菌属和其他口腔常见的微生物物种的丰度增加。有必要开展进一步的纵向和实验研究来探索细菌成分在动脉粥样硬化形成中的潜在影响。
本研究有一些局限性。首先,尽管本研究的队列比之前分析的队列大7倍不止,但参与者较少有高水平的亚临床动脉粥样硬化,这降低了统计效力。其次,整个胃肠道的微生物组成变化较大。粪便样本中含有来自远端结肠的微生物种群,而来自其他部位(如小肠)的微生物种群较少。因此,无法确定粪便样本中微生物物种的关联性是否得到充分体现。第三,本研究未考虑细菌种类之间的相互作用,如协同作用与冠状动脉粥样硬化的关系。第四,横断面研究设计限制了因果推理。最后,关于抗生素治疗的数据不包括住院治疗中提供的抗生素,然而,在这个年龄组中,预计不会有大量住院治疗的患者。在未来的研究中,应该使用不同的因果推理方法来确定所鉴定的物种是否与动脉粥样硬化的发展有因果关系。
通过结合基于大量人群的队列研究和影像学评估亚临床冠状动脉粥样硬化的数据,我们发现肠道中几种微生物物种的丰度与冠状动脉粥样硬化、炎症生物标志物及其口腔对应微生物均相关。如果它们存在因果关系,那么这些微生物物种种可能通过直接感染或改变宿主代谢等途径导致动脉粥样硬化的形成和进展。未来相关研究将表明这些肠道微生物物种是否可以用作动脉粥样硬化潜在的生物标志物或治疗靶点。
原文链接:
https://pubmed.ncbi.nlm.nih.gov/37435755/
关注医谱学术,实时掌握最新动态!
医谱app
扫码或者点击图片下载
微信公众号
扫码或点击图片关注
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、上载、下载、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。



发表留言
暂无留言
输入您的留言参与专家互动