陈珏教授丨知己知彼:国内外钙化治疗路径及最新临床研究解读

当前,钙化病变治疗受到业内广泛关注,尤其严重钙化病变对于介入医生而言是一项严峻的挑战。国内外针对不同程度钙化采取不同诊疗策略。IVUS(血管内超声)和OCT(光学相干断层扫描)腔内影像学钙质评分能准确评估钙化程度和预测支架膨胀情况,尤其IVUS被认为是评价钙化病变的“金标准”。创新性治疗方法如冠状动脉内旋磨术(RA)、轨道旋磨术(OA)、冠状动脉血管内碎石术(IVL)等展现出良好应用前景。近期,中国医学科学院阜外医院陈珏教授带来国内外钙化治疗路径及最新临床研究解读,致力为钙化病变患者提供更安全有效的治疗方案和精准个性化的治疗选择。

钙化病变的流行病学
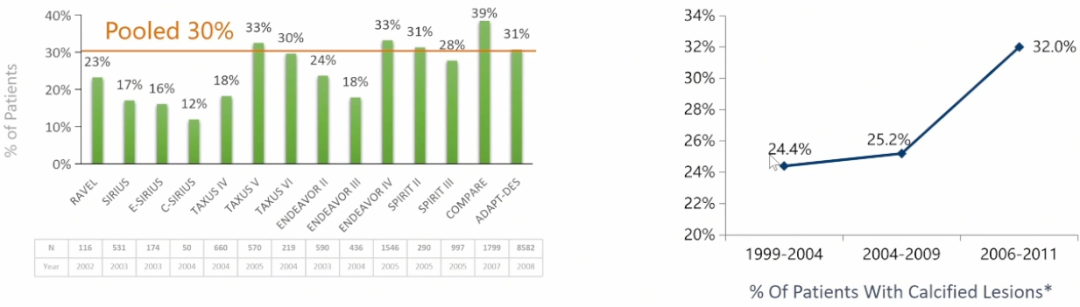
钙化病变在老年患者和相对年轻的患者中都比较常见。整体来讲,接受择期冠脉介入治疗的患者,中重度钙化病变发病率约为30%。下图左展示了14项DES研究中血管造影下中重度钙化的发病率,从中可以看出不同研究存在一些差距,但整体来看,时间轴往右的研究中钙化病变比例是逐渐增高的趋势,基本达到30%。图右提示钙化发生率增加。
严重钙化是预测心血管不良事件的独立危险因素
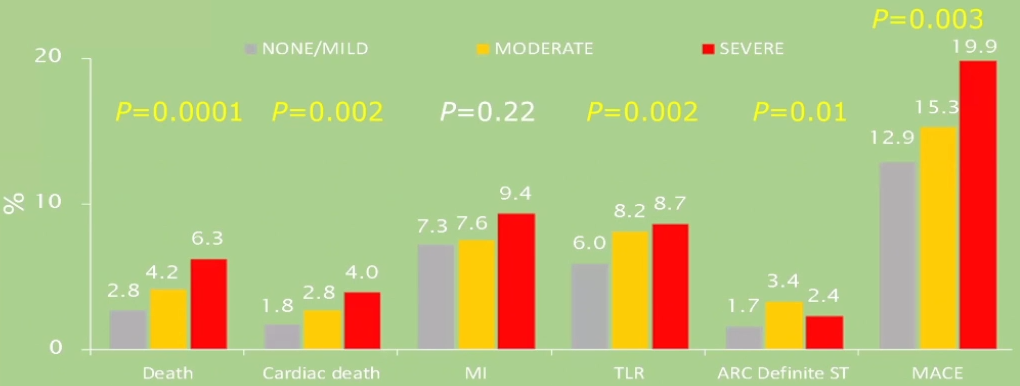
研究对6855名ACS患者不同钙化程度的1年缺血结果进行回顾性分析,发现在重度钙化病变中,全因死亡、心原性死亡、靶病变血运重建、支架内血栓形成、MACE(主要心血管不良事件)风险要明显高于轻度钙化病变的患者。
严重钙化增加介入治疗的难度和风险
严重钙化病变对于介入医生而言是一项严峻的挑战。我们可能会遇到器械不能到位、导丝断裂、球囊不能扩张或破裂、支架脱落或变形等介入器械难题,冠脉损伤夹层、血管急性闭塞、冠脉穿孔发生心包填塞、心肌无再流、急诊CABG、死亡等并发症,以及支架膨胀不全或贴壁不良、急性/亚急性或晚期血栓形成、支架内再狭窄等近远期风险。
对于这一类钙化病变,在冠脉造影后发现严重钙化病变的情况下,如何进行有效评估和预处理非常重要。IVUS是评估钙化病变的“金标准”,IVUS钙质评分可预测严重钙化病变的支架扩张情况:
1.在严重(>270°)表浅钙化病变中,IVUS钙化评分包括>270°表浅钙化的长度、钙化的角度、是否存在钙化结节和小血管(<3.5 mm),这些因素可预测支架在最大表浅钙化部位的膨胀不充分。
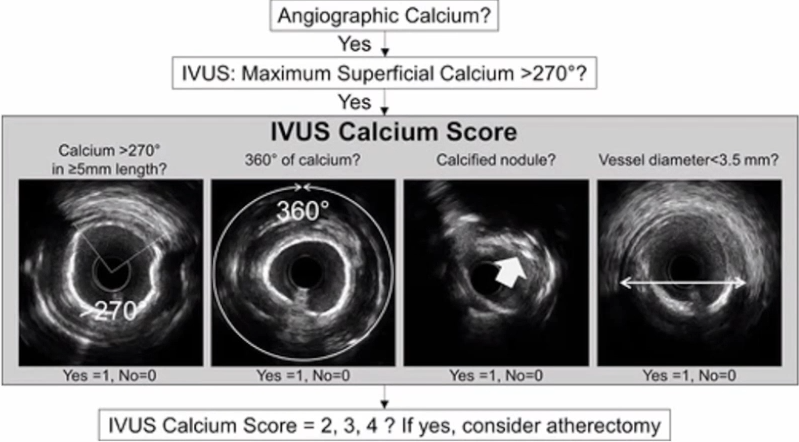
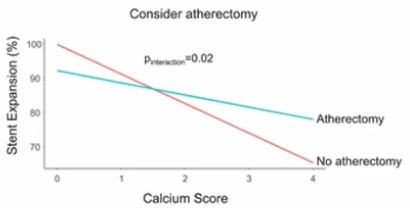
2.如果钙化分数≥2、建议使用旋磨术;如果在支架植入前使用,可以预期钙化断裂和良好的支架扩张。
OCT的钙化积分可预测支架膨胀
OCT能够精确测量钙化病变角度、病变长度及钙化厚度,根据钙化积分,预测支架膨胀。
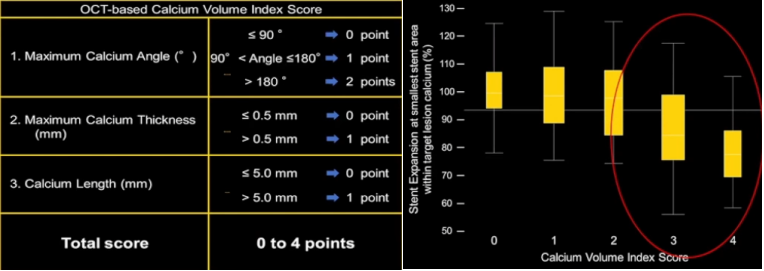
在腔内影像的指导下,我们可以根据钙化病变的特点选用不同的处理方法:若钙化<270°,可以采用常规NC球囊预处理;若有钙化结节存在,首选RA或OA;若钙化幅度较大>270°时,可以启动RA、OA、振波球囊和激光等,很多情况下需要联合多种方法。
2021年中国专家共识推荐使用旋磨的情况:
1.当器械不能通过时,即可启动旋磨;
2.钙化结节会导致器械通过困难、球囊破裂甚至血管破裂等严重并发症发生,通常需要行RA治疗;
3.球囊扩张压力达16 atm未充分扩张病变时,推荐行IVUS或OCT检查评估,或直接行RA治疗;
4.对IVUS检查提示成角超过271°的内膜钙化,或OCT检查提示钙化积分4分者(最大钙化弧度>180°,病变长度>5mm、最大钙化厚度>0.5mm),可直接行RA。
ACC/AHA/SCAI对严重钙化病变的治疗建议
严重钙化病变会阻碍支架膨胀,血管腔内影像评估厚度>500μm或弧度>270°的钙化病变需要斑块修饰来辅助支架植入。斑块修饰方式包括RA、OA、准分子激光冠状动脉斑块消融术、切割球囊、球囊声波碎石术等。
指南推荐:对于有纤维化或严重钙化病变的患者,用RA修饰斑块可以提高手术成功率(2a,B-R);在有纤维化或严重钙化病变的患者中,可考虑通过OA、切割球囊、激光血管成形术或IVL来修饰斑块以提高手术成功率(2b,B-NR)。
RA 海外临床文献前线
1.ROTATE Multi-Center Registry:ROTA多中心注册临床研究
该多中心注册研究统计了2002年-2013年间接受RA和支架治疗的钙化病变患者,排除标准是STEMI、心原性休克和病变部位血栓,最终入选985例患者,包含1176个病变。终点事件是随访2年MACE发生率。

考虑到患者的严重程度和病变特征,分析院内MACE事件和中远期预后的随访结果,发现RA具有较高的手术成功率和可接受的短期和中期MACE发生率。
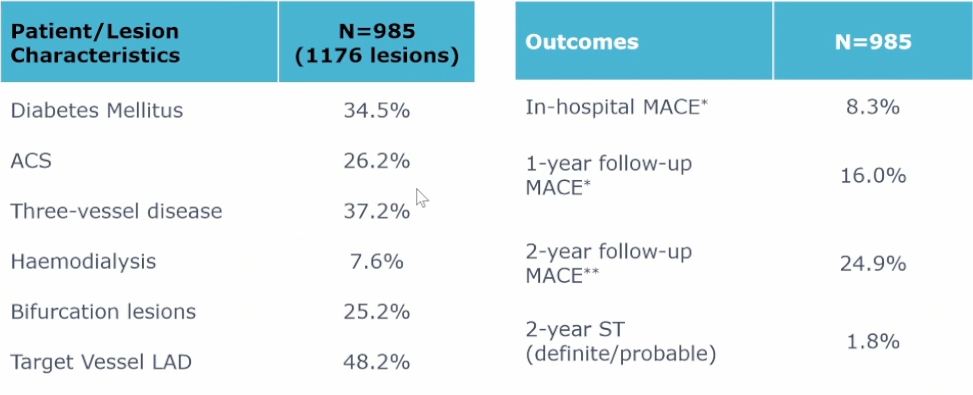
该研究还发现,治疗严重钙化斑块,计划性旋磨(主动旋磨)优于非计划性旋磨(被动旋磨)。
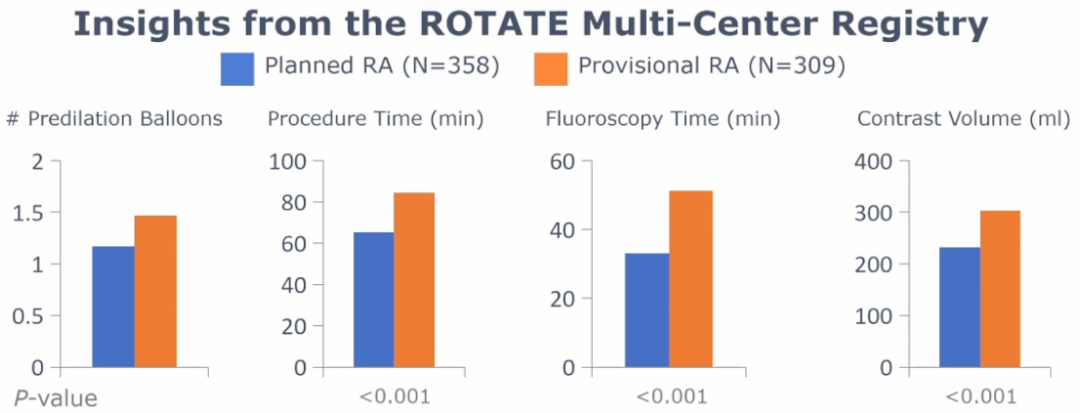
2.Shockwave vs. RA真实世界研究
这是一项针对亚洲人群IVL与RA的真实世界患者的临床结局研究。该新加坡、单中心、回顾性研究,分析了2017年-2020年间入选的53名IVL患者和271名RA患者的临床结局。主要终点是住院期间MACE和30天MACE【定义为全因死亡、心肌梗死(MI)、靶血管血运重建或卒中的复合终点】;次要终点是血管造影成功,术中穿孔或持续慢血流或无复流,支架血栓形成。
对于研究人群的说明:IVL组血管内影像显示严重钙化,定义为钙化>270°;血管造影显示严重钙化,器械不能穿过,或非顺应性球囊不能充分扩张。RA组主要是手术操作者认为有合适的重度钙化病变的旋磨标准适应证;排除年龄、性别或并发症缺失的病例。
研究结果(基线数据):与RA相比,IVL患者的急性冠脉综合征(56.6% vs 24.4%, p<0.001)、多支血管疾病(96.2% vs 73.3%,p<0.001)和急诊手术(17.0% vs 2.2%,p<0.001)的患病率更高。
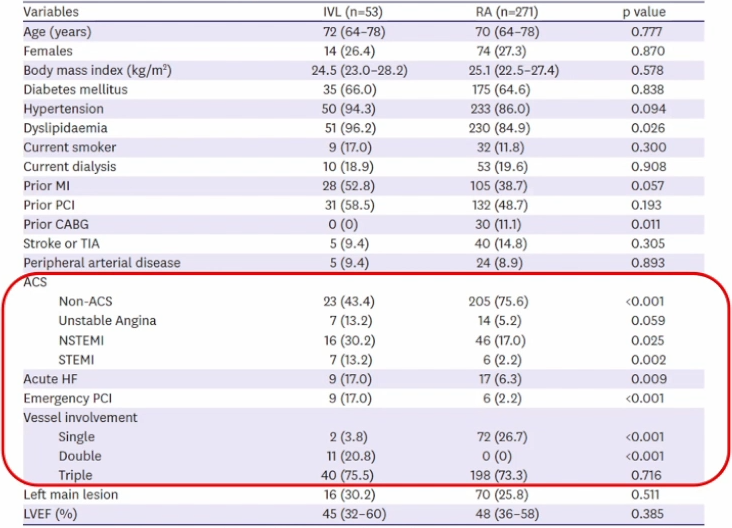
主要终点:与RA相比,IVL组住院期间MACE(11.3%vs5.9%,p=0.152)、MI(7.5% vs 3.3%p=0.152)和死亡率(5.7%vs 3.0%,p=0.319)均无统计学意义。IVL组30天MACE高于RA组(17.0%vs 7.4%,p=0.035)。

主要终点(倾向性评分):进行倾向评分调整回归,IVL组较RA组住院期间MACE(OR=1.677;95%CI,0.588-4.779),30天MACE(OR=1.910;95%CI,0.774 -4.718),没有达到统计学差异。
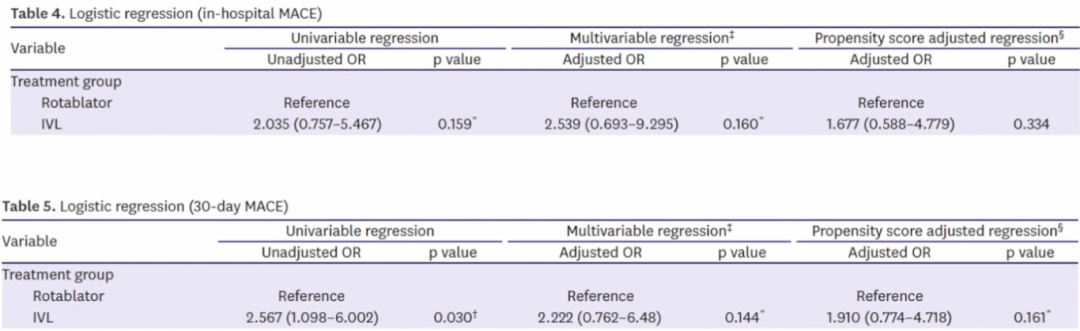
研究结论与限制说明:IVL组较RA组增加30天的MACE事件;倾向性评分回归分析显示IVL组较RA组增加院内和30天MACE的趋势。
本研究是单中心进行的小型、回顾性、非随机性研究。由于IVL组在常规治疗措施失败后作为辅助治疗,导致IVL组多血管病变、ACS、急诊PCI发生率较高。由于样本量小,我们最多可以对6个变量进行调整(年龄、性别、糖尿病、透析、出现ACS和LVEF)。所有这些因素都可能是导致IVL组MACE发生率高于预期的原因。
3.EuroPCR 2024:ROLLER COASTER研究
ROLLER COASTER试验是一项多中心、前瞻性、随机性临床试验,纳入171例经造影显示中重度钙化的患者,按1:1:1的比例随机分配至RA组、ELCA(准分子激光冠状动脉成形术)组和IVL组。术前、术中及术后即刻用OCT进行评价。主要终点是OCT测量的支架扩张百分比。采用意向性及非劣效性方法进行分析,以RA组作为参考。
纳入标准:年龄≥18岁;狭窄≥70%或血流储备分数<0.8/非高灌注指数<0.89;参考血管直径≥2.5且≤4 mm;冠脉造影显示中重度钙化;稳定型冠状动脉疾病或非ST段抬高型急性冠脉综合征。
造影特征:RA组、ELCA组和IVL组的组间造影特征也相似,冠脉造影显示重度钙化者占82.4%;OCT特征最大钙化厚度的均值为1.17(+0.24)mm,平均钙化长度为30.9(+12.9)mm,仅存在于浅表或深层部位的斑块较少(浅表9.6% vs.深层6% vs.两者均有 84.3%),其中42.7%的钙化位于血管分叉处,而7.4%位于主动脉口。
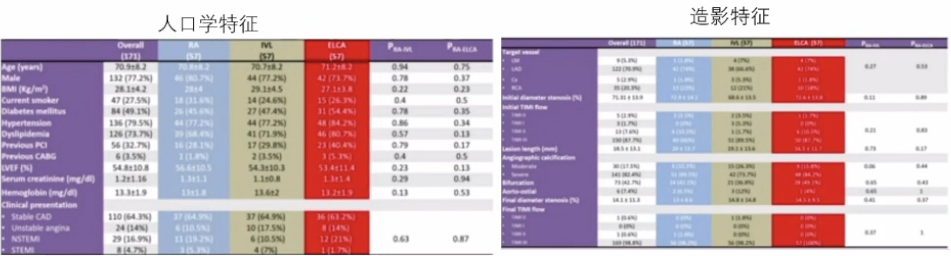
研究结果显示,RA组、IVL组和ELCA组设备成功率分别为89.5%,89.5%和86%,三组需行二次PMT的人数分别为6例、6例和8例。在22例需行二次PMT的患者中,分别有9例、7例和4例患者使用RA、IVL和ELCA治疗。最终成功率分别为5/9(5S.5%),5/7(71.4%)和3/4(75%)。
RA组、IVL组和ELCA组三组间的造影成功率、手术成功率和临床成功率相似。三组术后并发症发生率较低且组间差异无统计学意义。在总人群中,有4例患者(RA组和ELCA组分别2例)发生了严重术后并发症(如心血管死亡、围术期心肌梗死、支架血栓形成等),无死亡、非心血管死亡、支架内血栓形成及卒中发生。
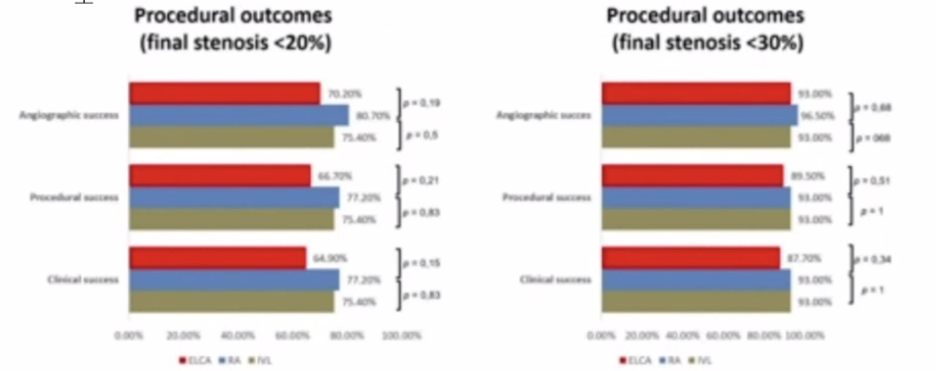
在意向性治疗分析中,与RA相比,IVL支架扩张百分比的均差达到了预定的非劣效性标准,而由于RA较高的支架扩张程度,ELCA组未达到预定的非劣效性标准。对最后一次斑块处理时使用的技术进行分析时,RA组和ELCA组之间的差异无统计学意义。
陈珏教授最后总结道,在严重钙化病变预处理流程中,若造影发现中重度钙化病变时,首先采用球囊尝试通过,若球囊可以通过就可以进行预处理。随后,借助腔内影像进行评估(OCT>IVUS),对于IVUS积分>2分,OCT积分>4分的情况,若属于深层钙化时建议选用振波球囊,若不属于深层钙化建议选用RA或OA;经旋磨处理后能得到满意的球囊扩张,则植入支架,若不能再采用振波球囊。对于钙化积分较低时,可以直接采用非顺应性球囊、切割球囊和积分球囊进行预处理,若球囊膨胀良好则植入支架,若球囊膨胀不全则选用振波球囊进行处理。对于球囊不能通过的患者,若微导管可以通过,首选RA或OA;若微导管不能通过,建议直接操作旋磨导丝,若旋磨导丝仍不能通过则选用激光;经上述处理后取得满意的球囊扩张,则植入支架,若不能再振波球囊进行处理。

专家简介
医谱app
扫码或者点击图片下载
微信公众号
扫码或点击图片关注
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、上载、下载、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。





发表留言
暂无留言
输入您的留言参与专家互动