European Heart Journal|ACS患者PCI后多支血管病变的冠状动脉旁路移植手术:为什么、针对谁、多早进行?
急性冠脉综合征(ACS)患者在经皮冠状动脉介入治疗(PCI)后出现多支血管病变(MVD)的情况并不少见,而冠状动脉旁路移植手术(CABG)作为一种可能的治疗选择,近年来在临床中被持续关注。近日,European Heart Journal发表了一篇题为“Coronary bypass surgery for multivessel disease after percutaneous coronary intervention in acute coronary syndromes: why, for whom, how early?”的文章,就ACS后混合血运重建的理想方法的基本原理、患者选择、最佳时机和辅助策略进行了详细讲述。医谱学术特此整理报道,以供临床参阅。

一、背景
ACS包括ST段抬高型心肌梗死、非ST段抬高型心肌梗死和不稳定型心绞痛,需要及时进行心肌血运重建,在大多数情况下通过对“罪犯病变”进行PCI来实现。然而,此类患者中有近50%存在MVD,即除了受罪犯病变影响的血管外,其他血管存在阻塞性冠状动脉斑块(直径狭窄>50%)。即使罪犯病变得到及时且成功的治疗,MVD仍与不良的长期预后相关。
在这种情况下,是仅治疗罪犯病变还是处理所有关键冠状动脉病变,这一问题已得到广泛回答。目前关于心肌血运重建的指南推荐对非罪犯病变进行“早期”血运重建,但完全性闭塞病变除外。但是对于立即进行、在同一次住院期间出院前进行,还是在另一次住院时进行,仍存在争议。
虽然完全血运重建的重要性似乎很明确,但当非罪犯病变为左主干(LM)或左前降支冠状动脉(LAD),或者存在包括LAD在内的MVD时,最佳的血运重建策略仍有待确定。实际上,所有关于完全血运重建的可用数据均来自基于PCI的试验,而CABG实现的血运重建完全性相关的结果从未得到评估。一方面,CABG可能提供慢性冠状动脉综合征中外科血运重建所证明的所有优势;另一方面,CABG带来了重大挑战,特别是在抗血栓治疗的管理、理想候选者的选择以及最佳时机的选择方面。
二、为什么要在PCI后进行CABG?
(1)在涉及LM或LAD的病例中,CABG在完成血运重建方面相较PCI具有显著优势(图1)。大型观察性SWEDEHEART登记处的最新成果,虽为非随机比较且存在一定局限性,但显示CABG与更低的病死率相关,且在调整多种混杂因素后主要不良心血管事件更少,这进一步证实了此前大量文献所指出的CABG在治疗LM病变方面优于PCI。
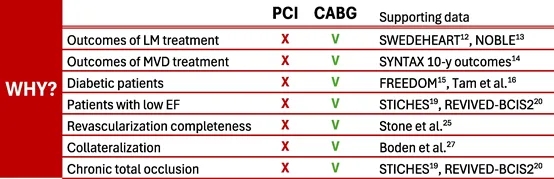
图1 ACS PCI罪犯病变后左主/LAD
完成血运重建的手术干预原理
(2)于糖尿病患者中,CABG的优势亦较为显著。FREEDOM试验表明,即便冠状动脉疾病严重程度相对较低,与PCI相比,CABG在8年时具有6%的生存优势。一项针对8602例接受CABG或PCI患者的倾向匹配研究显示,CABG相较于PCI具有显著的生存获益,且该优势在8年后持续增加。
(3)在左心室射血分数降低的患者中,CABG相较PCI同样具有优势。在缺血性心力衰竭的外科治疗(STICH)试验中,最初4.7年的随访结果呈中性,但有趋向于CABG降低病死率的趋势(CABG的风险比为0.86;95%CI,0.72~1.04;P=0.12)。在后来中位9.8年的随访(STICHES)中,证实了CABG相对于单纯药物治疗的生存获益(风险比为0.72;95%CI,0.64~0.82;P<0.001)。而在缺血性心室功能障碍的血运重建-英国心血管介入学会(REVIVED-BCIS2)试验中,情况并非如此(风险比为0.99;95%CI,0.78~1.27;P=0.96)。该试验纳入患者的左心室射血分数与STICH中纳入患者相对相似。需承认,REVIVED-BCIS2的随访时间(中位41个月)远短于STICH(58个月)和STICHES(118个月),且背景药物治疗有所改进,但与单纯药物治疗相比,REVIVED-BCIS2未呈现出生存获益的趋势,这与STICH首次报告中的情况相反。
(4)CABG在降低病死率方面优于单纯的指南指导下的药物治疗和PCI。其原因可由若干因素解释。其一,CABG实现完全血运重建的比率更高,此与更优的结果相关。其二,“外科侧支循环”理论可作为另一解释:PCI提供的是严格局部且以血流为重点的治疗,而CABG则能确保对PCI未处理且具较大动脉粥样硬化负担的冠状动脉节段并发症予以保护。
实际上,CABG不仅能预防单个限流性狭窄的并发症,还能防范可能于近端心外膜旁路血管中最终不稳定的病变所引发的并发症。
三、患者选择:针对哪些人?
PCI无疑是治疗ACS中罪犯病变的理想技术。然而,在特定情形下,罪犯病变治疗后采用PCI完成血运重建并非理想之选。此类情形涵盖存在复杂的LM疾病、MVD且残余SYNTAX评分>22、合并糖尿病、左心室射血分数降低以及存在慢性完全闭塞。具有中等到高度SYNTAX评分(>22)的复杂解剖结构,尤其是合并糖尿病时,应参照稳定型患者的状况,选择CABG来完成血运重建。存在存活心肌下的慢性完全闭塞,尽管存在争议,但对于PCI而言,这构成特殊挑战,因其治疗极度依赖操作者对病变血管进行顺行或逆行操作的能力,而此专业技能在诸多PCI中心可能并不具备。在此类病例中,罪犯病变经PCI治疗后,更适宜通过CABG来完成血运重建。
一旦评估此类MVD患者适合进行CABG,如何最佳地检测适合血运重建的病变成为了重要挑战。因为“解剖学”(主要依据管腔直径狭窄处理病变)或“功能性”完全血运重建(基于病变在最大血管扩张时诱导下游缺血或远端压力下降的能力,如分数血流储备<0.80或等效指标)的结果优势存在争议。指导多血管ST段抬高型心肌梗死血运重建的血流评估(FLOWER-MI)试验发现两者都没有优势。
鉴于PCI和外科血运重建对冠状动脉生理和血流动力学的影响不同,无法将功能性PCI研究的结果推广至CABG。此外,目前缺乏大型随机系列的数据支持任何一种选择。在最新的欧洲血运重建指南中,对ACS患者非罪犯病变的功能评估被列为Ⅱb类指征。研究表明,此时的功能评估可能因通常在ACS发作至少6~7天后才恢复的冠状动脉微循环功能障碍,而低估非罪犯病变的实际严重程度。因此,在决定通过经皮或外科途径解决残余病变之前,待急性梗死伴随的微血管功能障碍可能消退时,重复进行冠状动脉造影并进行功能评估,以更好地确定残余狭窄的严重程度和位置可能是合理的。
另一方面,体弱和手术风险高的患者(如通过EuroSCORE Ⅱ评估)可能从完全外科血运重建中获益较少,在此情况下,采用PCI完成似乎更可取。在SWEDEHEART注册研究中,与年轻患者相比,年龄大于70岁的患者接受CABG治疗在主要不良心血管事件方面的优势较小。CABG患者选择体人群包括:(1)低、中度手术风险患者;(2)LM病变患者;(3)具有中等复杂解剖结构的多血管疾病患者;(4)糖尿病患者;(5)慢性完全闭塞患者;(6)左心室射血分数降低的患者(图2)。
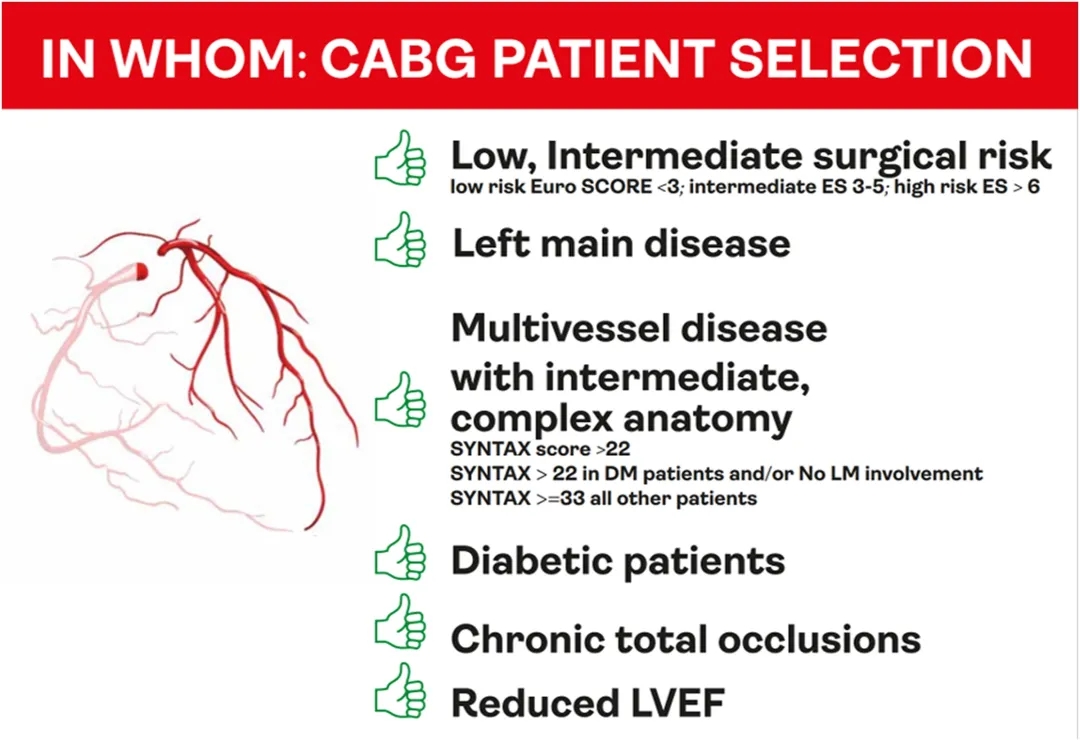
图2 支持LM/LAD血运重建完成CABG的患者特征
四、如果选择手术,最好的时机是什么?
两项试验显示,在患有MVD的ACS患者中,完全血运重建的益处与非罪犯病变的治疗时间无关,无论在同次住院、新住院期间还是首次PCI时。然而,一项针对54 148名患者的荟萃分析表明,在患有ACS和MVD的患者中,分期多支血管PCI患者的短期和长期病死率更低,且仅处理罪犯病变的PCI相较于立即处理所有病变的PCI病死率更低。最近的一项研究指出,急性缺血事件发生后1~7天的时间窗与较低的死亡率相关。但此结果不能完全适用于原发性PCI后的CABG。在COMPLETE和BIOVASC试验中,PCI完全血运重建的时机对结果无显著影响,且PCI立即完全血运重建对于全因死亡率、心肌梗死、计划外血运重建或脑血管事件的主要终点不劣于分期完全血运重建。
在分期CABG中,核心关注点在于缺血和出血风险的平衡。由于阿司匹林和P2Y12抑制剂双重抗血小板治疗(DAPT)常用于预防支架内血栓形成,所以在DAPT不间断的情况下进行手术并不被推荐。与术前至少5天停止DAPT的患者相比,手术当天仍保留氯吡格雷的患者,发生主要纵隔出血的风险翻倍,因出血而再次手术的风险显著增高,输血需求亦增加,且<5天组发生死亡、心肌梗死和中风复合结局的风险高出60%。在TRITON-TIMI 38与普拉格雷以及PLATO与替格瑞洛的研究中,也有类似发现。基于这些情况,当前一般建议在择期CABG前尽可能停用P2Y12抑制剂,其中替格瑞洛的停药间隔为3~5天,氯吡格雷为5天,普拉格雷为7天。
在处理ACS时,必须权衡血栓形成(例如支架内血栓)和新的动脉粥样硬化血栓形成的风险,与等待P2Y12抑制剂药效消退期间出血的风险。从临床角度出发,需要区分两种情形:对于不适合PCI的持续缺血患者,或者存在高危残余LM、近端LAD及涉及LAD的MVD患者,因其可能在未治疗区域发生新的ACS,应考虑在同次住院期间完成CABG;对于病情稳定或者支架内血栓形成风险高(例如接受长段、多个和/或分叉支架治疗,以及血小板活性高)的患者,应至少在首次PCI后30天进行晚期完成。对于早期治疗的患者,建议使用短效肠外血小板抑制剂坎格雷洛或替罗非班进行桥接治疗,以缩短DAPT停药时间间隔。
在PCI后早期选择CABG策略时,对于特定患者,非体外循环CABG、微创CABG和机器人辅助MIDCAB可作为传统CABG的替代方案。多项研究表明,在稳定患者中,相较于体外循环手术,这些方法能够减少输血、术后大出血和手术再次探查。在专家操作下,即使不中断DAPT,MIDCAB和RA-MIDCAB也可能降低罪犯病变PCI后早期进行CABG时失血的风险。

图 3 急性冠脉综合征经皮冠状动脉介入治疗后
手术干预完成左主/左前降支血运重建的手术时机
五、结论
当前证据在很大程度上支持ACS中对罪犯病变进行急性治疗后,对非罪犯MVD进行完全心肌血运重建。相较于PCI,CABG在实现血运重建完全性方面更具优势。因此,对于LM或近端LAD受累或包含LAD在内的MVD的情况,采用分阶段的PCI-CABG“杂交”血运重建(先PCI后CABG)治疗此类患者,可能兼具两种策略的长处。
在分阶段手术中,CABG面临主要问题。其一,与DAPT相关的较高手术出血风险,可能对预后不利;其二,DAPT中断易致支架内血栓形成。对于特定患者,即便不中断DAPT,采用非体外循环CABG、微创直接CABG(MIDCAB)和机器人辅助MIDCAB等替代策略,或可降低出血风险。
CABG的最佳实施时机尚不明晰。对于初次PCI治疗区域外存在持续心肌缺血、解剖结构不适宜PCI或具有高缺血风险临床特征(如伴有LM疾病的严重残余冠状动脉疾病或复杂MVD)的患者,早期CABG可能有益,此时可考虑用短效肠外血小板抑制剂桥接DAPT。而对于支架内血栓形成风险高(如近期植入长/窄/分叉支架)或血小板反应性高的患者,宜至少推迟1个月行CABG。此类决策应由多学科心脏团队依据患者特定的解剖和临床特征,并结合当地外科专业知识讨论决定。
欧洲ACS指南将ACS后的杂交冠状动脉血运重建(非LM/LAD狭窄行PCI及后续的CABG)列为适合患者的选择,然而目前缺乏随机对照试验的支持证据。规划此类试验虽合理,但因围手术期DAPT管理差异、冠状动脉解剖结构多变以及血运重建完成策略多样等因素,试验开展难度较大。在众多不确定性中,对于复杂冠状动脉疾病的ACS病例,考虑杂交血运重建选项意义重大。
医谱app
扫码或者点击图片下载
微信公众号
扫码或点击图片关注
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、上载、下载、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。



发表留言
暂无留言
输入您的留言参与专家互动