学术分享丨徐俊教授:阿尔茨海默病的诊疗新进展——代谢免疫机制与营养干预
首都医科大学附属北京天坛医院徐俊教授以“阿尔茨海默病的诊疗新进展--代谢免疫机制与营养干预”为题带来精彩学术报告。
一、AD的A-T-X-N新诊断框架
阿尔茨海默病(AD)的A-T-X-N新诊断框架,还包括“X”的其他变量,即血管性、免疫性、代谢性以及非神经元损害的系列疾病,这个概念也是一个演变的过程。2018年美国国家衰老研究院和阿尔茨海默病协会首次给出了生物学意义,也解释了这类疾病治疗困难的原因是因为早期诊断的时间窗太晚了。AD的A-T-N认为是在症状出现之前10年-20年的时间出现相应的症状。我国的指南在2020年针对已有的生物标志物给出推荐建议。

指南
2021年我国又针对AD源性轻度认知障碍诊疗给出共识建议,其中认为:
1.血浆Aβ42/Aβ40、P-tau217、P-tau181和NfL可用于AD源性MCI的早期诊断和疾病进展的评估(Ⅰ级推荐,A级证据)。
2.脑脊液Aβ42、Aβ42/Aβ40、P-tau181、P-tau217、T-tau、NfL可用于AD源性MCI的早期诊断及疾病进展的评估(Ⅰ级推荐,A级证据)。
3.ApoE基因型检测可用于MCI患者危险分层,预测其向 AD转化的风险,并可应用于临床研究中的疗效分析(Ⅱa级推荐,B级证据)。
针对AD血源性的推荐地位,国际社会给出不同建议。2021年《Lancet Neurol.》发表了《阿尔茨海默病的临床诊断:国际工作组的建议》文章,认为血浆生物标志物需要进一步标准化和验证,关于其中关键点罗列如下:
1.IWG:更新词汇,提出无症状阶段分类建议
2.与2018年NIA-AA诊断框架的ATN状态生物标志物定义AD接轨
3.A-T是诊断AD核心
4.生物标志物的异质性,缺乏确定的阳性阈值
5.PET检测的高成本和CSF测量的侵入性限制了临床广泛应用
6.需要AD表型阳性+AT阳性
7.血浆生物标志物需要进一步标准化和验证
8.A-T-X-N(共病)
经过四十年诊断标准的变迁,我们对于AD临床表现和生物标志物的特性有了长足的进步,越来越多的精神心理疾病都找到器质性的诊断依据。
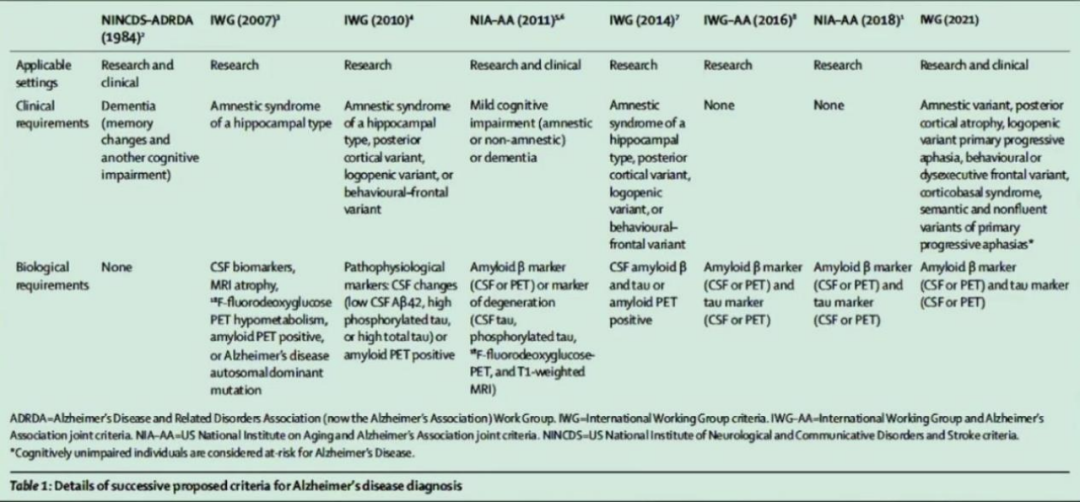
A-T-X-N新诊断框架
关于AD高危个体危险因素,建议如下:
1.AD有害因素:年龄增加;衰弱;女性;低教育水平;APOE ε4携带者;阿尔茨海默病家族史;颞叶顶叶血流量减少,葡萄糖代谢率减退;脑电图异常;MRI所见大脑新皮质联合区,特别是额、颞、顶区、整个海马等的脑萎缩;血管病危险因素等。
2.AD保护性因素:包含保护基因,如APOE ε2全表型,APOE ε3教堂性突变,或APP冰岛型的A673T突变,把Aβ病理性酶切的病变部位突变掉,从而起到保护基因的作用。此外,还包含较高的认知储备。
3.待确认的因素:神经炎症的类型;脑功能的认知储备(可以在MRI功能影像学上表现);以及生活方式因素如体育活动,睡眠,社交活动;精神疾病尤其是抑郁的状态疾病转归的可能性。
ATN指导的AD临床诊断:

ATN指导的AD危险分层:
1.最高危险人群:常染色体显性突变携带者(APP,PSEN1,PSEN2或21三体综合征)
2.高危人群:认知正常的伴有CSF或PET提示Aβ和tau蛋白阳性的;PET提示边缘系统外皮层tau阳性(Beaak5期或更高);APOE ε4纯合子。
3.风险未确定人群:Aβ阳性和tau蛋白阴性或未知;Aβ阴性和tau蛋白阳性。
2021年底国际专家针对AD血源生物标志物的价值,发表名为《阿尔茨海默病的基于血液的生物标志物:走向临床实施》的文章,认为AD血源生物标志物未来会带来AD的临床诊疗重塑。
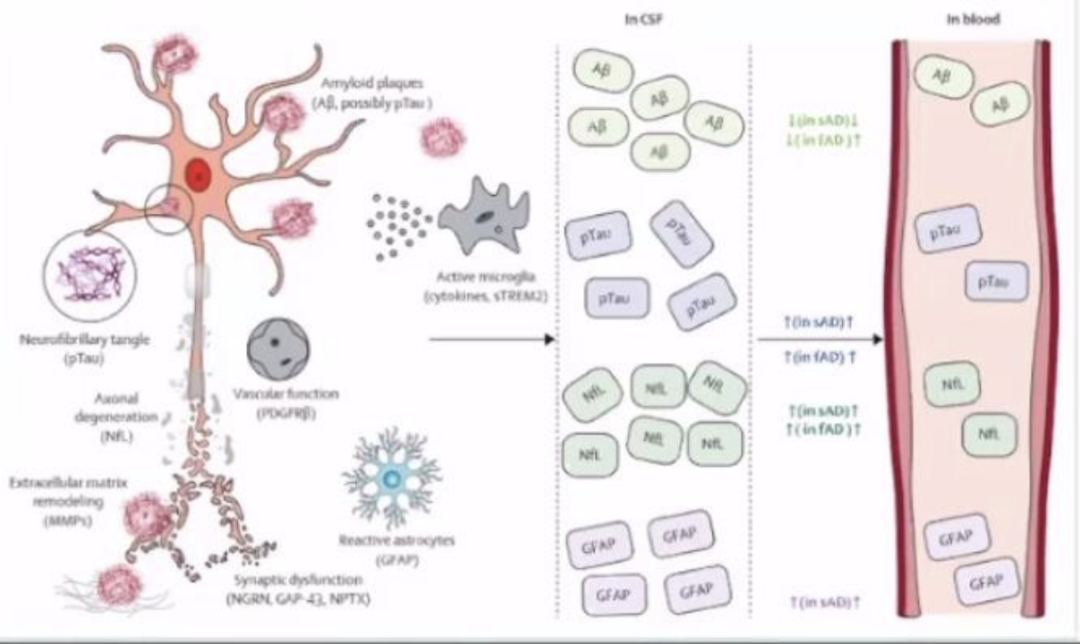
示意图
该研究认为多年来,基于血液的AD生物标志物似乎无法实现,但最近的结果表明它们可能成为现实。新的高灵敏度分析产生的令人信服的数据已经出现,在不同的队列中具有显著的一致性,但也独立于所使用的精确分析方法。血液中Aβ蛋白和磷酸化 tau 蛋白的浓度与脑脊液中的相应浓度以及Aβ蛋白-PET 或 tau-PET 扫描相关。此外,其他基于血液的神经变性生物标志物,例如神经丝轻链和胶质纤维酸性蛋白,似乎可以提供有关疾病进展和监测治疗效果的潜力的信息。那我们何时以及如何将这些生物标志物用于临床实践,是我们值得关注的问题。
以下给出了血液生物标志物在临床试验设计中的不同应用:针对纳入标准,增加诊断准确性二级指标,引导或提示药物治疗的标准以及评估临床预后的应用范围。
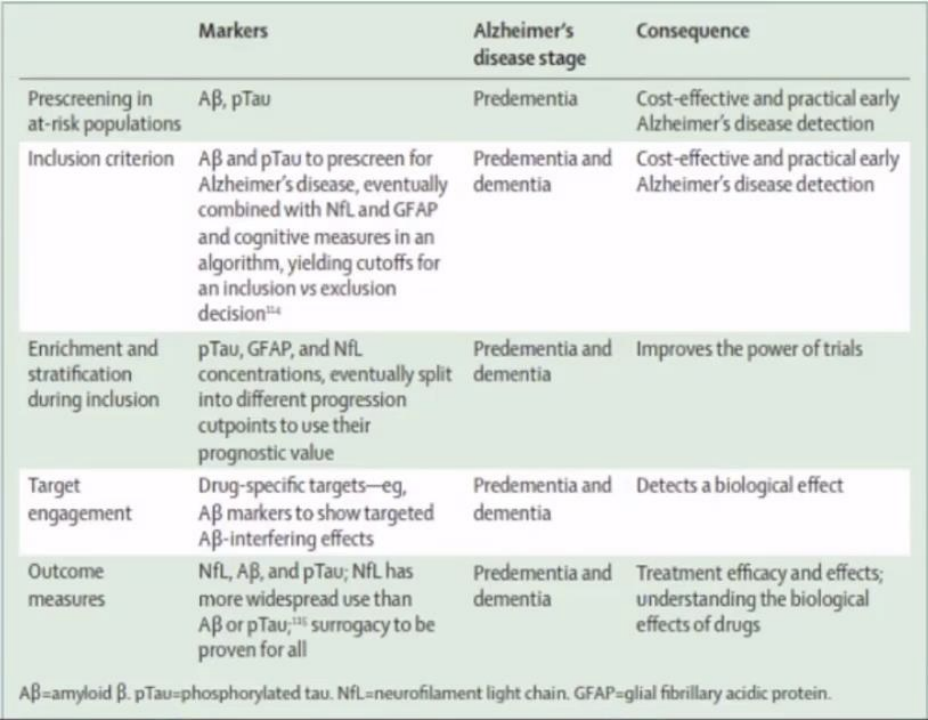
临床试验不同应用
除了上述的,还出现了AD的新诊断思路,其中意大利关于AD早期诊断抗体AlzoSure Predict专利已在中国获授权。

AD的新诊断思路
二、如何重塑Aβ蛋白作用机制
Aβ蛋白可能扮演了抗菌肽的作用,从下图可以看出肺炎衣原体可以经鼻入脑,感染能够影响AD相关基因表达,特别是与蛋白质折叠有关的一些基因表达下调,将导致错误折叠的蛋白聚集,也就是抵抗外来病原体,快速反应错误,自身被感染。

Aβ蛋白抗菌肽作用
《Nat Med.》有篇文章研究小胶质细胞激活和 tau 在 Braak 阶段共同传播,发现Aβ增强小胶质细胞炎症,促进Tau扩散。该研究通过正电子发射断层扫描脑成像研究了 130 名跨越衰老和 AD 临床谱的个体,用于小胶质细胞激活 、Aβ和 tau 病理,进一步评估了骨髓细胞 2 (TREM2) 脑脊液 (CSF) 浓度和脑基因表达模式上表达的小胶质细胞触发受体。发现PBR28 与 CSF 可溶性 TREM2 相关,并显示出类似于 TREM2 基因表达的区域分布。网络分析显示,在 Braak 样阶段之后,小胶质细胞激活和 tau 相互分层相关。回归分析表明,纵向 tau 传播途径取决于基线小胶质细胞网络,而不是 tau 网络。Aβ、tau 和小胶质细胞异常的共同发生是研究人群中认知障碍的最强预测因子。该研究结果支持一个模型,其中 Aβ 和活化的小胶质细胞之间的相互作用决定了 tau 在 Braak 阶段的传播速度。
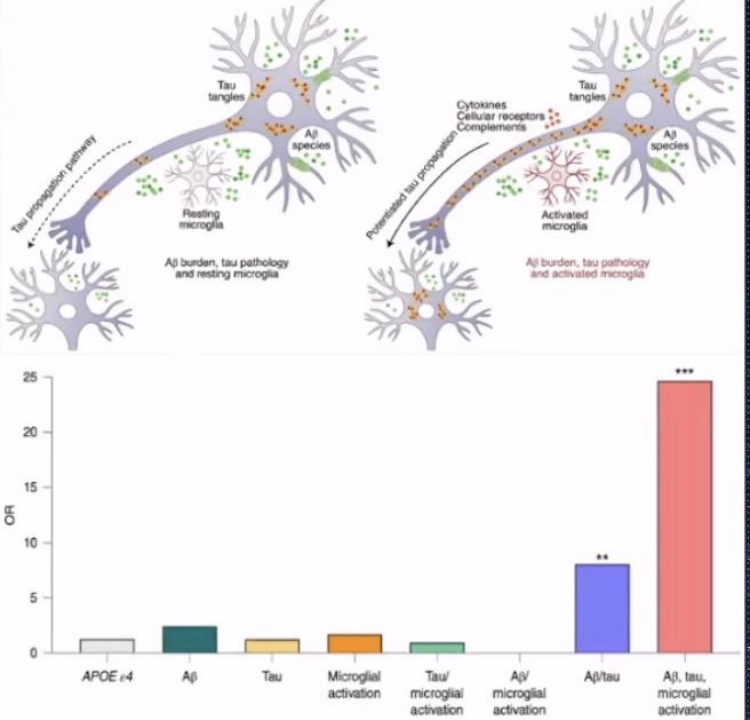
小胶质细胞激活、Aβ和 tau 病理作用机制
对于Aβ直接靶向的相关疫苗的研究也是屡战屡败,2020年在《老年痴呆症》的《阿尔茨海默病预防倡议 (API) 常染色体显性阿尔茨海默病哥伦比亚试验的基线人口统计学、临床和认知特征》这篇研究中,共纳入 252 人,并提供了按年龄范围匹配的总共 242 名突变携带者和非携带者的数据,不包括 10 名参与者的数据,以保护参与者的机密性、遗传状况和试验完整性。研究总结了 30 至 53 岁的 167 名突变携带者和 75 名非携带者的人口统计、临床、认知和行为数据。携带者明显比非携带者年轻,迷你精神状态检查 (MMSE) 得分明显较低,并且记忆力一直较低分数。
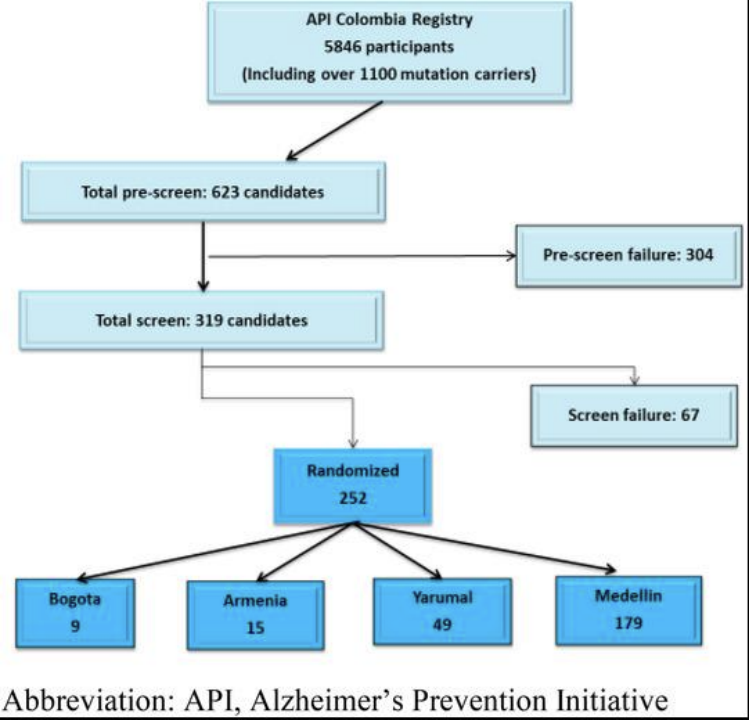
API流程图
但是美国国立卫生研究院衰老研究所(NIA)官方发言,其关于crenezumab试验结果的声明表示:抗Aβ药物对遗传性阿尔茨海默病患者没有显示统计学上显著的临床益处。可以说再次打击了Aβ疫苗的研发。
三、微生物对大脑的影响
当然,扩大视角来看AD不只是局限于大脑的疾病,2021年国际知名《Cell》杂志(IF=41.6)发表了一篇关于微生物对宿主生理的影响的文章,该研究来自于犹他大学医学院微生物与免疫学学系病理学系的Hill JH的团队,阐述了微生物作用于机体的机制、代谢产物。机制包括屏障功能、免疫调节、定植抵抗、发育等;主要代谢产物包括:外膜组分(肽聚糖、脂多糖等),代谢产物(短链脂肪酸等),新型产物。
从系统生物学角度来看,微生物作用于机体的机制包括屏障功能、免疫调节、定植抵抗和发育等,并且体内微生物群对神经、内分泌、皮肤、免疫和心血管系统具有多种调节机制。
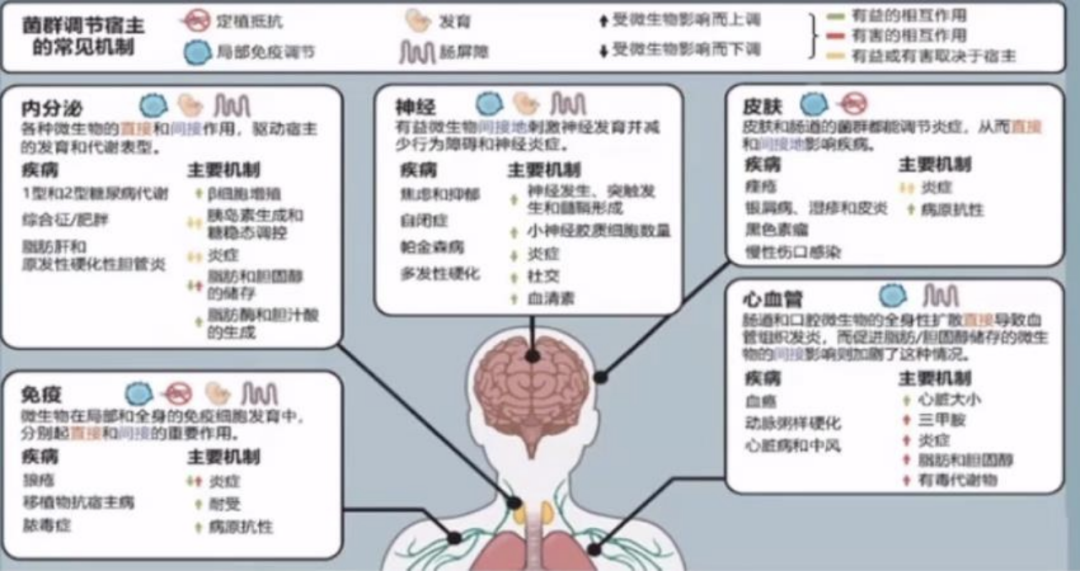
微生物群作用机制
同样微生物群对呼吸、消化道、骨骼肌肉和泌尿生殖系统的也有相应的影响,起到调节作用。
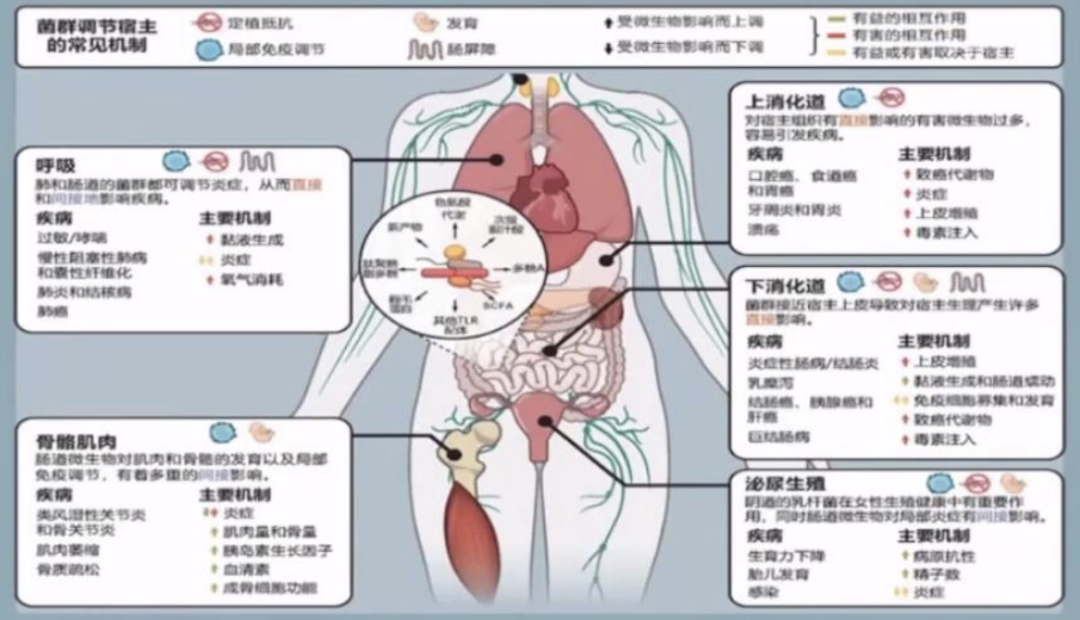
微生物群作用机制
《Cell》的另一篇是关于《微生物-肠-脑轴》的研究(IF=41.6),该研究来自于加州大学洛杉矶分校综合生物与生理学系Gulistan Agirman团队,阐述了微生物参与调控神经元的产生、分化、成熟,以及大脑免疫、血脑屏障通透性、大脑。结构和神经回路的全过程,影响机体的行为和(或)大脑功能。该研究发现随着大脑不断发育,肠道微生物组随之变化。
肠道菌群对大脑发育的影响体现在:宿主体内微生物在母体时具有较高的多样性,到了新生儿期,菌群多样性降低,随着后天饮食、与环境接触等影响,宿主可再次获得高多样性的肠道菌群;菌群参与调控神经元的产生、分化、突触形成及成熟,以及小胶质细胞的发育、成熟,免疫功能的完善。
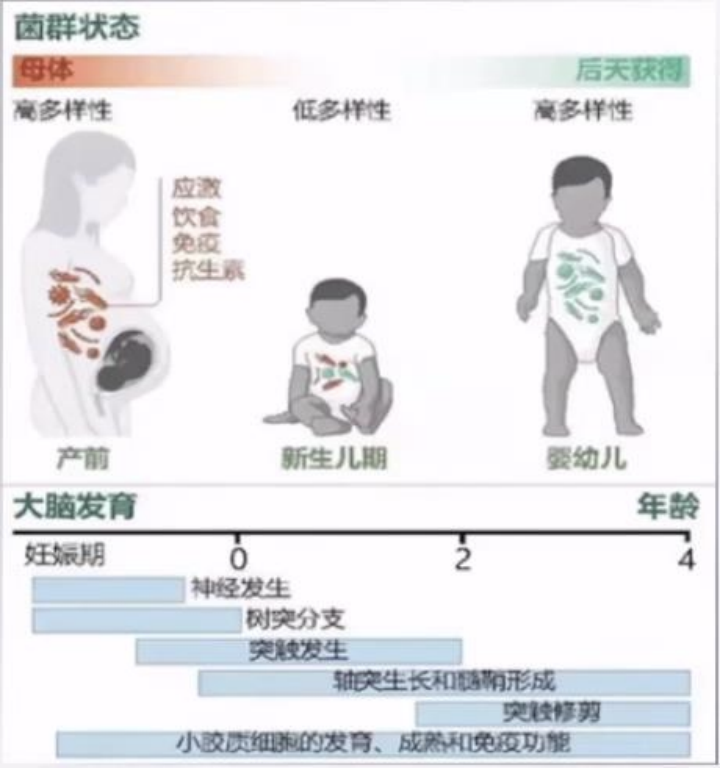
肠道菌群对大脑发育的影响
而且肠道菌群对大脑发育和功能非常重要。微生物参与宿主大脑发育、大脑结构、血脑屏障、大脑免疫、神经发生、神经信号传导、神经稳态、行为与认知等多方面的调控。此外,神经元的产生、分化、成熟,轴突形成、分化,髓鞘生成及成熟,神经免疫与血脑屏障依赖于微生物的参与。

肠道菌群通过多种机制与大脑主动交流:在免疫系统方面,微生物作用于肠道后,通过树突状细胞、巨噬细胞、B细胞、CD4+ T细胞激活细胞免疫及体液免疫,并作用于大脑中的小胶质细胞,调节大脑免疫系统;在内分泌/系统性方面,通过肠嗜铬细胞分泌胰高血糖素样肽1(GLP-1)及肽YY(PYY),肠内分泌细胞分泌5-HT,调节下丘脑垂体肾上腺素轴,内分泌轴也可通过此方式反馈调节肠道内分泌;在神经系统则通过肠神经元、经迷走神经通路调节神经系统,神经系统通过脊椎通路反馈调节肠道神经。

肠道菌群通过多种机制与大脑主动交流
综上所述,肠道菌群通过多种途径调节肠-脑轴。包含神经活性途径,如神经递质、神经活性代谢物;免疫途径,如细胞因子;短链脂肪酸和微生物代谢物;神经途径,如迷走神经、肠神经系统和脊神经;下丘脑垂体肾上腺轴;以及内分泌途径。
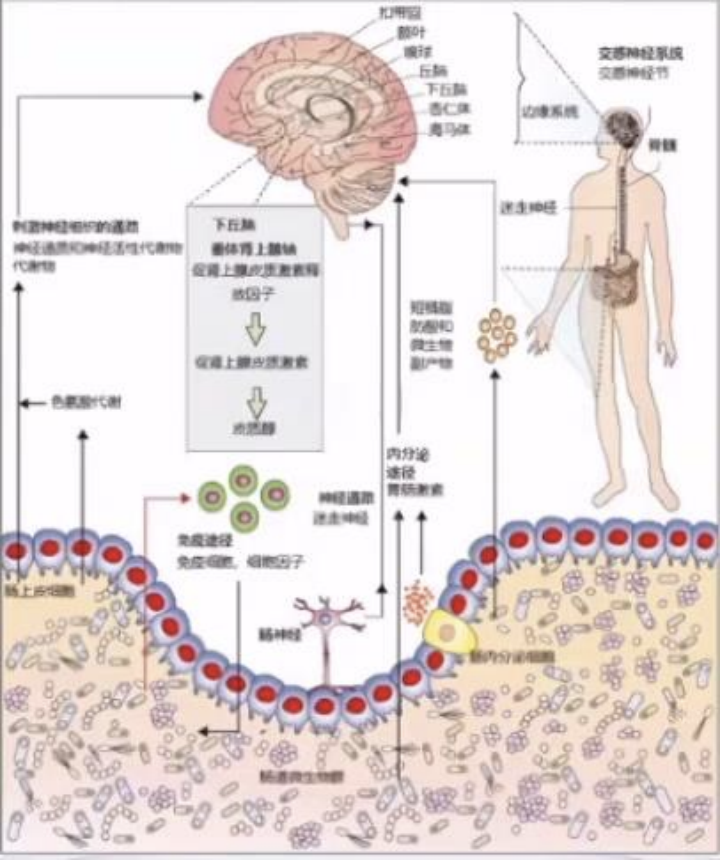
微生物群和大脑之间的沟通途径
研究人类微生物组的潜在方法如下:
1.患者与对照的差异:评估来自患者和对照组的微生物群,并确定多样性差异和功能代谢的差异。
2.三种潜在研究方法:
(1)动物研究探索机制
移植人类的粪便微生物给啮齿动物的肠道,进行人化处理。进行动物行为测试、分子和成像技术功能分析
(2)粪便移植
(3)饮食干预
通过选择性饮食、益生元或益生菌来针对微生物组。
关于轻度认知功能障碍(MCI)受试者的肠道菌群,饮食和AD标志物的相互作用,一篇文章也作了相应分析。该研究来自于美国维克森林生物技术中心微生物与免疫学系,内科-分子医学系的Hariom Yadav博士,与美国维克森林医学院J·保罗·斯蒂克特老年医学中心的Suzanne Craft博士,于2020年7月发表于国际知名杂志《EBioMedicine》上,最终探寻MCI患者肠道真菌与CSF中的AD标志物特点,膳食对肠道真菌、AD标志物的影响。
该研究为一项单中心、随机、双盲、交叉研究,研究设计如下:

研究设计
研究结果发现,MCI和认知正常受试者之间的肠道真菌群确实存在差异。从下图中可以看到MCI患者的a多样性降低(b);MCI患者了囊菌门所占比例较低,担子菌门所占比例较高(c);主要真菌属水平上的分析显示,MCI与CN的真菌群落组成明显不同(d);MCI患者葡萄孢属、核盘菌科、法夫酵母科、发菌科和哈萨克斯坦酵母、寄生性子囊菌属、囊藻科、枝泡菌属、托尼尼亚科的比例较高,而枝孢菌科和迈耶尔属所占比例较低(e)。

临床诊断为MCI何认知正常受试者之间的肠道菌群差异
此外,不同饮食诱导MCI与认知正常个体的肠道真菌群发生变化。
1.两组饮食干预对真菌β多样性无显著影响;改良的地中海生酮饮食(MMKD)干预对真菌群落的调节更明显(a,c)
2.MMKD干预不会导致认知正常受试者的真菌群α-多样性变化,但会导致MCI患者的的α-多样性显著变化(b);美国心脏协会饮食(AHAD)干预增加了认知正常和MCI受试者的α-多样性(d)。
3.MMKD对真菌门、科和属水平的的调节更显著(e,f,g)。

MMKD和AHAD对患有或
不患有MCI的患者的肠道真菌群组成有不同的调节
MCI和认知正常的个体中,饮食引起的真菌群变化与CSF中AD生物标志物的变化相关。
1.真菌属(包括德巴利氏酵母属、帚枝霉属、黑粉菌属、念珠菌属和枝孢属)与CSF中不同的AD标志物呈正相关或负相关(a)
2.认知正常与MCI受试者之间以及饮食干预之间存在特定的相关模式(b)
(1)MMKD:曲霉属和枝孢属在基线MCI患者中较高,在干预期间与p-tau呈负相关。枝顶抱属也显示出类似的变化趋势。
(2)AHAD:黑粉菌属和帚枝霉属与Aβ-40呈正相关;德巴利酵母菌和Dilutina属分别与Aβ-40呈正相关和负相关;霉菌属与p-tau呈正相关。
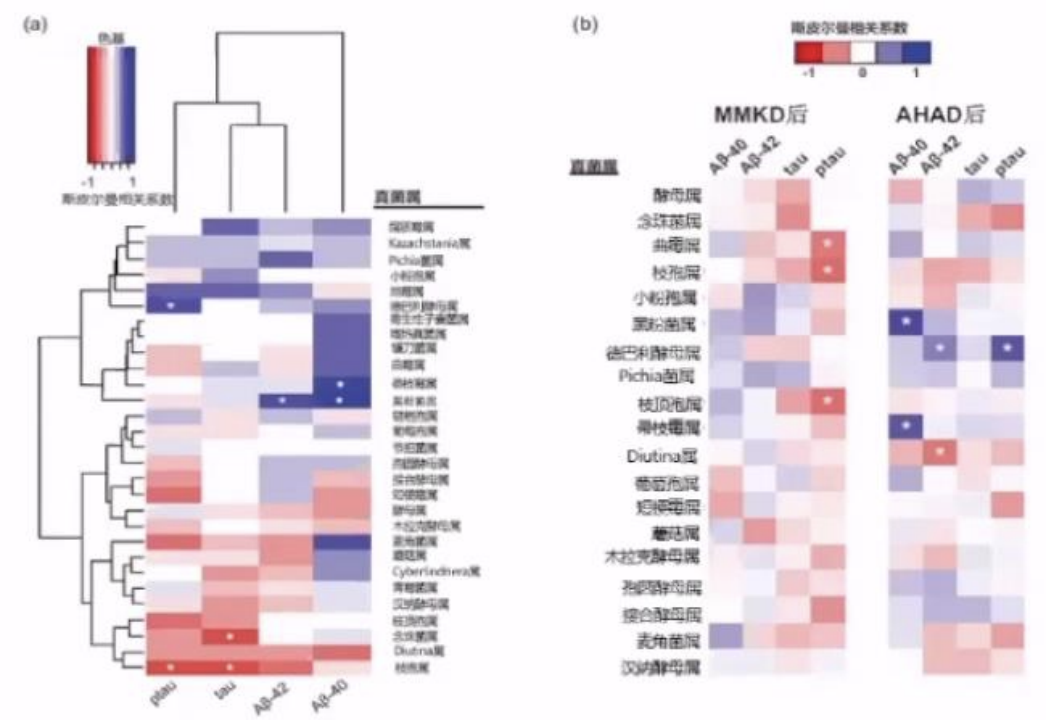
饮食引起的肠道真菌群变化与MCI
和CN受试者的CSF中AD生物标志物的变化有关
文章最后给出结论如下:
1.与认知正常相比,MCI受试者中的核盘菌科、法夫酵母科、发菌科、囊藻科、带形壳菌科和贵腐菌、哈萨克斯坦酵母、Phaeoacremonium和枝孢属的比例较高,季也蒙念珠菌丰度较低。
2.MCI受试者中的特定直菌类群与AD标记物以及肠道细菌间具有明显的相关阵列。
3.MMKD对MCI受试者的真菌多样性产生了更广泛的影响,增加了蘑菇属和木拉克酵母属,在有或没有MCI的受试者中酿酒酵母和麦角菌属下降程度不同。
当然,我国关于微生物的研究也有报道,在《卒中后认知障碍与肠道微生物及其代谢产物的相关性》文章中,探讨了卒中后认知功能障碍(PSCI)与肠道菌群的关系。
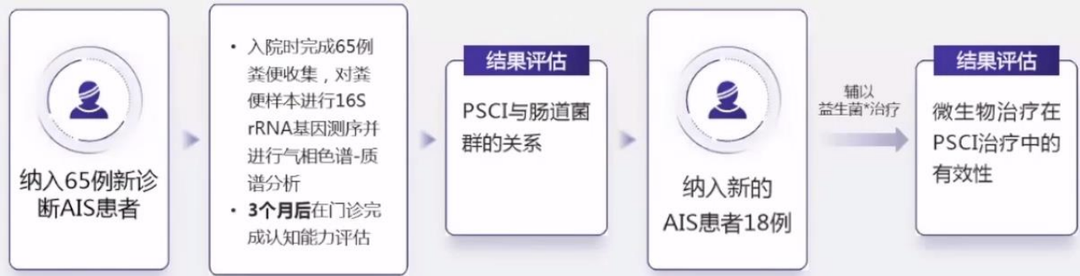
研究设计
研究发现与非PSCI相比,PSCI患者肠道微生物组成改变,α多样性降低。
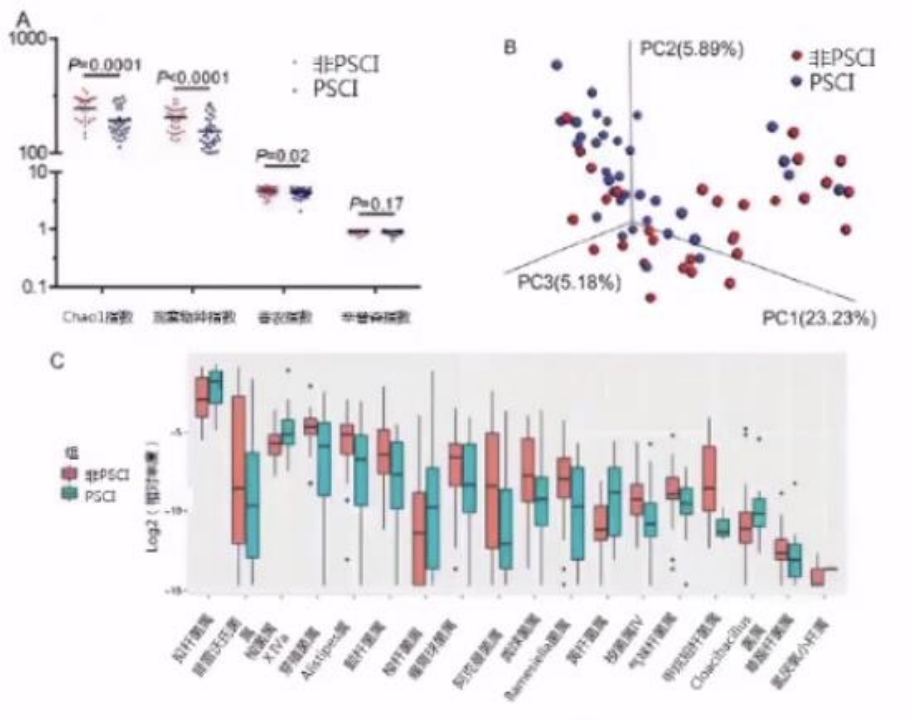
有或没有PSCI患者之间微生物群的负担显著不同
研究最后得出结论如下:
1.与非PSCI患者相比,PSCI患者的特点是α多样性减少,微生物组成及相应代谢物改变。
2.梭杆菌增多和微生物代谢的短链脂肪酸缺乏与PSCI显著相关。
3.基于肠道微生物群和SCFA的模型可以准确地预测脑卒中发作后3个月或更长时间的PSCI。
4.虽然传统的益生菌给药对PSCI的影响不大,但可以改善患者的情绪,包括卒中后3个月的抑郁和焦虑。
肠道菌群失调与AD关键病理机制密切相关,它通过增加淀粉样斑块形成、神经炎症、SG和胰岛素抵抗,从而促进AD病理的进展。

肠道菌群失调与AD关键病理机制密切相关
四、2021阿尔茨海默病脑健康营养干预专家共识
此外,鉴于脑肠轴新证据,抗生素对雄性AD鼠+的作用,促进了我国《2021阿尔茨海默病脑健康营养干预专家共识》的推进,该共识在CSPEN成立脑健康营养协作组的基础上,响应了“健康老龄化,预防脑衰老,保持脑健康”的战略需求,提高了临床对AD脑健康营养干预理念的认知。
1.该指南建议采用营养不良三级诊断方法(I级证据,A级推荐),首先,利用营养风险筛查工具选出高营养不良风险者;其次,对这类患者进行营养评估,以明确营养不良的类型与原因;最后,做出营养不良的诊断及严重程度分级,为下一步制定营养治疗计划提供依据。
2.推荐建议对60岁及以上老年人群、认知障碍科门诊及病房首次就诊患者进行常规营养风险筛查(Ⅱ级证据,A级推荐)。
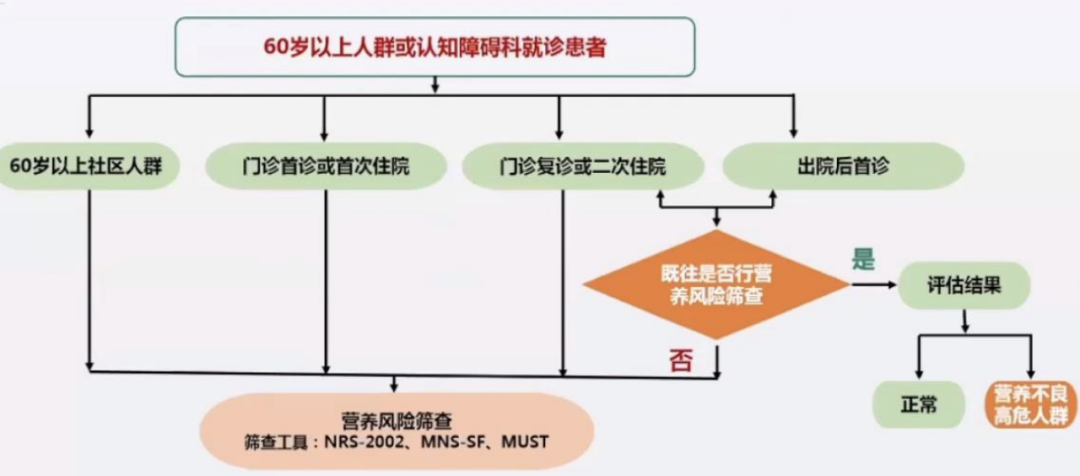
AD患者的营养风险筛查流程
4.对于营养风险筛查工具的选择,推荐使用MNA和MNA-SF进行营养风险筛查和营养评估(Ⅱ级证据,A级推荐)。

营养风险筛查工具的选择
5.AD患者的营养风险评估流程,推荐建议经营养风险筛查提示为高营养不良风险人群需要进一步完善营养评估(Ⅱ级证据,A级推荐)。
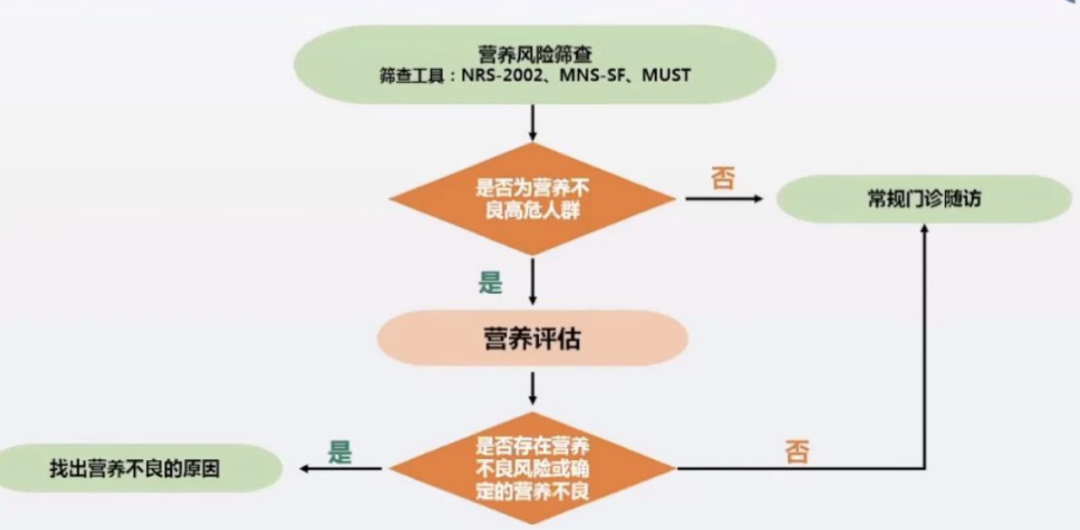
AD患者的营养风险评估流程
6.AD营养风险评估内容和工具如下:

7.AD营养管理总体原则。
基于上述营养评估和诊断结果,多学科医生、护理人员以及照料者需要制定以患者为中心全面、合理的营养治疗方案。营养治疗方案应具备可以合理解释、提供疗效建议以及再评估的能力,即营养管理计划。
推荐建议根据营养不良三级诊断结果制定以患者为中心、满足患者和照料者双重需求的营养管理计划,包括营养治疗方案及对其监测、评价和记录,以便随时调整营养方案;同时加强对照料者营养护理的教育和培训(I级证据,B级推荐)。
8.AD营养管理计划要点
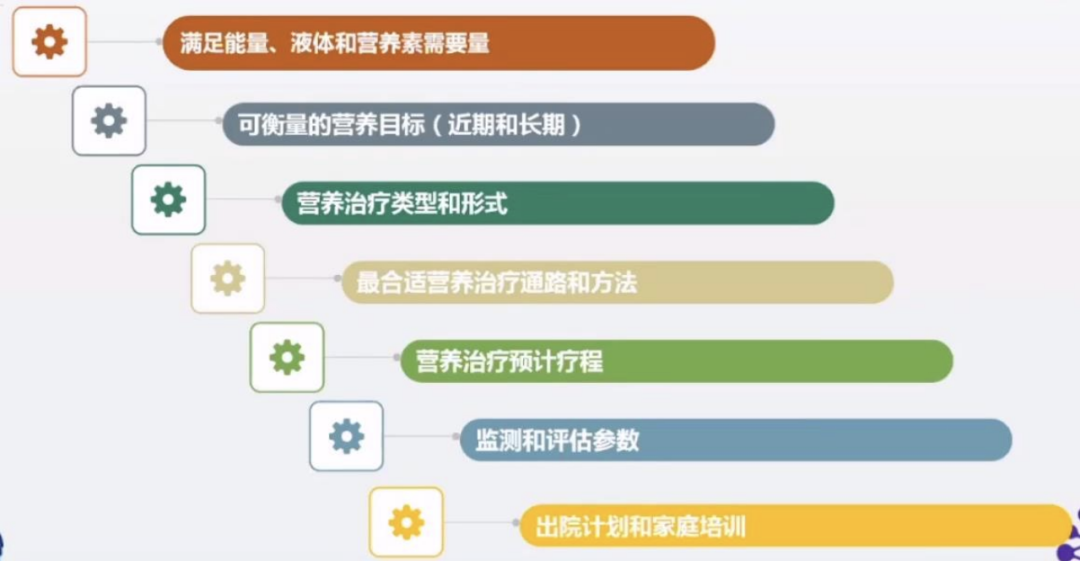
9.AD营养不良管理五阶梯原则
当下一阶梯不能满足60%目标能量需求3-5天时,应该选择上一阶梯。

10.AD患者不同阶段的营养支持
对于AD患者而言,还应该结合疾病特点,在疾病不同阶段寻找营养不良的原因,给予相应的营养干预措施。这些干预措施一方面应弥补现有的营养不良,同时应尽可能促进患者日常生活独立。

11.对AD照料者的持续教育与培训
适宜的照料管理模式不仅可以延缓痴呆患者病情进展,改善其生活质量,还可以减轻照料者负担。对照料者或护理人员进行培训和知识教育,可能会对痴呆患者的营养行为和进食能力产生积极影响。
12.营养治疗监测与评价

13.MIND饮食可额外减缓衰老相关认知功能下降
高度坚持MeDi、DASH和MIND这三种膳食模式均可以降低AD发病风险,但中度坚持MIND也可以降低AD发病风险达35%;并且MIND还可以显著减缓衰老相关认知功能下降。

《中国居民膳食指南科学研究报告(2021版)》提出中国居民应遵循“五谷为养,五畜为益,五菜为充,五果为助”的平衡膳食原则,也更适合国人的平衡膳食原则。

14.记录与随访
营养管理计划记录至医学电子病例,每1-3个月随访,评估疗效与转归,合理调整治疗方案。
综上所述,该共识建议AD是四级预防,要跳出固有思维陷阱,在营养干预方面要及早识别,全面管理,全程获益;其他干预方面要重视运动体脑,心态调适,科学睡眠。
五、脑健康AD相关
1.脑健康认知障碍早期预警的目的是早期干预,早期管理以及早期筛查。
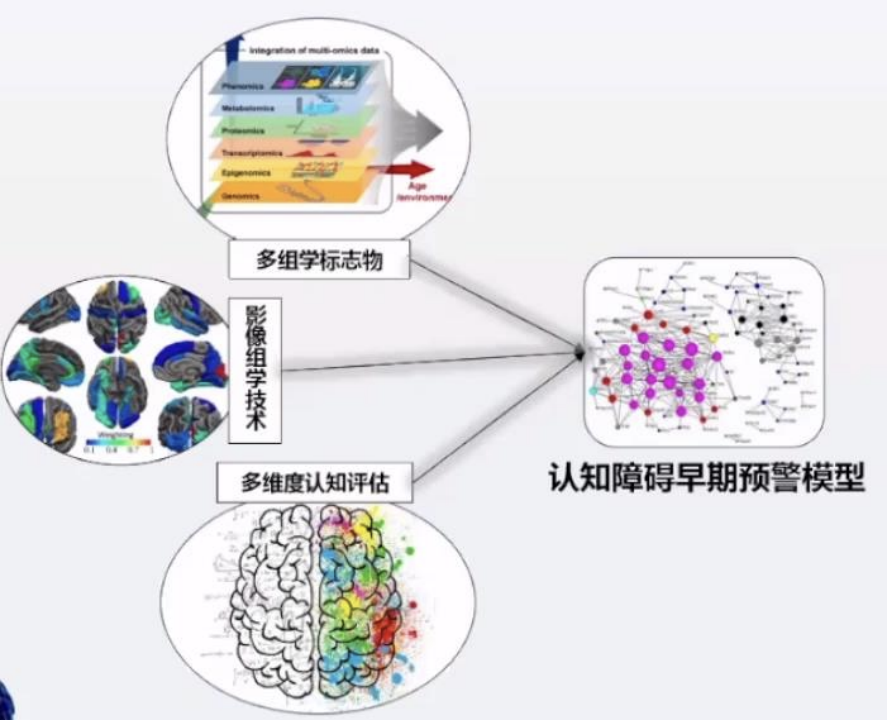
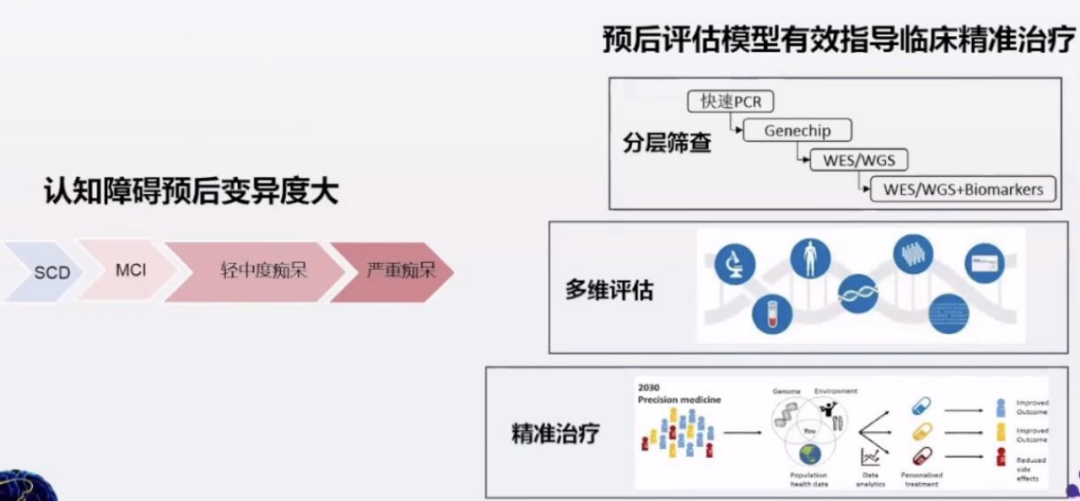
2.脑健康认知障碍预后评估体系
3.脑健康相关诊疗标准

此外,还有一些新疗法,例如Alnylam ALN-APP RNAi,干细胞,纳米材料,抗衰老等。新疗法可以清除大脑衰老干细胞,可增强神经发生和认知功能。

