EHJ | 中山大学附属第一医院王礼春教授团队:一例高危心肌病患者联合经心尖经导管主动脉瓣置换术与室性早搏消融术病例报告
瓣膜性心脏病与室性心律失常是晚期心肌病患者常见的共病,二者往往会协同促进心力衰竭的进展。重度主动脉瓣反流会引起慢性容量负荷过重,导致左心室扩张和功能受损,而频发室性早搏则会加剧机械不同步和心律失常驱动的心脏重构。
当前临床实践中多采用分阶段干预策略,但单独处理任一病变可能难以全面应对复杂的病理生理机制。经导管主动脉瓣置换术为高风险患者提供了微创治疗选择,室性早搏消融则可解决难治性心律失常问题,但分次手术会增加风险并延长康复时间。

近期,中山大学附属第一医院心血管内科王礼春教授作团队发表在《欧洲心脏杂志》(European Heart Journal)上的一篇病例,报道了一种经心尖联合介入术式,通过单一穿刺路径,同步实施经导管主动脉瓣经心尖置换术与左心室起源的室性早搏消融,从而同时矫正瓣膜功能障碍并消除心律失常触发灶。这种整合结构与电生理治疗的策略,可打破容量超负荷与心律失常性心肌病之间的恶性循环,为高风险患者提供个体化解决方案。
核心要点:
·对于高危心肌病患者,采用经心尖联合治疗方案处理重度主动脉瓣反流与室性心律失常具有可行性;该术式通过同期消除容量负荷与心律失常触发灶,可加速心脏逆重构。
·针对原发性主动脉瓣反流和心室早搏的靶向矫正,或可在不直接干预二尖瓣的情况下促使继发性二尖瓣反流消退,这凸显了在复杂多瓣膜修复术前处理潜在心室驱动因素的重要性。
病例介绍
患者67岁,男性,因反复胸闷、气促入院。其患有慢性心力衰竭(NYHA评分IV级)、扩张型心肌病及重度主动脉瓣/二尖瓣反流病史4年。既往曾接受 ICD/CCM 植入术,并接受规范药物治疗(包括β受体阻滞剂、ARNI、盐皮质激素受体拮抗剂及利尿剂)。
心电图提示,左心室起源的单源性室性早搏二联律(图1)。动态心电图显示室性早搏负荷达37.8%,以单源性为主,伴室性二联律/三联律及短阵非持续性室性心动过速。超声心动图证实左心室及左心房严重扩大(左心室舒张末期内径83mm,左心房内径53mm),左心室射血分数降低(35%),重度主动脉瓣反流(反流口面积6.3mm²)和中重度二尖瓣反流(反流面积27.3cm²)。
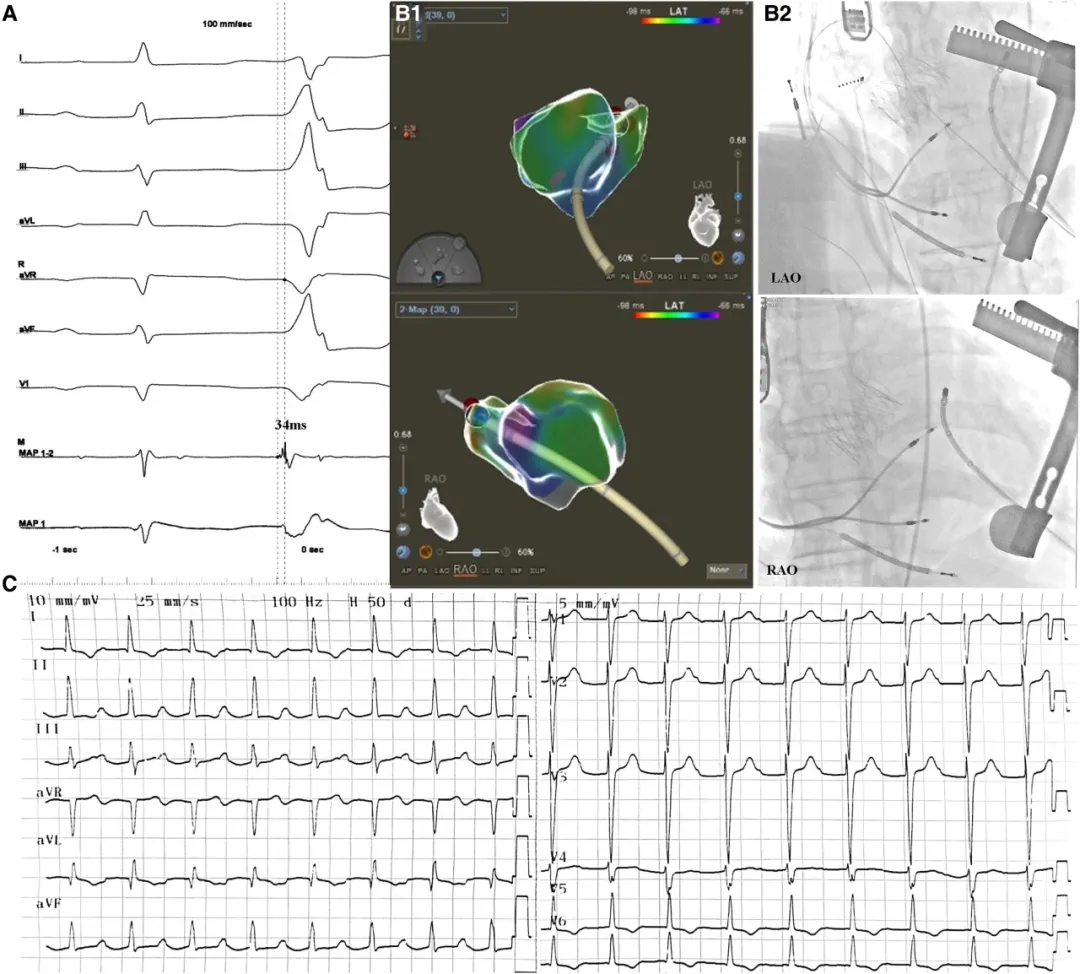
图1 术前心电图。表现为窦性心律伴一度房室传导阻滞及频发室性二联律。室性早搏(PVCs)形态学特征为:胸导联V1呈R波型,V2-V6导联呈Rs或RS型,提示其起源位于左心室。
治疗过程
本次手术在复合手术室(HOR)全身麻醉下进行。经心尖路径植入#29号经导管主动脉瓣生物瓣膜。瓣膜释放过程中,通过植入式心脏复律除颤器实施快速心室起搏(160次/分)。
随后经同一心尖穿刺点置入短鞘,导入消融导管,在三维心脏电生理标测系统引导下于二尖瓣环1点钟位置标测到室性早搏起源点,其局部电位较体表心电图提前34ms。射频消融(接触力8-12克,功率35W,温度43℃,灌注流速15mL/min)3秒内成功消除室性早搏,并于相邻位点进行巩固消融(图2)。
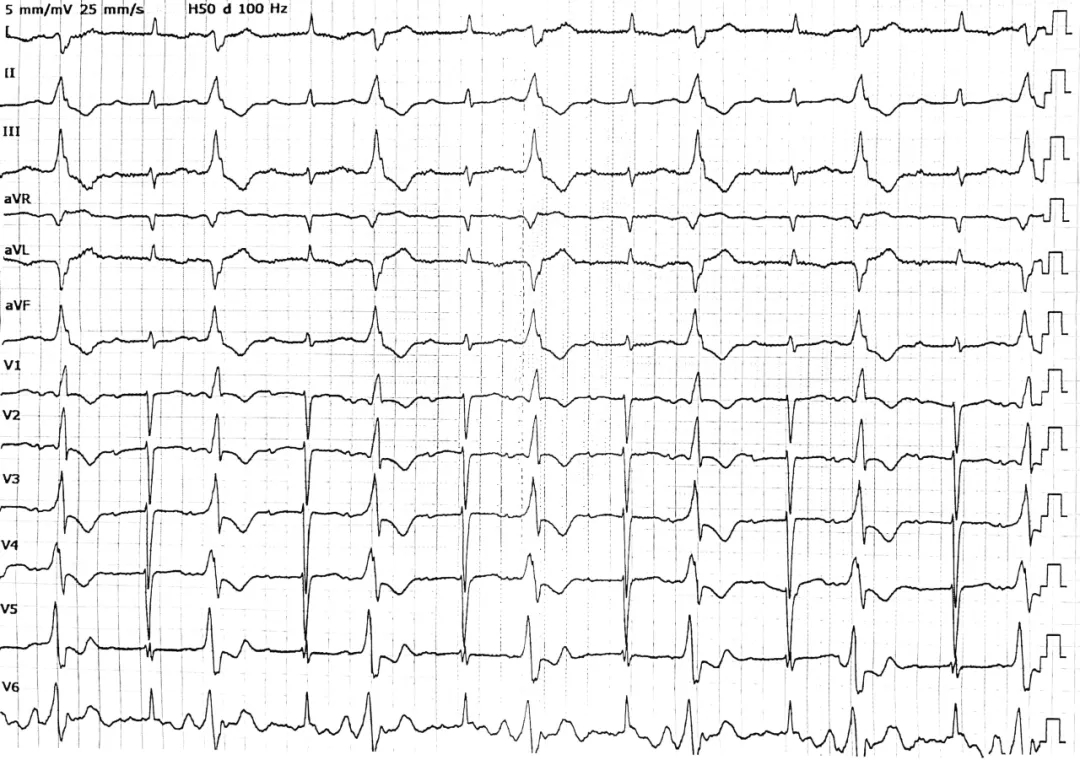
图2 消融靶点。(A) 室性早搏(PVC)起源点的心内电生理特征:最早激动点较体表心电图提前34 ms,消融导管(MAP1-2)可记录到心房电位。(B) 消融靶点的三维影像(B1)与X光投照体位(B2)。(C) 术后心电图。RAO:右前斜位,LAO:左前斜位。
术后随访
术后患者呼吸困难等症状逐渐改善。为期三周的随访动态心电图监测证实PVC被完全抑制。超声心动图显示显著的心脏逆重构:LVEDD降至63mm,LA内径降至35mm,LVEF提升至55%。主动脉瓣反流完全消失,二尖瓣反流改善为轻度。
讨论
心力衰竭是多种心脏疾病的最终归宿之一。本病例展示了结构性瓣膜异常与心律失常负荷在晚期心衰进展中的协同作用,以及经心尖联合入路同时处理这两种病变的治疗潜力。
结构性瓣膜功能障碍与高负荷PVC共同作用,会协同推动心力衰竭进展。重度主动脉瓣与二尖瓣反流导致慢性容量超负荷,引起左心室扩张和收缩功能受损;同时,高负荷PVC通过无效收缩和心律失常介导的重塑加剧心肌应变。若仅单独处理任一病变,可能难以阻断疾病进展。例如,单纯纠正主动脉瓣反流或许能暂时减轻容量超负荷,但持续存在的高负荷PVC将继续损害心室同步性并促进心律失常性心肌病;反之,若仅消融PVC而未处理瓣膜病变,心室将持续承受容量负荷压力。
因此,同期干预对实现全面逆重构至关重要,这一观点在本病例术后心脏维度(LVEDD 63mm)与功能(LVEF 55%)的快速恢复中得到印证,主动脉瓣反流与频发PVC是该患者慢性心功能不全的主要病因。由此可见,本病例突显了在处理多因素致心力衰竭时采取整体治疗策略的必要性。
经心尖复合术式通过单一入路同期完成TA-TAVI与PVC消融。传统分阶段干预对此类患者存在固有风险:若在TAVI前施行导管消融,需在重度主动脉瓣反流条件下操作,不仅增加手术复杂度,更会加重血流动力学不稳定——在心室功能受损严重的患者中,该风险尤为显著;反之,若在TAVI后经动脉逆行消融,则存在影响人工瓣膜功能或因导管操作受限导致标测不准确的风险。
本案例采用的经心尖路径使两项操作均高效完成,且未影响新置换瓣膜的功能完整性。心尖入路实现了左心室通路精准消融,并完全避免经主动脉瓣操作。该策略在降低手术创伤的同时,可以获得更好的协同疗效:TAVI即刻解除容量超负荷,为消融创造了稳定的电生理基质;而PVC的消除则阻断了心律失常介导的心肌重构。据目前所知,这是经心尖TA-TAVI与PVC消融在同一手术中联合实施的首例报道。此次双介入治疗的成功,彰显了通过统一入路整合结构与电生理治疗的可行性,尤其适用于无法耐受多次手术的高危患者。
值得关注的是,重度二尖瓣反流(27.3 cm²)在未直接干预的情况下改善为轻度。这证实本例二尖瓣反流属继发性改变,主要由左心室扩张与不同步驱动。TAVI与PVC消融术后,LVEDD的降低(83→63 mm)减轻了瓣环扩张,而PVC的消除恢复了心室协调收缩。这些变化共同促进二尖瓣叶对合改善,符合“功能性二尖瓣反流可能随心室逆重构而消退”的理论。这一发现对部分患者是否需同期行二尖瓣干预提出了挑战。
结论
经心尖复合术式代表了治疗瓣膜疾病合并心律失常高危患者领域的范式转变。该策略通过同步纠正主动脉瓣反流与室性早搏,有效阻断心力衰竭的恶性循环,促进心脏快速逆重构。这一实践彰显了以病理生理机制为导向的整合治疗在复杂心肌病管理中的核心价值。
专家简介
Li YB, Wu Y, Su C, Wu ZK, Wang LC. Combined transapical transcatheter aortic valve implantation and premature ventricular contraction ablation in a high-risk cardiomyopathy patient: a case report. Eur Heart J Case Rep. 2025 Sep 6;9(9):ytaf441. doi: 10.1093/ehjcr/ytaf441. PMID: 40977933; PMCID: PMC12448879.
本文为医谱原创,转载请标注来源
-END-
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系


发表留言
暂无留言
输入您的留言参与专家互动