JACC|经导管三尖瓣置换术:突破边界
经导管三尖瓣置换术(TTVR)目前已成为治疗重度症状性三尖瓣反流患者的一种可选方案。由于该领域尚处于早期应用阶段,许多挑战仍有待解决。本病例系列展示了三种不同情境,凸显了这类患者临床管理中的难点。从决策制定角度,我们探讨了TTVR在合并晚期心肝综合征患者中的应用合理性,以及一例既往接受过左侧心脏瓣膜手术后转诊行三尖瓣干预治疗的相对年轻患者案例。更多从技术和介入策略层面,我们描述了一例经导管修复失败后成功实施TTVR植入的病例。尽管TTVR在大样本人群中已显示出令人信服的安全性和有效性结果,但临床实践中的患者选择仍具挑战性,本病例系列有助于深化我们对TTVR在特定临床情境中作用的理解。
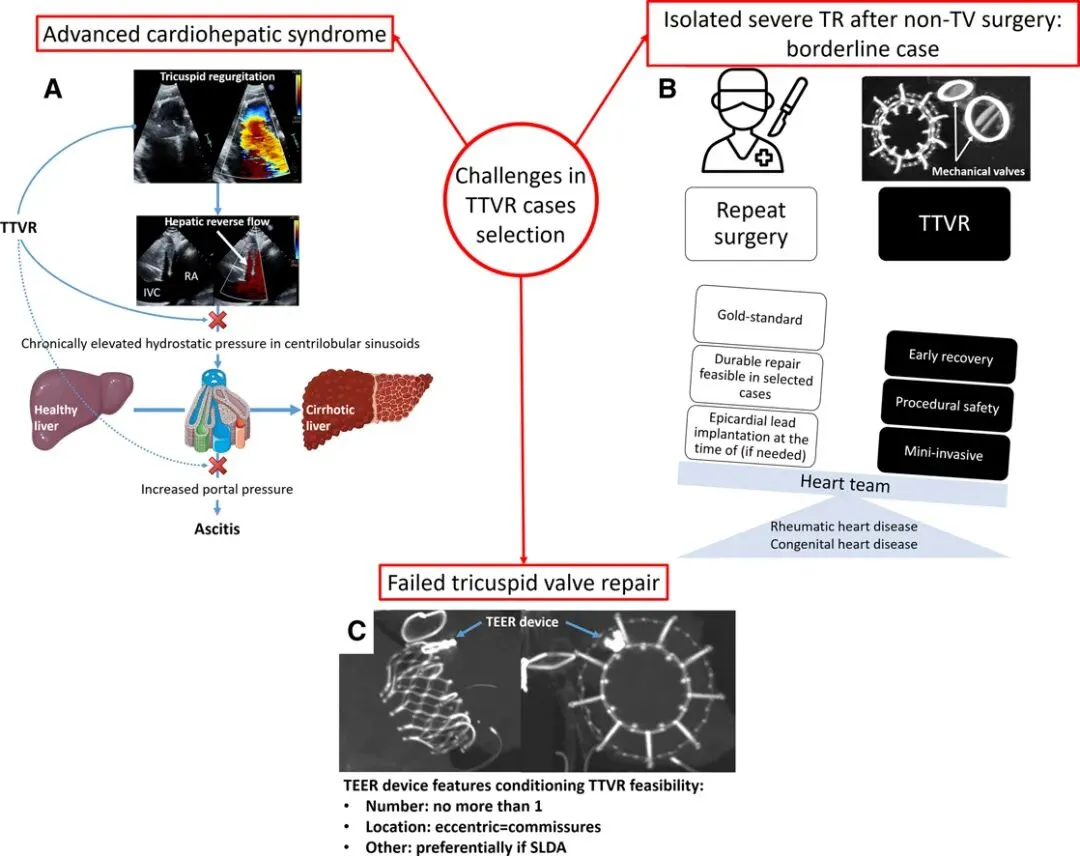
本病例系列中临床挑战主要特征的可视化总结示意图
(A) 心肝综合征的病理生理学特点及经导管三尖瓣置换术在这些患者中的潜在应用。
(B) 在既往接受外科治疗的高危患者中,心脏团队对孤立性重度三尖瓣反流的处理考量。
(C) 经导管缘对缘修复失败后成功植入经导管三尖瓣置换装置的病例。
核心要点
•合并心脏肝硬化的严重症状性三尖瓣反流患者可能是TTVR治疗获益显著的亚组人群。
•对于有心脏手术史且出现显著孤立性三尖瓣反流的患者,TTVR可视为避免高风险再次手术的可靠治疗方案。
•经专家中心严格筛选后,部分经导管缘对缘修复失败病例可采用TTVR进行治疗。
CASE 1
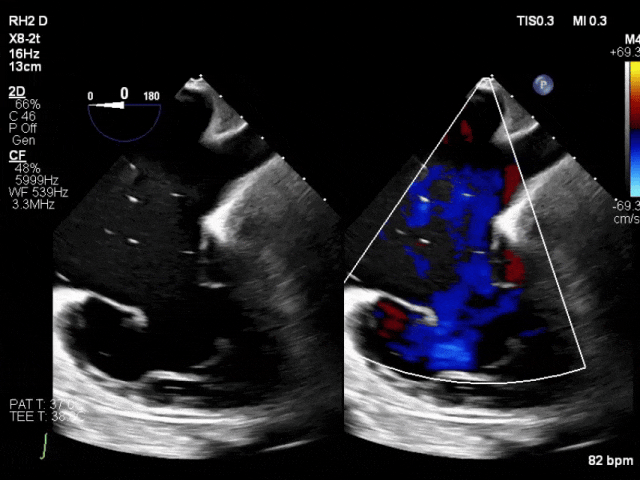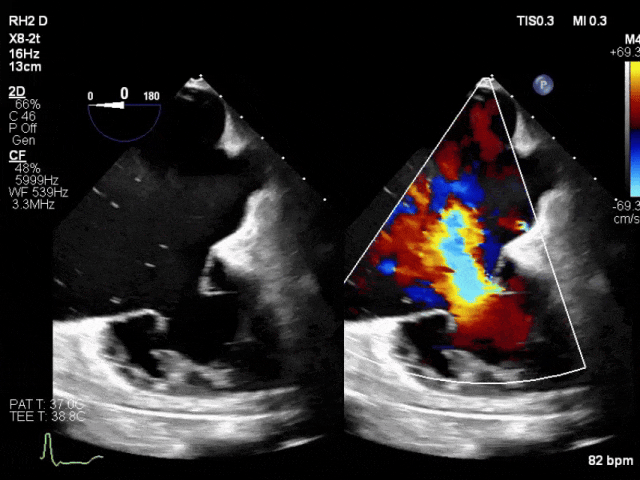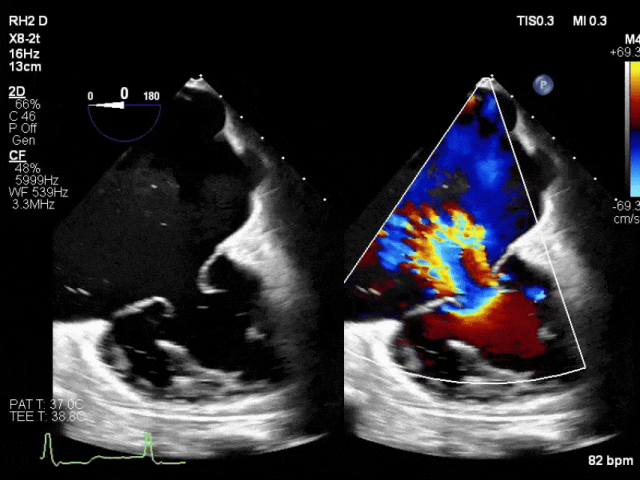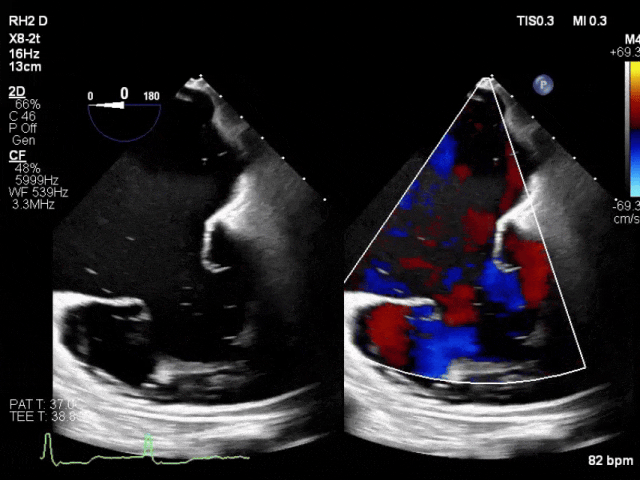
一名84岁男性,已知射血分数保留型心力衰竭合并永久性房颤,因意识状态改变及嗜睡入院。初步检查符合新诊断肝硬化(Child-Pugh C级)所致肝性脑病。患者同时存在低血压(89/53 mmHg)和乳酸升高(最高达6.5 mmol/L)。经胸超声心动图显示右心室严重扩张伴轻度功能障碍,以及瓣叶严重牵拉导致的极重度三尖瓣反流。基于实验室检查排除其他病因,其心脏病变被认为是肝硬化的主要诱因。
初始药物治疗包括乳果糖、利尿剂和多巴酚丁胺。鉴于营养不良状态,迅速启动鼻饲营养支持。患者极度虚弱,无法自主离床。
心脏团队会议提出两个关键问题:
1)三尖瓣反流是否为当前临床表现的主因?
2)纠正反流能否逆转病情?
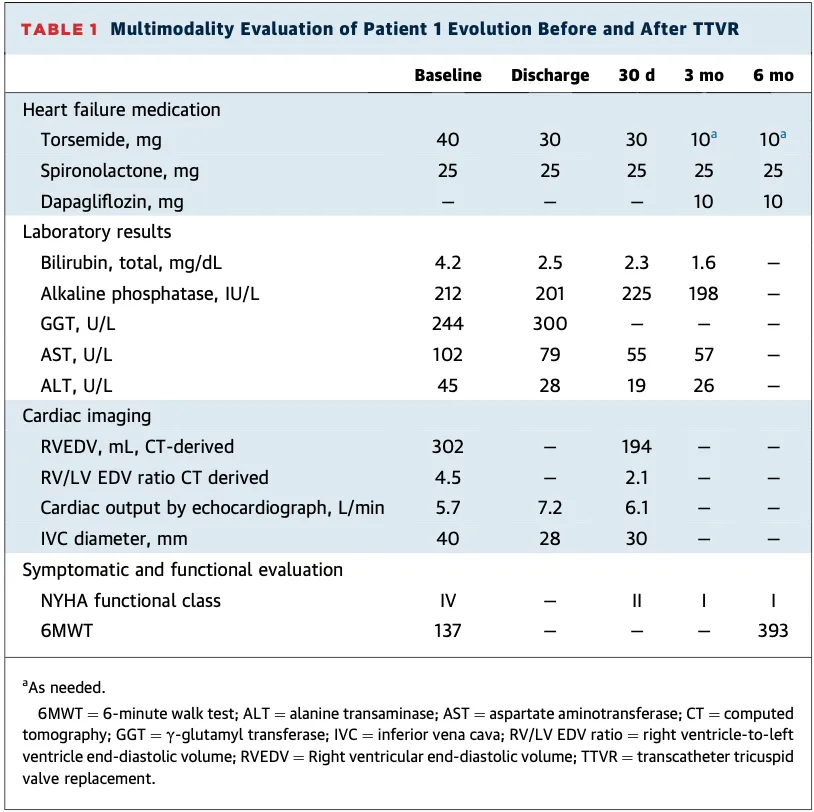
由于患者入院时危重状态和失代偿期肝硬化,姑息治疗也被纳入讨论。经初始药物治疗,患者乳酸酸中毒缓解、意识状态改善,病情稍有好转。转至康复机构进行体能恢复和营养状态改善。一月后再次就诊时,鉴于手术风险极高且解剖结构不适合经导管缘对缘修复,决定行TTVR治疗。手术成功植入EVOQUE瓣膜系统。术后7天出院并继续居家康复训练。6个月随访显示症状持续改善:腹胀及下肢水肿消退,运动耐量显著提升——6分钟步行距离从康复后的137米增至TTVR术后6个月的393米(表1)。末次随访时肝硬化严重程度从Child-Pugh C级改善至A级。
CASE 2
一名66岁女性因下肢水肿及腹胀加重入院。患者17年前因风湿性心脏病接受机械主动脉瓣和二尖瓣置换术,同期行De Vega三尖瓣成形术。
检查发现其瓣叶增厚并显著牵拉导致极重度三尖瓣反流。虽最初考虑再次手术行单纯三尖瓣置换,但患者病情迅速恶化,因容量负荷过重住院,需强效静脉利尿剂及多次腹腔穿刺。临床状况持续恶化,患者极度衰弱。外科会诊认为其因衰弱及慢性肝病属手术极高危人群。
经优化心衰治疗无改善后,决定采用Edwards EVOQUE瓣膜行经导管三尖瓣置换术,虽存在机械瓣干扰仍成功完成高质量影像引导植入。术后出现快速心室率房颤,经胺碘酮控制;低血压发作需血管活性药物支持,6天后停用。术前4天开始的静脉利尿治疗持续至术后,出院前转为口服用药。因拔管前发现下咽部缓慢渗血,在确认出血风险受控后延迟启动肝素/华法林桥接治疗。患者术后12天出院。1年随访时症状完全缓解,未再需腹腔穿刺。术后4年余未再因心血管事件住院,TTVR功能正常且停用利尿剂。但期间多次因维生素K拮抗剂相关出血事件(胃肠道、关节)入院,均经保守治疗控制。
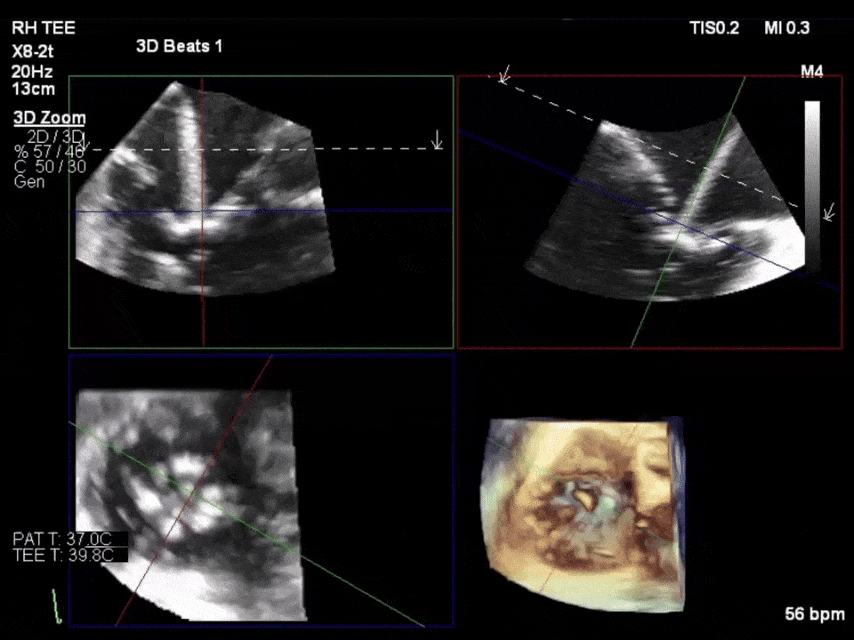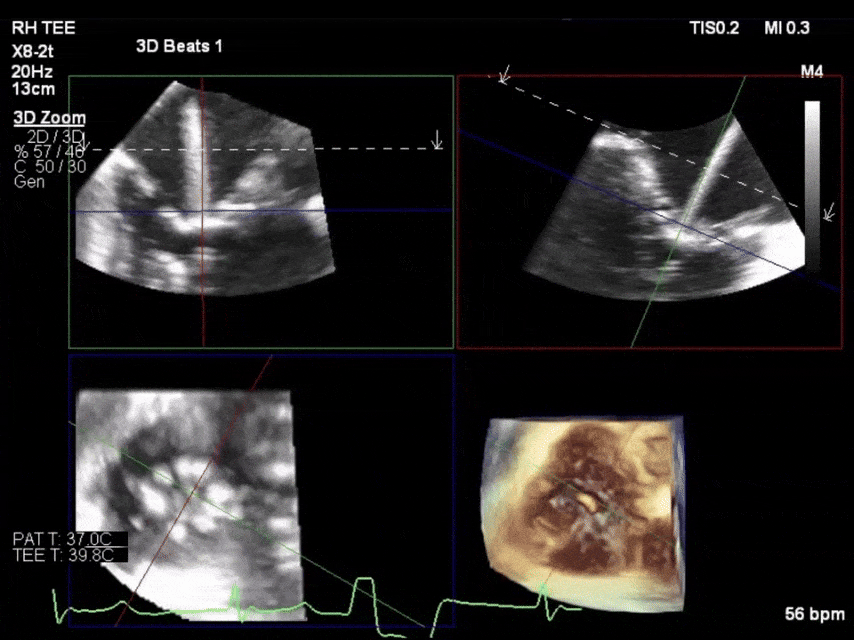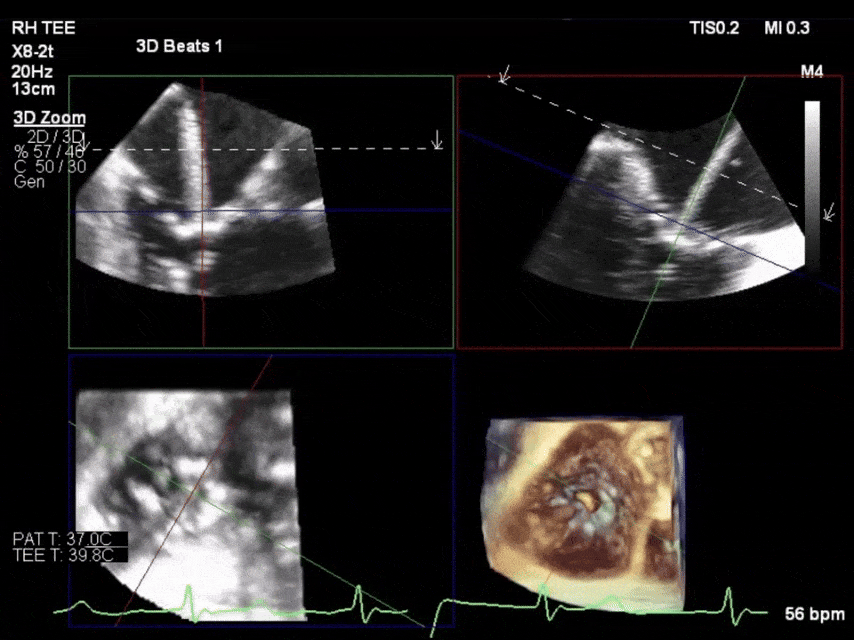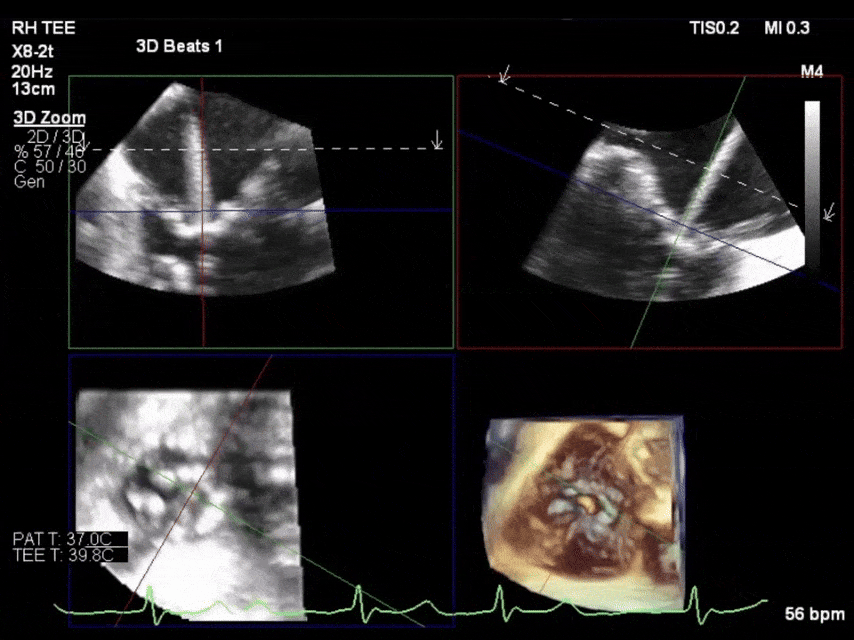
CASE 3
69岁女性,既往有房颤病史、4年前接受A型主动脉夹层修复术,3年前因重度二尖瓣反流(MR)及三尖瓣反流(TR)行经导管缘对缘修复术(TEER),此次因心衰管理问题就诊寻求第二诊疗意见。
二尖瓣修复效果持久稳定,但TR因发生单侧瓣叶装置附着(SLDA)于术后短期内复发为极重度反流。尽管强化药物治疗,症状仍持续恶化,遂考虑TR再次干预。
虽患者相对年轻,但心脏团队评估认为其因既往手术史及衰弱状态属外科高危。经导管方案中,因存在较大对合间隙及原发性瓣叶退变,再次TEER不可行,故TTVR成为唯一选择。前叶脱落的夹子对依赖瓣叶锚定的EVOQUE瓣膜植入构成挑战——该夹子可能阻碍锚定件进入瓣叶后方并影响成像。但由于脱落夹子靠近前隔联合处,研判其可为输送系统操作及瓣膜释放保留中央区足够空间。术中对锚定件与TEER装置的相对位置进行精确定位评估,最终锚定件分列装置两侧无空间冲突,且无瓣周漏。1年随访时患者自述"重获新生",未再出现心衰症状。
讨论
接受三尖瓣反流干预的患者病情复杂,其管理需要与心衰患者同样采取全面、多学科协作的治疗策略。经导管三尖瓣置换术(TTVR)现已能够为疾病进展更晚期的患者提供治疗。本病例系列揭示了我们在TTVR患者选择过程中面临的关键挑战。
晚期心肝综合征
患者1反映了肝硬化患者合并重度三尖瓣反流(TR)与慢性肝病时形成的恶性循环:在原发性病因基础上,充血性肝损伤进一步加重。这种状态下,静脉淤血导致肝小叶中央窦状隙结构损伤,加剧门静脉高压并引发顽固性腹水。从病理生理学角度看,显著的血流动力学肝静脉压力梯度使患者对中心静脉压(CVP)升高极度敏感。因此TR可能是慢性肝病失代偿的诱因,这与CVP被公认为慢性心衰患者肝功能异常的主要预测因子相符。本例患者因就诊时病情危重,我们未能预见到瓣膜治疗会带来如此显著的临床获益。这类患者常因病情过重被排除于干预治疗之外(即C类人群)。鉴于肝病与TR继发容量负荷过载的相互作用,慢性肝病本身不应成为TTVR的绝对禁忌证,但需专门研究明确该疗法在此类亚组患者中的作用。实际上,TR纠正后CVP降低可能使这类患者获益最大,但肝功能障碍的病因至关重要——如本案例所示,原发性心脏病因患者在TTVR后改善可能最显著。
非三尖瓣手术后孤立性重度TR
患者2代表既往接受过瓣膜手术(多为左心瓣膜病或先天性右室流出道功能障碍)后出现症状性孤立性重度TR的典型病例。本例采用的De Vega成形术(因疗效不佳已淘汰)未植入人工瓣环等可作为球扩瓣平台锚定区的材料。就获益/风险比而言,重复心脏手术的预后影响已明确纳入常用外科风险评估体系(STS和EuroSCORE II评分),但最新TR专用评分TRI-SCORE未包含该要素。对于风湿性或先天性心脏病常见的相对年轻患者,在其病程中适时采用微创经导管治疗(作为后续再次手术的过渡)可能符合终身管理理念。鉴于TTVR的安全性,对于有心脏手术史的临界孤立性重度TR患者,这或将成为可靠策略。此类病例因存在手术植入物使超声成像困难,术前需仔细评估,术中可能需心腔内超声辅助。
TEER失败后的TTVR
TEER是目前研究最深入、技术最成熟的TR经导管治疗方案,但中度以上残余TR被证实是预后不良的强预测因子。因此决策时需评估能否实现充分TR减轻。TTVR的优势在于可使90%以上患者术后TR降至轻度以下。本案例证明TTVR可作为TEER后显著残余TR的补救方案,但需精细解剖评估。我们认为存在多个TEER装置或非联合部定位是TTVR的两大潜在限制因素。本例因单侧瓣叶装置附着使器械向心室侧移位,反而使TTVR瓣膜能在原生瓣环实现完美密封而无显著瓣周漏。随着经验积累,这类手术可安全实施,但必须在高度专业化中心进行评估以确保成功率。
结论
随着TTVR应用拓展,对其治疗价值的深入理解将优化患者选择。本文三个成功案例呼吁开展更多研究验证这些有限样本得出的推论。
参考文献 <上下滑动查看>
-END-
更多内容推荐
关注医谱 专业的心血管医生学术交流平台!
版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系。

发表留言
暂无留言
输入您的留言参与专家互动