临床共识声明 | 心血管多模态成像在法布雷病评估中的作用
导语
安德森-法布雷病(Anderson-Fabry disease,AFD)是一种罕见的X连锁遗传性疾病,其特征是α-半乳糖苷酶A缺乏,该酶缺陷会影响糖鞘脂代谢,导致球三糖神经酰胺(Gb3)在溶酶体内过度蓄积。AFD可累及肾脏、心脏、血管和神经系统,主要见于儿童期发病的男性患者,但心脏表现常出现在成人中。AFD心肌病由心肌细胞内Gb3蓄积引起,最初表现为左心室肥厚和舒张功能障碍,进而发展为限制性心肌病和双心室受累的心力衰竭。AFD心肌病的早期诊断可能较为隐匿,需要与其他具有肥厚表型的心肌病进行准确鉴别诊断。然而,及时启动特定治疗至关重要,这些治疗已显示出良好前景,尤其是在早期治疗时。诊断心脏受累的AFD需要临床评估、基因检测和心脏成像的详细整合。基础和高级超声心动图、心脏磁共振(CMR)和核成像可为早期诊断提供关键信息,且这些患者的管理通常仅限于该领域具有丰富专业知识的中心。
2025年发布在《Eur Heart J Cardiovasc Imaging》(中科院Top1区,IF:6.6)的这篇本临床共识声明由欧洲心脏病学会(ESC)心肌和心包疾病工作组以及ESC欧洲心血管影像协会(EACVI)的专家制定,旨在为所有临床医生提供实用建议,指导多模态成像在AFD心脏受累的诊断评估、预后分层和管理中的应用。
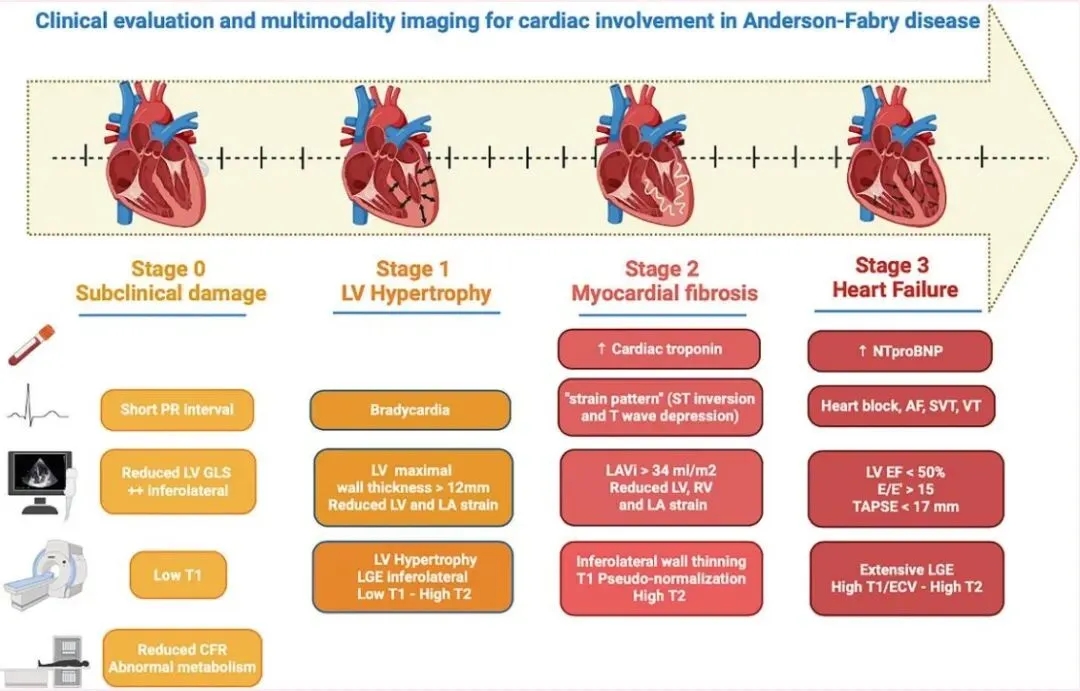
图像摘要
01
安德森-法布雷病(AFD)是一种泛种族分布的X连锁罕见遗传性疾病,主要影响青壮年的糖鞘脂代谢。具体而言,该疾病的缺陷在于α-半乳糖苷酶A(α-GAL)基因,导致球三糖神经酰胺(Gb3)在溶酶体内病理性蓄积,进而引起细胞肥厚和功能障碍。据报道,其发病率在1/40,000至1/117,000之间,但这可能被低估,因为近期新生儿筛查显示其患病率高达1/8800。
AFD的经典表型由GLA基因的严重遗传缺陷导致,酶活性为零或极低,见于男性患者,其特征为儿童期发病和多系统疾病,主要累及肾脏、心脏、血管和神经系统。在具有残余α-GAL活性的特定遗传变异的男性患者中,临床表现通常仅限于心脏,并在成年期显现(即所谓的晚发表型或心脏变异型)。女性患者中,X染色体的随机失活导致心脏受累程度各异,通常在成年后期发病,并具有一些特定特征。在经典型和晚发表型中,包括心力衰竭和心律失常在内的心脏受累是AFD患者生活质量下降和死亡的主要原因。据估计,在原因不明的左心室肥厚(LVH)成人患者中,AFD的患病率为0.5%至1%。心脏损伤进展缓慢,在症状出现前多年保持亚临床状态。为了在早期阶段怀疑AFD,临床医生应考虑临床预警信号和仪器检查结果。在经典表型中,早期心外表现可能提示诊断。在晚发心脏变异型中,鉴别诊断可能更为复杂,需依赖心电图和成像预警信号的识别。心电图(ECG)可显示早期指标,如短PQ间期和复极异常。但在大多数情况下,临床怀疑由成像结果引发,常见于二维(2D)超声心动图和心脏磁共振(CMR)。随后,男性患者需进行α-半乳糖苷酶A/LysoGb3检测,女性患者需进行基因检测以确认诊断。多模态成像在心脏受累分期和预后分层中也处于核心地位。本临床共识声明旨在描述基础和高级多模态成像在AFD心脏损伤的诊断、分期和监测中的作用,并探讨当前存在的差距和未来方向。
02
AFD是由GLA基因致病性变异引起的肥厚型心肌病的X连锁表型模拟疾病。数百种不同的变异与该疾病相关,其中大多数为错义变异。GLA基因的产物α-半乳糖苷酶A是一种酶,可从通过内吞作用进入溶酶体的寡糖、糖蛋白和糖脂中切割半乳糖。Gb3是AFD中在包括心脏、肾脏、皮肤和血管内皮在内的众多组织中蓄积的主要酶解底物。
由于大量罕见突变(私人突变)的高患病率,研究AFD的基因型-表型关系较为困难。但现有数据表明,家族内和家族间的表型异质性较为常见。尽管如此,保留残余α-半乳糖苷酶A活性的致病性变异(可通过检测评估用于诊断,图2)通常与导致功能完全丧失的突变相比,表型更轻微。
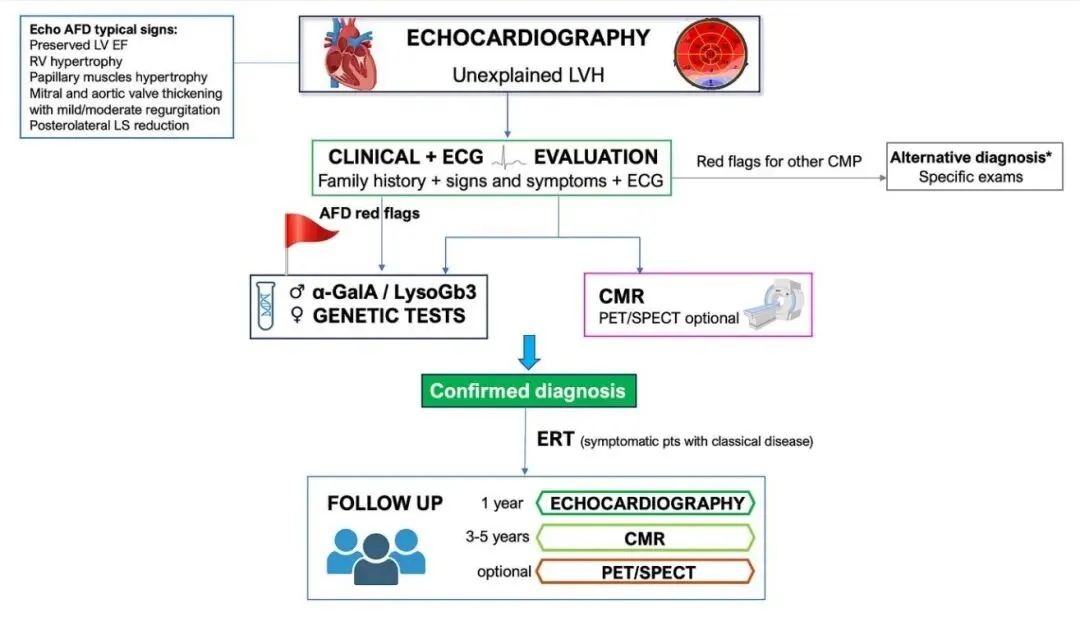
图1 AFD诊断和监测的建议流程:临床评估与多模态心脏成像的应用
注:* 心脏淀粉样变性、糖原贮积症、肥厚型心肌病和线粒体病;α-GalA act.:α-半乳糖苷酶A活性;CMP:心肌病;EF:射血分数;LS:纵向应变;LVH:左心室肥厚;LysoGb3:溶酶体球三糖神经酰胺;RV:右心室。
识别特定的致病性变异对于选择最合适的治疗至关重要,因为并非所有变异都可通过分子伴侣治疗。AFD的全身性受累具有许多典型体征,被称为“AFD心外预警信号”:肾功能不全、神经病理性疼痛、血管角质瘤、白蛋白尿、角膜涡状混浊、少汗症、冷热不耐受和运动不耐受、胃肠道症状(恶心、呕吐、非特异性腹痛、便秘和腹泻)、听力损失、耳鸣和眩晕。
AFD的性别差异
女性AFD患者通常发病较晚,病程较轻,但X染色体的偏倚失活可能导致其表型与半合子男性同样严重。已有研究描述了性别特异性的血浆生物标志物组,提示蛋白质组水平存在性别差异。与男性相比,女性患者的严重左心室肥厚(LVH)通常发生在晚年,但在肥厚出现之前,可通过应变超声心动图等先进技术提示替代性纤维化,并通过CMR识别。在法布雷病结局调查中,约46%的女性AFD患者出现心脏症状,其中包括心绞痛、呼吸困难和心悸。总体而言,女性心力衰竭的发病时间晚于男性,预期寿命更长。在严重瓣膜反流或狭窄方面,未发现两性之间存在显著差异。
03
基础超声心动图
-
左心室形态学
心肌病是AFD的主要表现。在更常见的晚发形式中,心肌病是主要且通常是唯一的表现。超声心动图适用于评估与心肌病相关的症状,包括劳力性呼吸困难、心房颤动、房室传导阻滞、异常心电图或AFD家族史。在存在提示性临床特征的情况下,原因不明的LVH应引起对AFD的怀疑。法布雷心肌病(FC)的特征是LVH[左心室(LV)最大壁厚度≥12mm],这是中老年AFD患者超声心动图的典型表现。LVH通常为向心性,但与肌节基因突变引起的心肌病难以区分的室间隔肥厚也很常见。FC呈进行性,LVH随年龄增长而加重。尽管弥漫性向心性LVH是最常见的异常,但累及室间隔的区域性LVH可能导致动态左心室流出道梗阻(LVOTO),伴二尖瓣叶收缩期前向运动,发生率高达45%。部分患者可能仅表现为心室中部或乳头肌肥厚以及心室中部梗阻,而非LVOTO,另一些患者可能表现为远端LVH。在舒张期短轴视图中,若至少一个乳头肌的垂直或水平直径超过11mm,则认为乳头肌肥厚(图3)。乳头肌肥厚可能先于LVH出现,但并非AFD特有。左心房常扩大。右心室肥厚和主动脉根部扩张是AFD超声心动图的其他相关表现(表1)。AFD与其他心肌病的主要成像特征总结于表2。
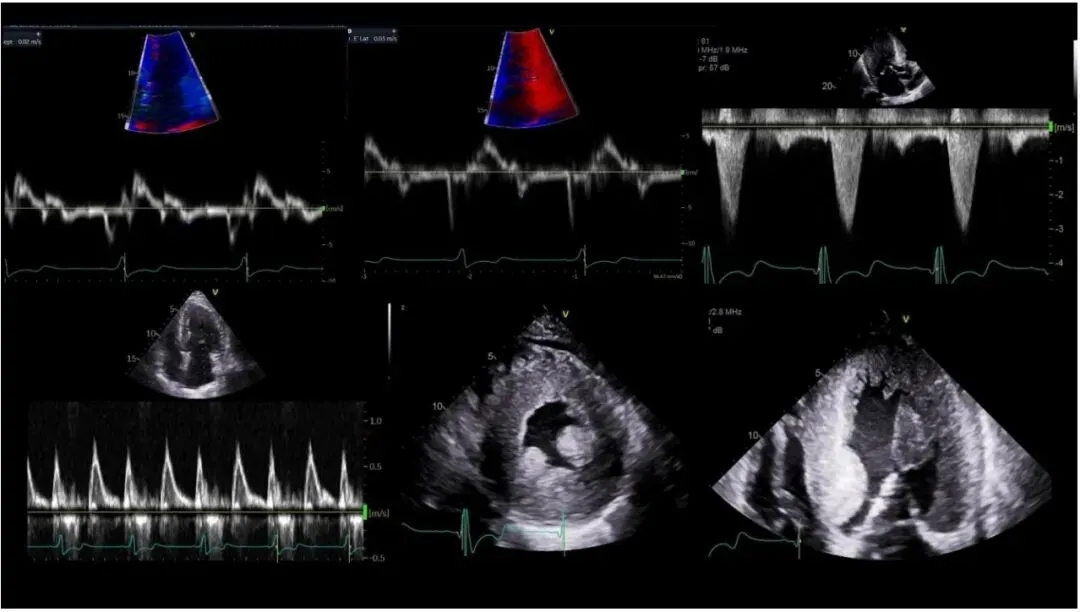
图2 法布雷病超声心动图表现的代表性病例
上左、下左和上中:左心室舒张功能障碍;上右:左心室流出道梗阻(LVOTO);下右和下中:左心室肥厚(LVH)。
-
左心室收缩和舒张功能
射血分数通常保持正常,左心室大小正常。LVH常伴随主动脉瓣和二尖瓣增厚以及相关的轻度瓣膜反流。左心室整体纵向应变(GLS)降低可能是FC的早期信号。左心室舒张功能障碍和左心室射血分数保留的异常纵向应变是AFD的早期表现,而非随年龄增长进展并与症状相关的显著LVH。左心室舒张功能障碍随LVH加重而进展。在部分患者中,心室中基底段下侧壁可能表现为运动减退或无运动,反映区域性心肌纤维化。据报道,在心脏受累晚期的患者中,运动时每搏输出量增加受限,左心室收缩储备异常。
-
心脏瓣膜病和主动脉评估
AFD中显著的心脏瓣膜受累通常不常见。最早的描述可追溯至20世纪70年代中期,当时在两名纯合子患者的心脏活检标本中发现二尖瓣和三尖瓣重构,包括瓣叶增厚和瓣叶间皱褶。反流比狭窄更常见,但仅少数病例(约10%)达到严重程度,主要与年龄增长和肾功能恶化相关。需要全面评估左心室几何形状和重构,以描述功能性二尖瓣反流的可能机制,包括腱索束缚和瓣环变形。主动脉根部扩张也可能发生,男性患者年轻时即可出现,主要累及瓦氏窦和升主动脉水平,可能伴随主动脉反流。由于糖鞘脂沉积,主动脉瓣受累较少见(图3A)。已有少数严重主动脉瓣狭窄患者接受外科手术或经导管介入治疗的报道,术前评估需采用多模态成像方法,以改善左心室和主动脉的形态功能特征,不仅关注主动脉瓣和血流动力学。主动脉直径增大是AFD患者的常见表现,多为轻度或中度扩张。主动脉扩张的患病率随年龄增长而增加,且男性患者显著高于女性患者。在一项探索106例AFD患者主动脉重构的大型研究中,男性主动脉根部和升主动脉扩张的发生率分别为32.7%和29.6%,而女性分别为5.6%和21.1%。AFD中主动脉扩张的发生归因于血管内皮中糖脂蓄积引起的主动脉中膜退行性改变,尸检生化研究已证实这一点。主动脉根部直径>40mm与晚期心脏受累的超声心动图征象相关,包括严重LVH。然而,尚未有该人群中需要手术或出现主动脉瘤破裂或夹层等并发症的报道。
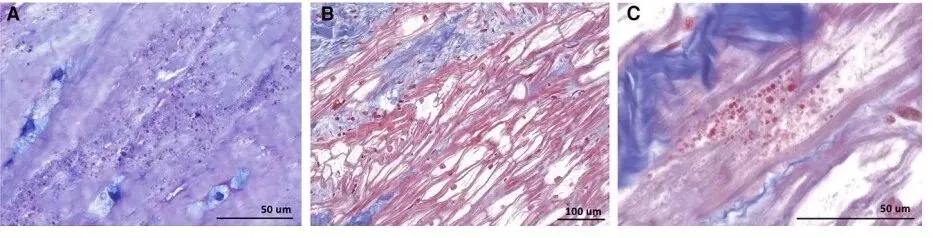
图3 主动脉瓣可见含 Gb3 的小体沉积(A,甲苯胺蓝染色)。心内膜心肌活检显示间质纤维化,以及肌纤维丢失和广泛空泡化的肥大心肌细胞。由于组织处理,大部分心肌细胞表现为空泡状(B)。在部分心肌细胞中,可见由 Gb3 沉积构成的圆形小体簇(C)。Masson 三色染色。
-
右心室结构和功能
右心室肥厚(RVH)定义为右心室(RV)壁厚度>5mm,是AFD的常见表现。RVH的患病率通常在31%至40%之间。然而,Niemann等人发表的一项研究评估了53例拟行酶替代治疗的AFD患者,报告RVH发生率高达71%。RVH的发生率随年龄增长而增加,且与LVH不同,它对女性和男性的影响似乎相似。RVH与疾病严重程度相关,约三分之二的LVH患者存在RVH。在无明显肺动脉高压的患者中,孤立性RVH较为罕见。通过右心室舒张末期直径评估的右心室大小通常在正常范围内。Kampmann等人描述RVH可能伴随收缩功能障碍。在该研究中,28%的RVH患者发现严重收缩功能障碍[三尖瓣环平面收缩期位移(TAPSE)<10mm]。然而,后续研究报道的右心室收缩功能障碍发生率显著较低。Palecek等人指出,在58例AFD患者中,仅1例(2%)存在右心室收缩功能障碍(TAPSE<19mm)。Graziani等人发现,45例AFD患者的TAPSE和右心室分数面积变化均正常。在该研究中,仅1例患者的收缩期脉冲频谱多普勒速度降低(<9.5cm/s)。约一半的AFD病例报告存在右心室舒张功能障碍,但严重右心室舒张功能障碍似乎非常罕见。

表1 AFD的多模态成像关键表现
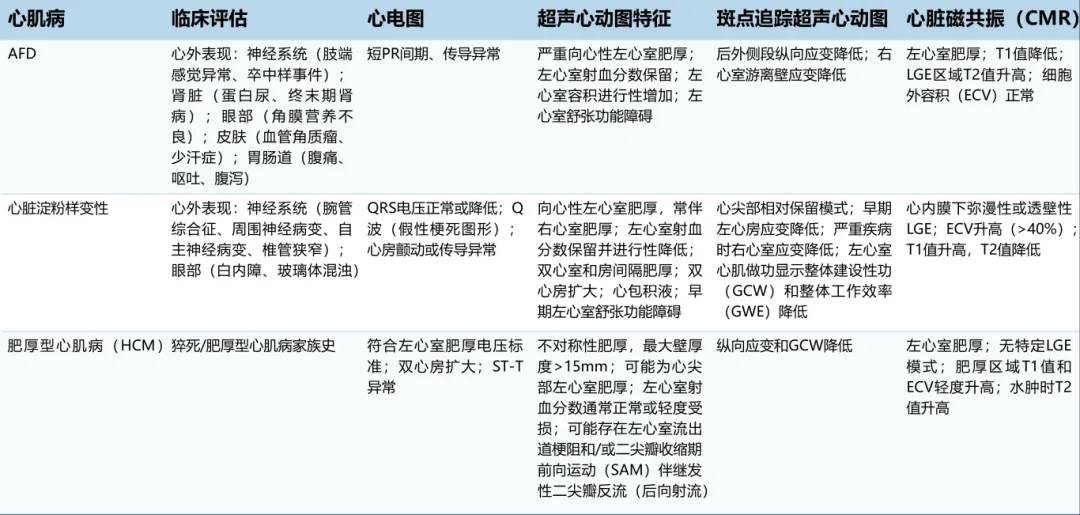
表2 AFD、心脏淀粉样变性和肌节性肥厚型心肌病(HCM)的临床、心电图和成像鉴别诊断特征
注:AF:心房颤动;LV:左心室;LVEF:左心室射血分数;LVH:左心室肥厚;LVOTO:左心室流出道梗阻;MR:二尖瓣反流;RV:右心室。
高级超声心动图
-
斑点追踪超声心动图
AFD患者心肌组织内糖鞘脂蓄积在晚期被纤维化取代,纤维化通常位于后外侧壁基底段。可通过斑点追踪超声心动图无创性怀疑心肌纤维化的发生。事实上,在AFD中,左心室纵向应变通常在基底后外侧段降低,这与CMR表现一致(图5)。此外,基底-心尖段圆周应变梯度消失是AFD患者心脏受累的早期标志物。最新的欧洲心脏病学会(ESC)心肌病管理指南已将左心室GLS降低纳入AFD预警信号,但未设定特定临界值。此外,右心室应变已被证实是与肥厚型心肌病鉴别的有用标志物:事实上,与肥厚型心肌病患者相比,AFD患者的右心室游离壁应变受损更严重(<23%),且游离壁与整体右心室应变差异更小。最后,由于AFD主要以左心室舒张功能障碍为特征,并导致射血分数保留的心力衰竭(HFpEF),如最新EACVI多模态成像评估HFpEF共识所建议,左心房储备应变可作为评估HF患者舒张功能和左心室充盈压的标志物。这可能有助于这些患者心脏异常的早期诊断,确保早期治疗,并用于治疗监测。
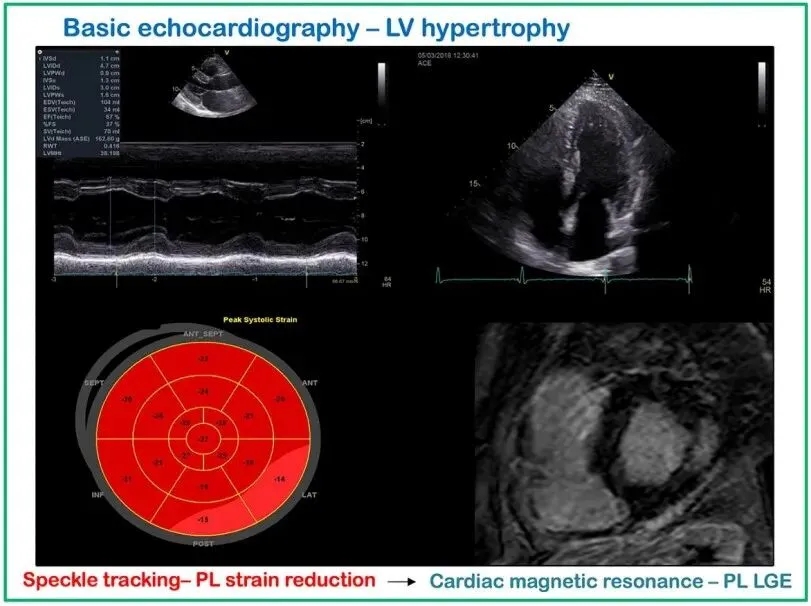
图4 法布雷病多模态成像分析的代表性病例
标准和斑点追踪超声心动图以及心脏磁共振成像结果;PL:后外侧;LGE:晚期钆增强。
-
三维超声心动图
三维超声心动图有望克服二维超声心动图在评估复杂左心室心肌力学方面的一些内在局限性,提供额外的变形参数(如三维面积应变),并通过单次三维采集更准确地定量左心室容积、质量和射血分数(图6)。在AFD患者中,应随时间监测左心室壁厚度和左心室质量。在不对称肥厚的情况下,二维计算可能高估左心室质量和最大壁厚度。此外,在AFD患者中,二维超声心动图测量的左心室质量比CMR测量的可重复性更低。研究表明,使用二维超声心动图而非CMR可能影响29%患者的LVH诊断、26%患者的疾病特异性治疗资格以及预后。三维超声心动图无需任何几何假设即可测量左心室质量,提供的值更接近CMR测量结果。此外,与二维计算相比,三维左心室质量的观察者间和复测变异性更小。
目前,日常实践中三维斑点追踪的可行性(63%-83%)低于二维斑点追踪超声心动图(80%-97%)。值得注意的是,据报道AFD中三维应变的可行性为76%。三维应变参数与左心室质量呈负相关。其中,三维GLS成分是最敏感的参数,与心力衰竭严重程度[利钠肽水平和纽约心脏协会(NYHA)分级]和长期预后相关。另一方面,左心室下侧壁中部和基底段区域性三维圆周应变降低反映了CMR晚期钆增强(LGE)所示的典型AFD相关心肌瘢痕。三维应变还可能有助于识别与右心室肥厚程度相应的早期亚临床右心室功能障碍。然而,三维应变的准确性(尤其是区域水平)在很大程度上取决于最佳图像质量和容积率。追踪不佳主要影响心尖三维数据集中远场的左心室基底段。解决这些技术问题需要足够的专门培训和实践技能,这可能显著限制常规临床实践中使用当前技术进行三维斑点追踪的患者数量(图5)。单次心跳三维采集可实现的空间和时间分辨率的技术改进以及人工智能算法的应用,可能会促进三维超声心动图在日常工作中的应用。然而,三维超声心动图相比传统二维超声心动图评估AFD患者的附加价值仍需更强有力的证据支持。
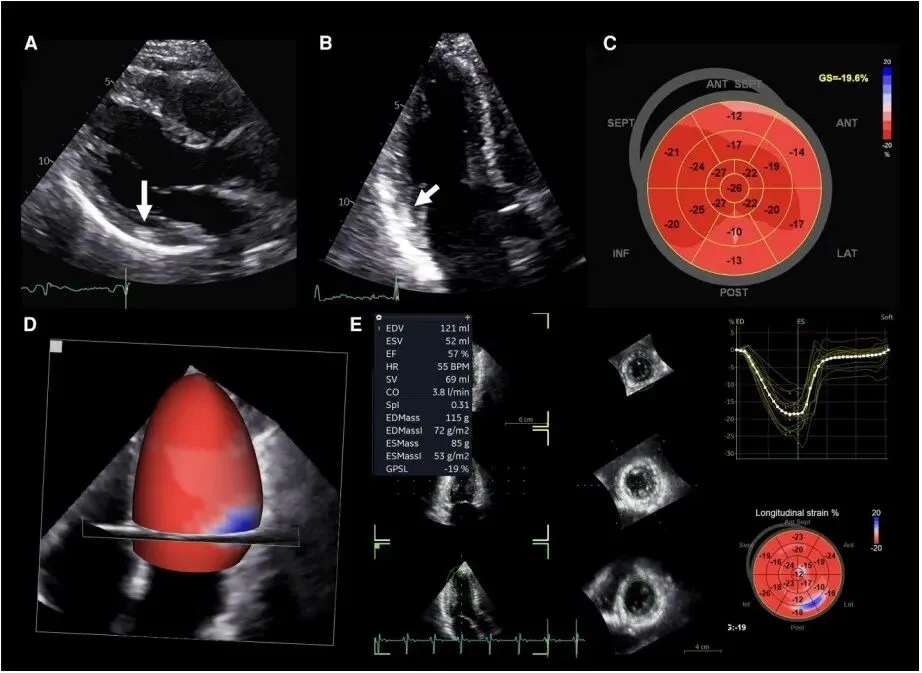
图5 57岁有FC家族史患者的二维和三维超声心动图早期心脏受累表现
ANT:前壁;SEP:室间隔;INF:下壁;LAT:侧壁;POST:后壁;GS:应变。
心脏磁共振(CMR)
-
心室形态学评估
尽管超声心动图足以诊断FC,但建议所有心肌病患者(包括FC)进行CMR检查(包括LGE和T1 mapping),以进一步表征心肌组织(图3)。CMR提供左心室结构和功能的金标准评估。标准CMR方案包括左心室长轴电影图像(两腔心、三腔心和四腔心视图),以进行形态学评估。然后从二尖瓣环到左心室心尖采集心室的相邻短轴电影图像。勾勒心内膜和心外膜边界后,可精确估算左心室质量、容积和射血分数。电影图像还可精确测量左心室壁厚度。CMR能准确显示下侧壁和前室间隔,这些结构有时难以通过超声心动图成像。基于人工智能的算法已被证明是左心室壁厚度定量的有价值工具,与经验丰富的观察者相比,具有更好的可重复性和更短的时间。如前所述,AFD最常见的表现是向心性LVH,通常伴随左心室乳头肌质量增加。此外,CMR可能显示AFD患者心肌小梁增多,这被描述为心脏受累的极早期信号。它还先于心肌T1值降低和LVH的发生。AFD的继发性结构改变,如左心房扩大和右心室肥厚,也可通过CMR识别并精确量化。此外,尽管左心室射血分数通常保持正常,但CMR应变分析可能显示左心室收缩力学受损。在疾病的肥厚前期,左心室GLS受损与原生T1降低相关,可能有助于早期心脏受累的诊断。同样,在疾病早期阶段即可检测到心房变形受损,先于LVH或舒张功能障碍的发生。这一发现支持AFD患者存在心房肌病的概念,该心房肌病直接由影响心房顺应性的Gb3蓄积引起。最后,最近验证的基于左心室和左心房容积分析的CMR模型可能允许无创估算左心室充盈压。尽管在此背景下尚未探索,但其应用在AFD患者的评估和监测中可能具有前景。
-
晚期钆增强(LGE)
LGE成像能够检测心肌替代性纤维化,在AFD患者的诊断路径和管理中发挥关键作用。在AFD中,LGE特征性累及左心室基底段下侧壁,呈中层分布。因此,在表现为原因不明LVH的患者中,这一发现应引起对AFD诊断的怀疑。然而,也有非典型模式的报道,且在疾病晚期,病变进展至其他左心室节段较为常见。LGE的患病率在40%至65%之间,在男性患者中,与LVH的严重程度相关。尽管如此,它也可能先于LVH的发生,尤其是在女性中。重要的是,心肌纤维化的存在和程度是AFD患者关键的预后决定因素,并预示恶性心律失常事件的风险增加。此外,LGE评估还可提供关于患者对疾病特异性治疗反应的重要信息。事实上,在开始酶替代治疗的患者中,LGE的存在与LVH逆转的可能性低以及心肌功能和运动能力改善有限相关(图7)。
-
T1-T2 mapping
原因不明的肥厚和典型的后外侧瘢痕可引起对AFD的怀疑;但mapping技术具有重要附加价值。Mapping是一种定量技术,其中单个图像像素根据纵向(T1)或横向(T2)磁性进行彩色编码。铁过载或脂质蓄积时可观察到T1降低,而心肌纤维化或水肿时T1升高。AFD通常降低心肌原生T1,这是细胞内糖鞘脂蓄积的结果,尤其是在板层小体中呈向心性脂质膜分布。T1降低始于疾病早期,先于LVH的发生。约40%的LVH阴性患者可检测到T1降低,且与早期心电图改变和疾病进展相关(图7)。在疾病晚期,T1降低更为显著。然而,随着炎症和纤维化的发生,信号可能变弱,若存在广泛LGE,甚至可能逆转。因此,解读T1 mapping时应谨慎,原生T1正常不能排除AFD诊断。尽管存在这一局限性,T1降低目前在AFD与其他LVH原因(包括慢性后负荷增加(高血压和主动脉瓣狭窄)、肥厚型心肌病和心脏淀粉样变性)的鉴别诊断中发挥关键作用。事实上,与AFD不同,这些疾病均以原生T1升高为特征,其中心脏淀粉样变性的升高通常更为显著。值得注意的是,与健康对照组相比,运动员心脏的原生T1也可能轻微降低,但数值通常保持在正常范围内。对于整体分析,应在中腔短轴T1图的室间隔绘制单个感兴趣区域,以减少磁化率伪影。为了评估局灶性改变,应在视觉检查发现异常的节段(尤其是基底段下侧壁)绘制额外的感兴趣区域。重要的是,建议根据特定的扫描仪和序列使用原生T1的局部参考范围。
T2在疾病表型分析中也具有价值,因为T2升高通常反映水肿。在AFD中,T2在左心室基底段下侧壁的LGE区域通常升高,并与肌钙蛋白升高相关。T2升高支持炎症在AFD发病机制中的关键作用,这与正电子发射断层显像(PET)和心内膜心肌活检的发现一致。在这方面,Gb3蓄积可能引发免疫介导的心肌炎,在高达56%的AFD患者的组织学检查中已检测到这一现象。重要的是,结合LVH、LGE和T1/T2 mapping可用于AFD心脏受累的分期。对于治疗监测,T1变化微小,表明现有治疗无法从心肌细胞中清除脂质,这为新的治疗方法提供了机会。
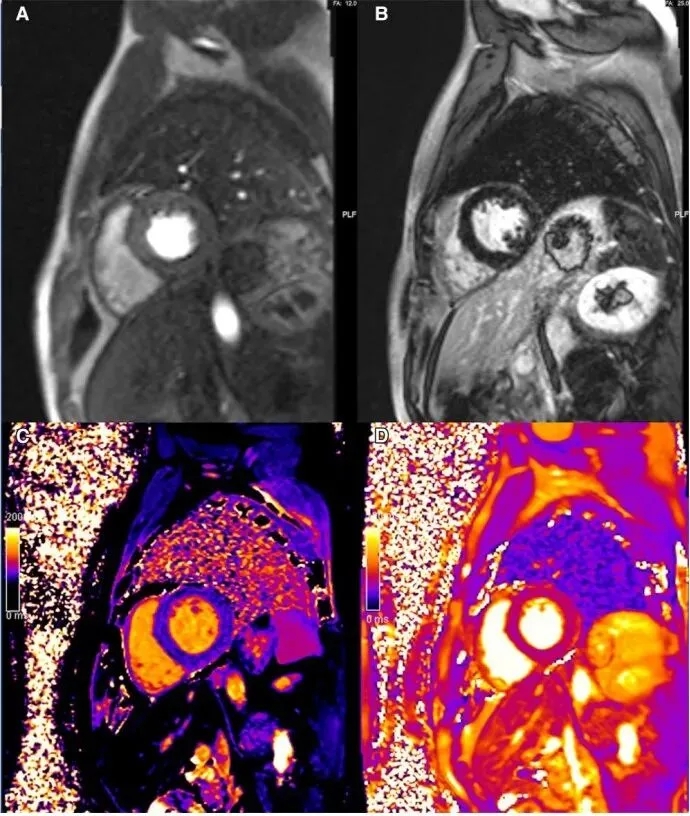
图6 早期AFD的心脏磁共振成像
43岁男性经典型法布雷病患者,接受酶替代治疗(ERT),电影序列显示轻度LVH(最大壁厚度12mm)(A),对比后序列无LGE证据(B)。原生T1 mapping值弥漫性降低(C),无节段性原生T2 mapping值升高(D)。
-
核成像
心脏单光子发射计算机断层显像(SPECT)和PET成像可为AFD患者提供有用信息,并深入了解其潜在病理生理学。需要进一步研究评估当前和未来的核成像技术如何有助于这些患者的临床评估和管理。AFD的一个特征是Gb3在包括心脏在内的各种组织中进行性蓄积。SPECT成像通常使用⁹⁹ᵐTc-甲氧基异丁基异腈等放射性药物,可使临床医生可视化和评估心肌灌注,而AFD中Gb3沉积可能导致心肌灌注改变。SPECT扫描上观察到的灌注缺损可提示心脏特定区域的血流灌注受损,这是AFD相关心脏受累的特征。2008年,Chimenti等人研究了AFD患者胸痛的机制。他们发现,心绞痛患者存在灌注缺损、冠状动脉血流缓慢和壁内动脉狭窄,表明微血管疾病可能是AFD患者症状发生和心肌功能进行性障碍的重要原因,突显了其临床相关性。
为了排除有胸痛或左心室功能障碍的AFD患者的微血管疾病(因为典型的SPECT灌注成像既无法可靠地可视化微血管疾病,也无法通过正常的冠状动脉计算机断层扫描或有创血管造影排除,除非收集功能指标),这些患者的灌注成像应优先选择PET定量灌注成像或使用新型数字SPECT系统的冠状动脉血流储备成像,或结合流量定量的CMR。Tomberli等人证实了这一点,他们发现PET获得的冠状动脉血流储备整体降低是法布雷病心脏受累的早期信号,与性别和LVH无关。因此,冠状动脉微血管功能障碍可能是AFD患者心脏受累的唯一表现,对临床管理具有潜在重要意义。
¹⁸F-氟脱氧葡萄糖-PET(¹⁸F-FDG-PET)通常用于基于巨噬细胞显示的葡萄糖利用增加评估心肌炎症。¹⁸F-FDG-PET也已在AFD中进行了研究。特别是,Spinelli等人研究了24名携带α-半乳糖苷酶A突变的女性。在该研究中,观察到局灶性¹⁸F-FDG摄取是疾病相关心肌损伤的早期信号,可能代表对心肌细胞Gb3蓄积的炎症反应。此外,¹⁸F-FDG摄取的存在与超声心动图显示的左心室纵向功能受损和CMR显示的LGE区域相关。特别是,Nensa等人使用混合¹⁸F-FDG-MRI在疑似心肌炎患者中前瞻性比较了¹⁸F-FDG-PET与LGE和T2加权MRI序列,表明MRI表现与心肌F-FDG-PET摄取增加总体一致性良好。需要进一步的数据来研究携带AFD相关突变的年轻患者的局灶性心肌¹⁸F-FDG摄取是否可作为疾病活动度的标志物和后续疾病进展的预测因子。如心内膜心肌活检所示(图4B和C),AFD中糖鞘脂的进行性蓄积最终可导致心肌纤维化,随后发生心脏交感神经去神经支配。最近的研究使用I-间碘苄胍(I-MIBG)-SPECT或专用PET示踪剂评估了这种蓄积的程度和后果,表明去神经支配区域与有无LGE的患者的左心室功能障碍相关。此外,已有证据表明,交感神经元似乎比心肌细胞更容易受到AFD的影响。Imbriaco等人证实,AFD患者的心脏交感神经元损伤通常先于心肌纤维化出现。他们的研究强调了I-间碘苄胍成像作为早期疾病检测工具的潜力。这一方面尤其有价值,因为它可能先于心肌纤维化,能够早期检测心脏受累。Spinelli等人证实了这些结果,揭示了心脏MIBG摄取降低与AFD心脏受累之间的重要关联。他们的研究表明,左心室纵向功能障碍可能作为疾病的早期信号出现。最后,Massalha和Slart强调了在不可逆纤维化发生前识别表型标志物的重要性。他们强调需要综合的多模态成像方法,包括I-间碘苄胍成像等技术,以及C-间羟基麻黄碱PET对心脏自主神经功能进行更准确量化的潜力。总之,心脏核成像为法布雷病的潜在病理生理学提供了重要见解。需要进一步的研究来确立核成像在法布雷病中的临床作用,尤其是新型分子成像技术。
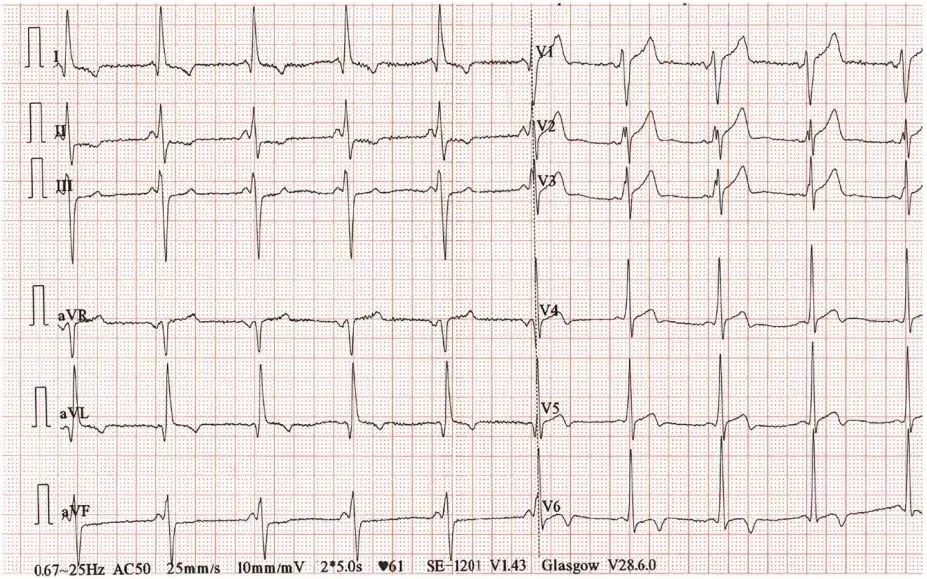
图7 AFD中的ECG特征。具有短PR间期,QRS和复极异常的AFD心电图的代表性病例。
-
AFD的早期心脏改变
AFD的临床特征谱较广,症状出现时间因残余α-半乳糖苷酶A(α-GAL-A)活性而异。在男性患者中发生的经典早发形式中,酶活性<1%,心血管体征在20-30岁期间出现,同时伴随多系统临床受累。
短PR间期和复极异常等心电图异常先于结构性心脏病和症状出现(图8)。30岁以后,约一半的男性和三分之一的女性出现LVH。因此,在儿童和年轻成人中出现LVH时,AFD的诊断可能性极低。在心肌病特征显现后,约60%的患者抱怨各种心脏症状,包括:劳力性呼吸困难,主要归因于射血分数保留的心力衰竭(HFpEF),高达四分之一的患者出现(10%的患者报告严重心力衰竭,NYHA分级III/IV级)。胸痛,由微血管功能障碍引起(23%),偶尔由变时性功能不全引起,极少数由心外膜冠状动脉疾病引起(报告的心肌梗死发生率为2%)。心悸(15%-43%),最常见由心房心律失常引起(17%为心房颤动),也可由室性心律失常引起(8%为非持续性室性心动过速)。任何病因的晕厥,在男性中更常见(1.7%-5.6%),由窦房结功能障碍/严重传导障碍(高达30%)和心律失常引起。在无合并肾脏受累的情况下,高血压并不常见。在心肌病阶段,典型的心电图表现变得明显,如高电压和“劳损”图形(静息心电图上ST段压低和T波倒置,LVH的标志物)。6%-8%的患者进展为射血分数降低的心力衰竭,主要发生在未接受酶替代治疗(ERT)的患者中,且与死亡率增加相关。
04
传统上,LVH被认为是AFD最强的预后决定因素。LGE检测到的心肌纤维化也是这些患者心血管结局的公认预测因子,与LVH的存在具有独立价值,且其随时间的进展与室性心律失常的额外风险相关。在过去十年中,心脏成像的重要进展使人们对AFD心脏受累的病理生理学有了更好的理解,并为更准确的预后评估提供了新工具。
关于常规超声心动图,Meucci等人最近提出了AFD心脏受累的分期系统:0期:无心脏受累迹象;1期:左心室肥厚;2期:左心房扩大;3期:心室功能障碍(左心室射血分数<50%或平均E/E′≥15或TAPSE<17mm)。
在一项纳入314例AFD患者的多中心队列研究中,更晚期的心脏损伤与长期随访中心血管事件风险增加独立相关,且与单独评估LVH相比,显示出增量预后价值。二维或三维斑点追踪超声心动图可能提供附加信息,不仅有助于LVH发生前的早期诊断,还有助于优化患者的风险分层。有趣的是,最近一项在200例AFD患者中进行的CMR研究验证了一种基于三个变量预测5年不良心血管事件风险的模型:年龄、左心室质量指数和新型T1 mapping参数T1离散度(体素心肌T1弛豫时间的标准差)。然而,尽管从病理生理学角度来看具有吸引力,但T1离散度的应用可能耗时,且仍主要局限于研究领域。关于T2 mapping,LGE节段中T2值升高与肌钙蛋白升高和疾病进展相关,支持心肌炎症在AFD心脏受累病理生理学中发挥关键作用。基于这一证据,Nordin等人在182例患者的队列中提出并验证了一种基于CMR表现的AFD进展分期模型:1期:糖脂蓄积,始于儿童期,特征为T1进行性降低,无LVH或LGE;2期:炎症和/或心肌细胞肥厚,出现LVH(男性更显著),T2升高,基底段下侧壁出现LGE(有时先于LVH,尤其是在女性中);3期:纤维化和/或功能障碍,T1值假性正常化,基底段下侧壁变薄,LGE进展至其他左心室节段。
05
超声心动图
超声心动图是监测AFD心肌病的一线成像方式,建议成人每年进行一次,青少年每两年进行一次。共识文件提供了疾病特异性治疗启动的指征,主要基于疾病变异型(经典型/晚发型)和性别。重要的是,在存在LVH(定义为左心室壁厚度>12mm)或LGE显示心肌纤维化的情况下,建议启动治疗,无论疾病形式和性别如何。相反,当前指南未考虑心脏受累的肥厚前期迹象(即T1降低或左心室GLS受损),这些病例的决策需要个体化。ERT后左心室壁厚度的变化存在差异。大多数研究表明,经过数年治疗后,左心室质量基本保持不变,但在男性和老年患者中可能增加,在女性患者中可能降低。尽管如此,在具有特定基因型的患者和基线左心室质量指数升高的患者中,已证实治疗后左心室质量降低。此外,米加司他治疗后左心室质量也显示降低。标准多普勒技术评估的舒张功能在ERT治疗12个月后基本保持不变或略有改善。E/E′比值(比二尖瓣血流E/A比值更敏感)可能显示ERT治疗后舒张充盈压改善。斑点追踪应变测量可能提示AFD心肌病的进展,并指示ERT治疗的必要性。在CMR无LGE的患者中,AFD患者降低的斑点追踪应变和应变率测量可能随着ERT治疗而改善。斑点追踪超声心动图测量的左心房应变可能随着ERT治疗而改善,并与左心房容积指数降低相关。
心脏磁共振(CMR)
多参数CMR在AFD治疗反应监测中已占据关键地位。事实上,CMR能够更准确和可重复地量化LVH,并且最重要的是,能够深入了解心肌病理,允许无创评估糖脂蓄积和其他疾病过程(包括炎症和纤维化)。大量心肌纤维化、炎症以及主要的甘露糖-6-磷酸受体下调可能导致ERT抵抗。在疾病非常晚期阶段,ERT给药的适宜性可能存在重大担忧。多项CMR研究报道,在有LVH且无或仅有少量LGE的AFD患者中,启动ERT后左心室质量降低。相反,LGE广泛的患者在治疗启动后,尽管LVH无变化,但LGE稳定或增加。此外,在最近的一项多中心研究中,20例新治疗患者(58%为男性,60%有LVH)接受ERT治疗1年后,T1降低减轻,左心室壁厚度降低。相反,在疾病更晚期且治疗稳定的AFD患者中(ERT中位持续时间为4.2年),尽管LVH、T1或LGE定量无变化,但1年内LGE节段的T2升高,同时肌钙蛋白水平升高和左心室GLS恶化。综上所述,这些结果支持在及时启动ERT时,其在减少心肌脂质负荷和心脏重构进展方面的有效性。另一方面,关于分子伴侣治疗心脏反应的CMR数据有限。特别是,米加司他治疗与左心室质量稳定相关,且在最近的一项小样本研究中,与T1降低改善的趋势相关,这在疾病早期患者中更为明显。
心脏核成像
AFD中ERT的主要目标之一是减少心脏组织中Gb3的蓄积。心脏核医学(SPECT或PET扫描)可用于检测和量化疾病特异性治疗的疗效。鉴于SPECT和PET能够提供关于冠状动脉微血管功能障碍、急性和慢性炎症以及心脏交感神经支配的信息,需要进一步的研究来评估这些方法是否可能在AFD的监测和治疗中具有临床应用价值。有趣的是,ERT似乎不影响冠状动脉微血管功能障碍。特别是,Kalliokoski等人的初步结果表明,尽管血浆Gb3浓度显著降低且患者症状改善,但12个月的ERT并未改善心肌灌注储备。越来越多的证据表明,炎症通路不仅在具有成熟纤维化的AFD心肌中积极参与,而且在疾病早期阶段也在全身水平参与。在这方面,心脏同时进行F-FDG-PET和CMR可能允许区分真正的瘢痕与伴随活动性炎症的纤维化。Nappi等人研究了系列心脏F-FDG-PET-MRI在AFD中的作用,以及成像结果与评估疾病稳定性的FASTEX评分的潜在关系。尽管纳入的患者数量有限,但该研究支持以下假设:在基线无心脏纤维化时启动ERT的患者,疾病进展更慢,突显了在疾病过程早期启动ERT可能获得更大治疗益处的潜力。需要进一步的研究来证实这一点。
06
多模态心脏成像在AFD的诊断和管理中发挥关键作用,尤其是在评估心脏受累的存在和严重程度方面。近年来,先进成像技术的快速发展极大地促进了对AFD心脏受累病理生理学的理解,强调了心肌缺血和炎症作为导致心脏损伤的额外机制的重要性。此外,CMR的系统应用使得能够识别在明显心脏肥厚之前出现的早期心脏受累的新标志物。另一方面,心脏受累的标准化分期仍然缺乏。最近的研究提出了基于超声心动图分期的预后分层,而基于临床、心电图和多模态成像结果的多参数分期最近已被提出,但尚未在大型队列中验证。在这方面,AFD患者心脏性猝死风险的预后分层仍然是一个重大挑战,因为肌节性肥厚型心肌病的风险模型未针对基因型模拟疾病和表型模拟疾病进行验证,且迄今为止尚未确定可靠的AFD特异性心律失常风险因素。同样,监测心脏损伤进展和AFD特异性治疗的疗效仍然具有挑战性。AFD的罕见性及其与遗传和表观遗传因素相关的异质性,以及男性和女性疾病进展的不同模式,使得难以确定定义心脏损伤进展、稳定甚至逆转的成像标准。采用标准化多模态方法的心脏成像研究网络对于收集更大规模和更均一的人群以及识别疾病进展和治疗反应的成像生物标志物至关重要。此外,人工智能在心电图和成像分析中的应用可进一步有助于改善早期诊断,并识别监测心脏受累和定义预后的生物标志物。人工智能应用于其他心肌病的心电图和CMR的初步经验显示出良好前景。
07
AFD的心脏受累以贮积性心肌病为特征,可能进展为肥厚型/限制性心肌病,导致左心室舒张功能障碍和心力衰竭。存在多种典型成像表现(表1),可辅助FC的诊断,所有成像方式均可能在其中发挥重要作用。此外,超声心动图、CMR和核成像可作为指导治疗选择和监测这些患者治疗反应的工具。本临床共识声明为临床医生提供了多模态成像联合应用的指征,以改善AFD的管理。
参考文献:
Cameli M, Pieroni M, Pastore MC, Brucato A, Castelletti S, Crotti L, Dweck M, Frustaci A, Gimelli A, Klingel K, Kuchynka P, Kuusisto J, Lazaros G, Mandoli GE, Merlo M, Moon J, Muraru D, Pantazis A, Rigopoulos AG, Ristic A, Elif Sade L, Sheppard MN, Tschöpe C, Petersen SE, Imazio M, Bohbot Y, Cikes M, Garg P, Keenan N, Petrescu A, Stankovic I, Szabo L, Uusitalo V. The role of cardiovascular multimodality imaging in the evaluation of Anderson-Fabry disease: from early diagnosis to therapy monitoring. Eur Heart J Cardiovasc Imaging. 2025 Apr 30;26(5):814-829. doi: 10.1093/ehjci/jeaf038.
· END ·
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系

发表留言
暂无留言
输入您的留言参与专家互动