冠脉介入治疗中钙化结节的识别和处理策略
钙化结节(Calcified Nodules, CNs)是冠状动脉粥样硬化病变中一种特殊且具有挑战性的类型,形态学特征复杂,介入治疗反应的差异性大,支架失败(如支架贴壁不良或再突出)率高,成为目前经皮冠状动脉介入治疗(PCI)中的常见难题。
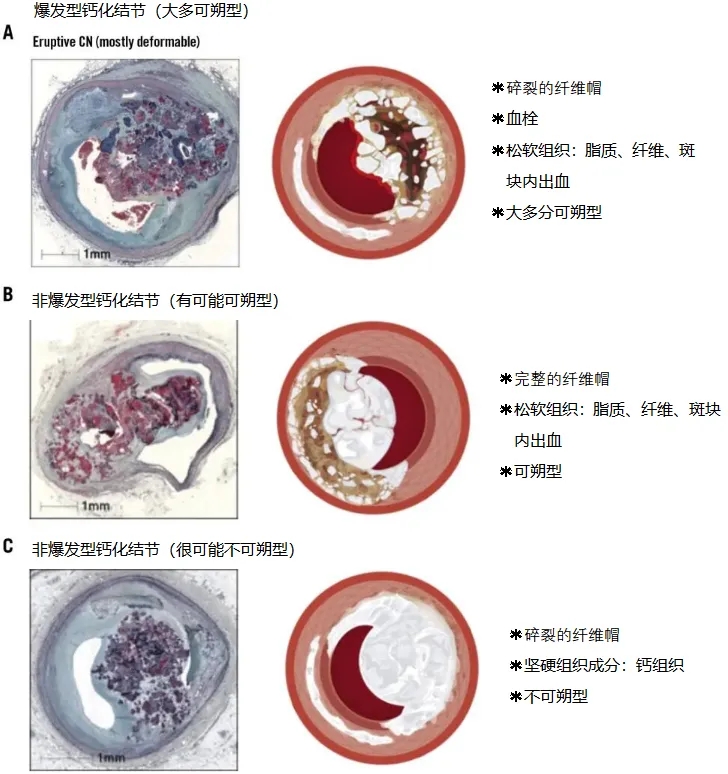
图1.钙化结节的分类、特点和可朔性。钙化结节分为2类:爆发型结节(A);非爆发型结节(B,C)。根据结节的成分,非爆发型结节可能可朔型或不可朔型。 CN: 钙化结节(calcified nodule)(DOI: 10.4244/EIJ-D-25-00296)
定义与分类
钙化结节(CN)是指突出于管腔、表面呈凸形的钙化病变,常伴有邻近节段的板状钙化。分两种亚型——爆发型钙化结节(Eruptive CN)与非爆发型钙化结节/结节状钙化(Non-eruptive CN / Nodular Calcification)。
爆发型钙化结节生物学上活跃,纤维帽破裂,表面有血栓覆盖,与斑块内出血相关。常见于急性冠脉综合征(ACS),多位于冠脉铰链点(如图2右冠中段)。在组织学上被认为是“真正的”CN。
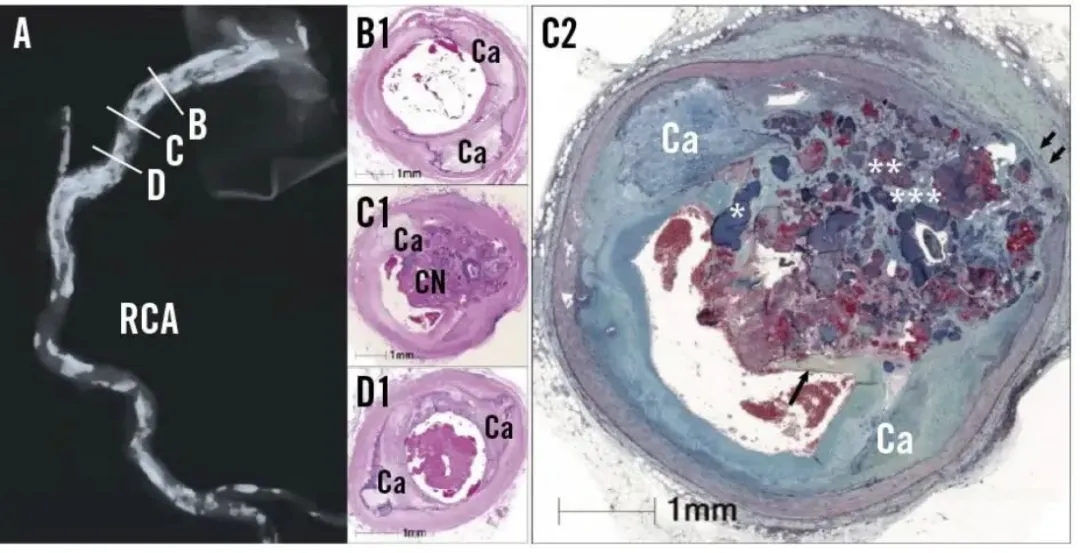
图2.右冠状动脉钙化和爆发性钙化结节(eruptive CNs)的组织学特征。A.右冠状动脉(RCA)的CTA影像,显示广泛钙化,B–D 采用苏木精-伊红(H&E)染色的横断面;B1. 位于放射影像所示典型铰链点; C1. 位于该铰链点处的爆发型钙化结节;C2. 爆发型钙化结节(CN)的 Movat’s 五色染色切片:可见片状钙化围绕爆发性结节,结节内包含致密钙化(*)、伴潜在钙化脂质的纤维蛋白(**)以及黏多糖基质(***),可见纤维帽肩部(箭头),其旁邻近有附着于爆发部位表面的血栓,铰链运动还导致了血管中膜的破坏(双箭头);D1. 远端的片状钙化。
非爆发型钙化结节/ 结节状钙化的纤维帽完整,结构稳定,通常表现为慢性冠脉综合征或无症状。可能是爆发型CN愈合后的表现。
流行病学特点
尸检研究表明,斑块破裂和斑块侵蚀是导致急性冠状动脉血栓形成并引发心源性猝死的最常见原因,而爆发型CN 是最少见的原因。在急性冠脉综合征(ACS)患者的临床研究中也观察到了类似的模式。麻省总医院(MGH)的 OCT 注册研究对 126 名接受术前 OCT 成像的 ACS 患者进行了分析,结果显示斑块破裂、斑块侵蚀和 CN 的发生率分别为 43.7%、 31.0% 和 7.9%。近期,TACTICS 注册研究同样证实,与斑块破裂(59.1%)和侵蚀(25.6%)相比,CN 是 ACS 最不常见的原因(4.0%)。这些发现与其他研究一致,即 ACS 患者中 CN 的患病率约在 2% 至 8% 之间。
然而,近期的研究表明,在常规临床实践中,CN 的普遍程度比预期的更高。在 PROSPECT 子研究中,利用三支血管 IVUS 评估非罪犯病变时发现,17% 的可分析血管和 30% 的患者中存在 CN。研究发现 CN 在钙化病变中尤为常见:一项研究显示,ACS 患者中约三分之一的严重钙化罪犯病变归因于 CN。此外,在接受旋磨术(RA)治疗的钙化病变中,腔内影像学识别出的 CN 比例高达 50%。这些发现提醒术者,在遇到严重钙化的冠状动脉病变时,必须考虑 CN 存在的可能性。
研究还发现,糖尿病、既往接受过搭桥手术(CABG)或正在进行血液透析的患者中,CN 的患病率更高。值得注意的是,在伴有慢性肾脏病(CKD)的 ACS 患者中,约 40% 的罪犯病变为 CN。最近一项利用连续 OCT 观察 CN 自然史的纵向研究证实,新发 CN 的形成与血液透析密切相关。此外,较大的钙化负荷伴随残留脂质斑块、左主干分叉部位,以及病变处较大的造影角变化——这反映了血管旋转扭力的增加,常见于右冠状动脉中段——均与 CN 的形成相关,这些发现为其病理生理机制提供了重要线索。
慢性肾病、长期透析患者(约40% ACS罪犯病变)、糖尿病、既往搭桥术后、高钙负荷、左主干分叉、冠脉铰链运动大(Δ角度大)等因素与CN形成相关。这些是钙化结节病变容易形成的高危因素。
病理生理机制
爆发型CN: 坏死核心内的无胶原钙化易受机械应力(如冠脉铰链运动,hinge motion)影响而碎裂。碎裂的钙质突破纤维帽,导致内皮损伤、血小板聚集和血栓形成,引发ACS。斑块内新生血管破裂引起反复出血和纤维蛋白沉积,促进钙化进展。
非爆发型CN: 可能为爆发型CN愈合后形成,血液成分经历成骨转化,小钙化融合为大块钙化。钙化逐渐替代脂质核心,趋于稳定。
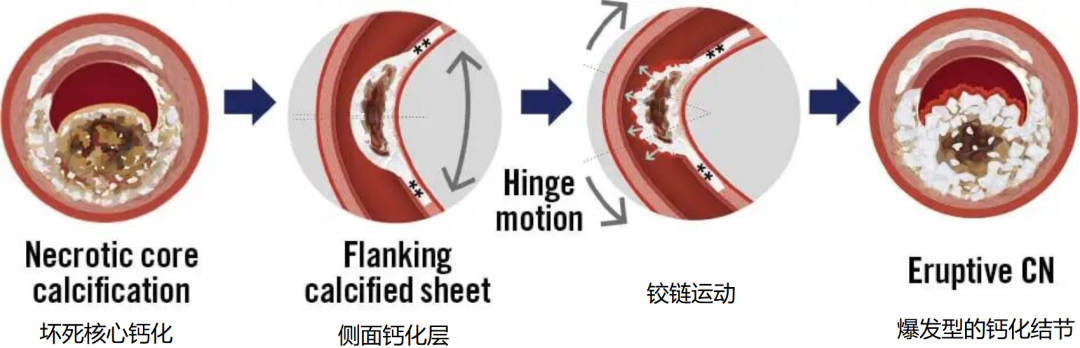
图3.钙化和运动对钙化的影响
CN 内部的血管生成也可能促进其演变。研究中频繁观察到不同时期的纤维蛋白沉积,这表明存在反复的毛细血管损伤或渗漏(图 1)。这种毛细血管破裂和纤维蛋白沉积的循环过程可能驱动了结节状钙化的逐渐生长和挤出,最终导致其突入管腔。细小的钙化结节碎片会破坏上层纤维帽和内皮层,触发血小板聚集和纤维蛋白沉积,从而促进管腔内血栓形成。毛细血管破裂引起的斑块内出血以及表面血栓的形成,最终可能导致管腔急性狭窄和 ACS 的发作。
关于非爆发型CN(结节状钙化)的发育机制虽然尚不明确,但一种假设认为它可能是爆发型 CN 的愈合形式。爆发型 CN 内部的斑块内出血可能通过血液成分的成骨转化而消退,将细小的钙化碎片整合为一个较大的钙化团块,并伴有受损纤维帽的愈合。组织学发现支持了这一点:钙化针状物之间经常可见纤维蛋白,以及破骨细胞和炎症细胞。此外,钙化可能向坏死核心和残留脂质斑块内进展,随着 CN 的成熟逐渐减少其体积。因此有假设认为,非爆发型 CN 可能伴随偏软(脂质/纤维蛋白)或偏硬(钙化)的成分(图 1,图),这可能导致临床上不同的治疗反应,特别是表现在“可变形”与“不可变形”CN 的区别上。
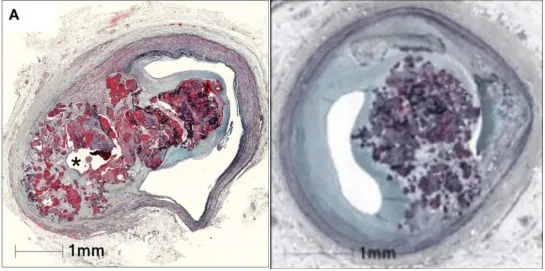
图4.非爆发型CN的组织学表现。非爆发型CN(或称结节状钙化)始终局限在血管内膜之内,没有管腔表面的破损或血栓形成。它们可能伴随以下成分:(A) 柔软成分(黑星号 ):包括坏死核心、黏多糖基质和纤维蛋白沉积。(B) 坚硬成分(兰星号):如坚硬的钙化斑块。这些成分上的差异可能会影响非爆发型CN 的可变形性。
Sugizaki等人近期的一项临床研究进一步支持了这些假设。在该自然史研究中,研究者对未治疗的钙化病变进行随访,并通过重复 OCT 检查观察其演变过程。结果发现,新发钙结节(de novo CNs)的形成与衰减型钙化(attenuated calcium)的存在密切相关,提示其内部可能仍残留脂质性成分。这一发现与组织学证据一致,即 CN 更可能起源于坏死核心钙化,而非富含胶原蛋白的钙化。此外,收缩期和舒张期之间较大的造影血管角度变化与新发 CN 的形成相关,再次强化了铰链运动产生的机械力在其发展中的作用。
识别与评估方法
血管造影(Angiography)
如果有“放射性透亮缺损”,提示可能存在CN。 但易高估狭窄程度,且部分CN无典型表现。增强技术(如StentBoost、ClearStent)可提高检出率。
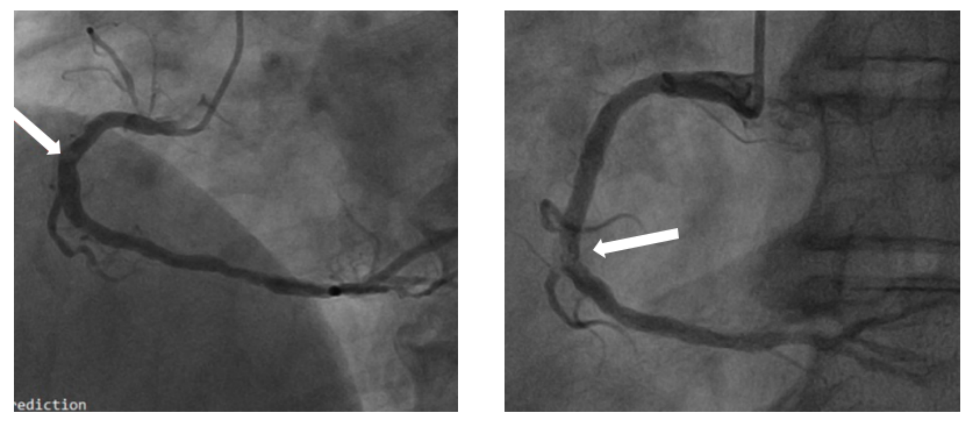
图5.冠状动脉造影的钙化识别和特征。注:白色箭头指示充盈缺损,后腔内影像学证实为钙化结节。
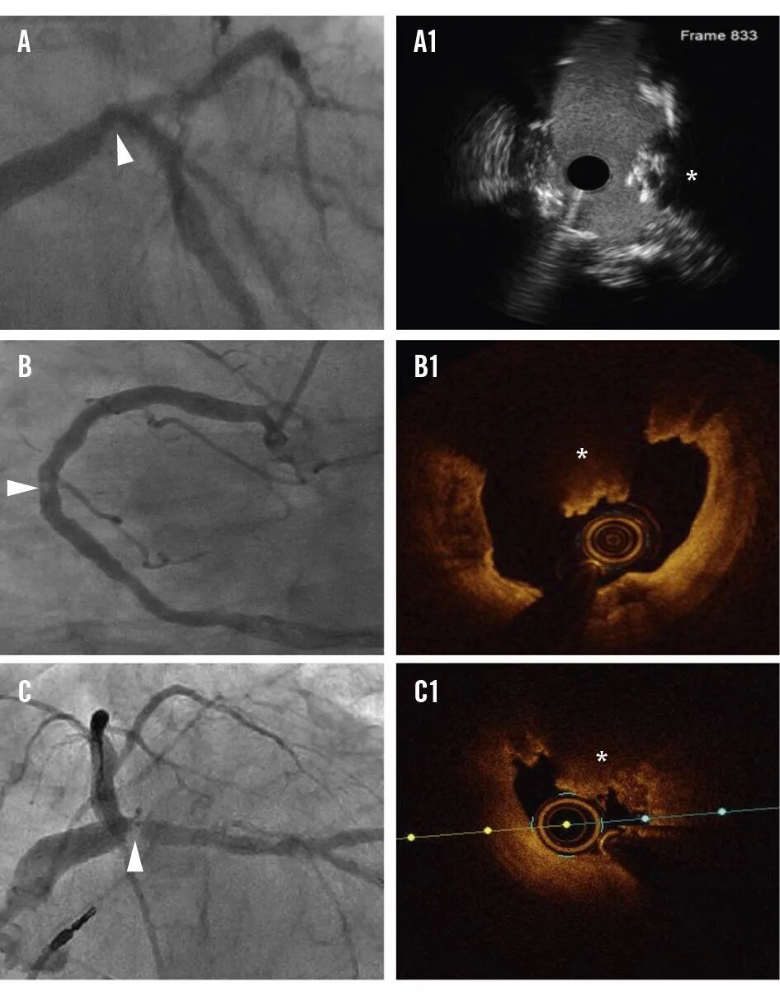
图6.钙化结节的冠状动脉造影特征。冠状动脉造影特征,CNs呈透亮区(白色箭头)。IVUS (A1)和OCT (B1,C1)证实钙化结节。CN:钙化结节(calcified nodule)。
血管内超声(IVUS)
普通IVUS可见强回声伴声影,高分辨率IVUS(HD-IVUS)可判断纤维帽是否连续,区分爆发型(破裂)与非爆发型(完整)。
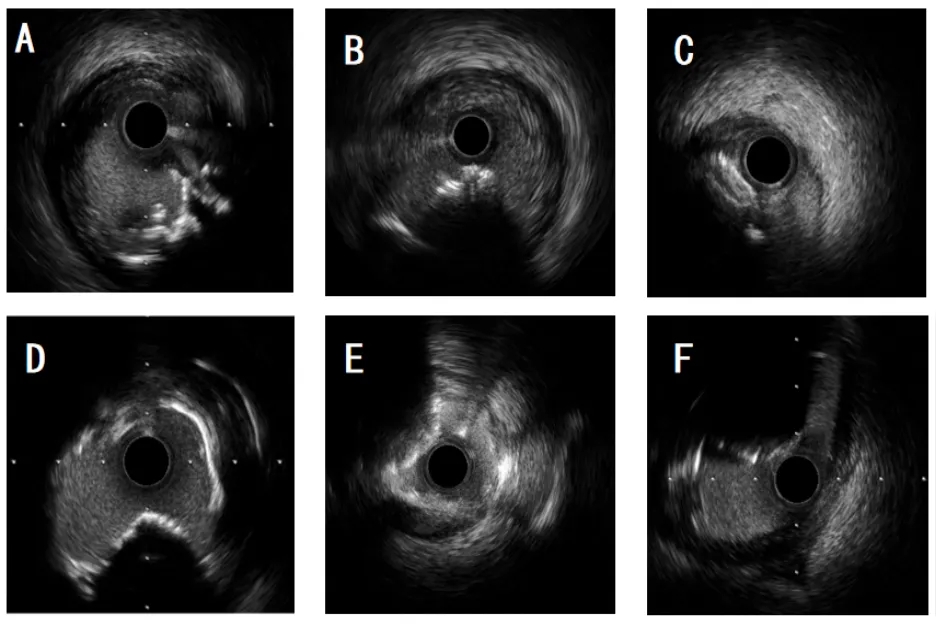
图7.IVUS可显示和区别不同类型的钙化病变。A和B为爆发型钙化结节,在IVUS上表现为凸入管腔的不规则簇状钙化团块,表面不规则,常伴强后方声影和可能血栓低回声信号。C-F为各种形态的非爆发型钙化结节,在IVUS上表现为凸入管腔的团块状或盘状钙化,表面相对光滑、纤维帽较完整,后方伴声影但无明显簇状不规则结构。(IVUS设备:Boston Scientific OptiCross HD 60MHz)
光学相干断层成像
光学相干断层扫描(OCT)是诊断CN的金标准,分辨率高。爆发型CN表现为表面不规则、纤维帽破裂、血栓覆盖。非爆发型CN则表面光滑、纤维帽完整。
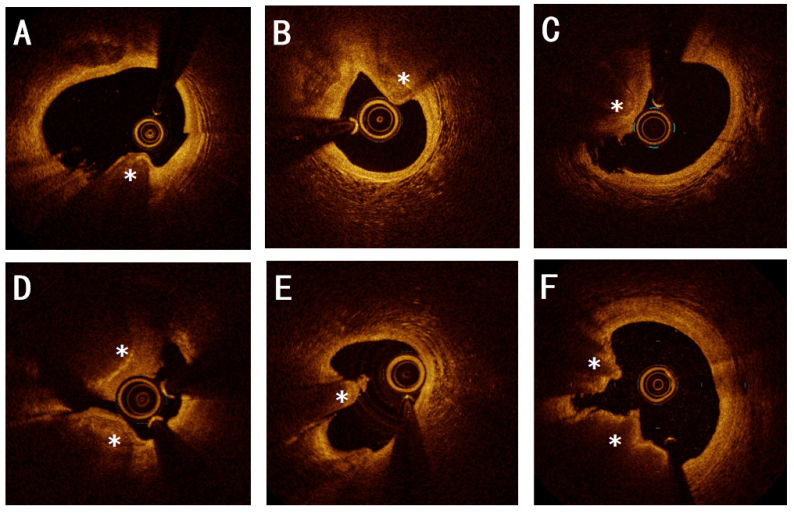
图8.OCT可显示和区别不同类型的钙化病变。A-D为各种形态的非爆发型钙化结节,在OCT上的表现为凸入管腔的钙化团块,表面相对光滑、覆盖完整纤维帽,无血栓附着,但伴强信号衰减。E-F为爆发型钙化结节,在OCT上OCT上表现为凸入管腔的不规则高背散射钙化团块,表面不规则、纤维帽破裂,常伴有附壁血栓和强信号衰减。(OCT设备:Abbott Dragonfly OpStar™ )
治疗策略
①球囊预处理:首选初始策略使用非顺应性(NC)或切割/刻痕球囊进行高压扩张评估可变形性,若在两个正交体位均实现充分球囊扩张,提示CN可变形,可能无需进一步处理。局限性在于易发生偏心扩张,导致夹层;对重度钙化效果有限。
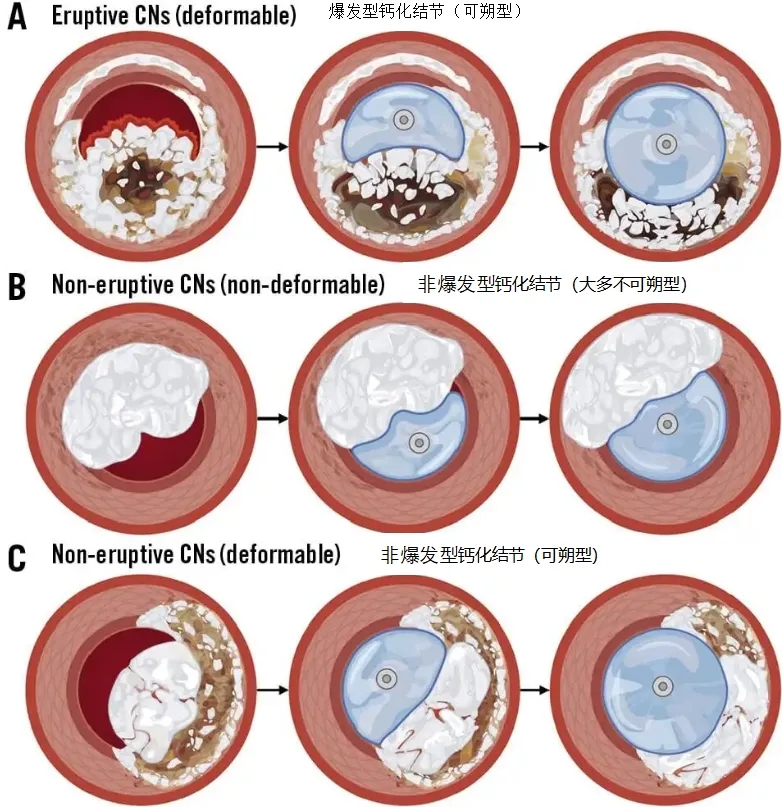
图9.钙化结节和可朔性。
②斑块旋磨术:适用于重度钙化。但存在“导丝偏倚”(guidewire bias),即旋磨头偏向导丝一侧,难以有效处理偏心性CN。研究未显示其能显著降低靶血管重建率。
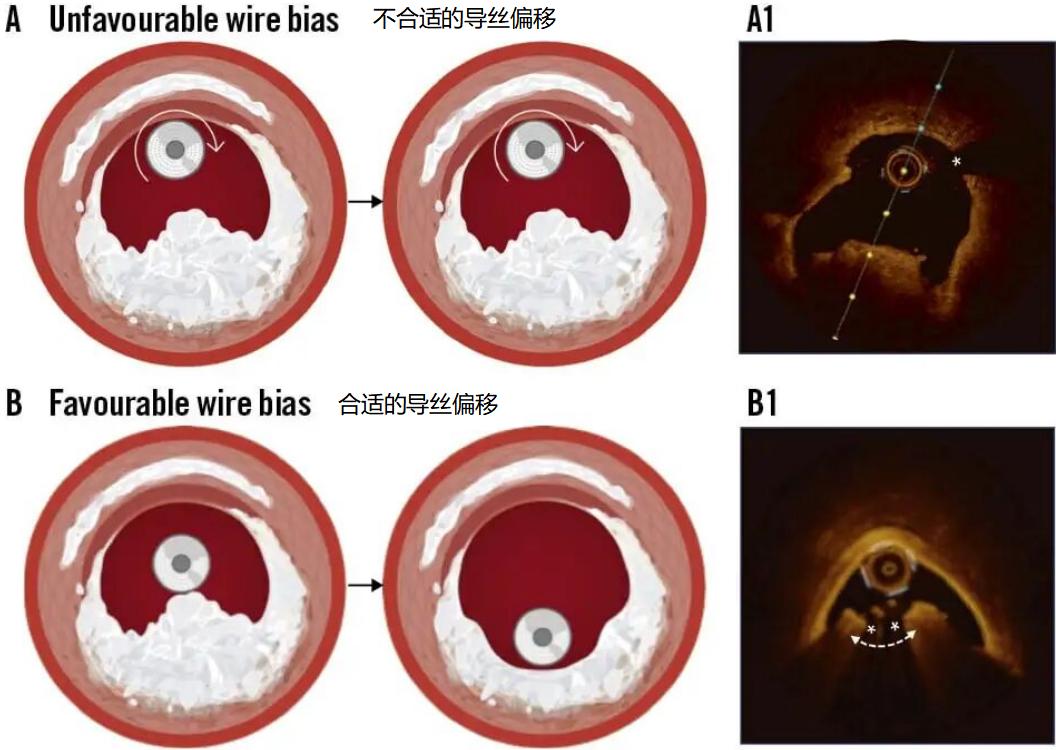
图10.旋磨导丝在管腔的位置对旋磨的影响。
③轨道旋磨:理论上更少受导丝偏倚影响,效果与管腔大小相关。基线管腔面积≤2.5 mm²可显著减小CN体积(38.8%),>2.5 mm²则效果有限(仅16.8%)。建议结合OCT评估选择合适病例。
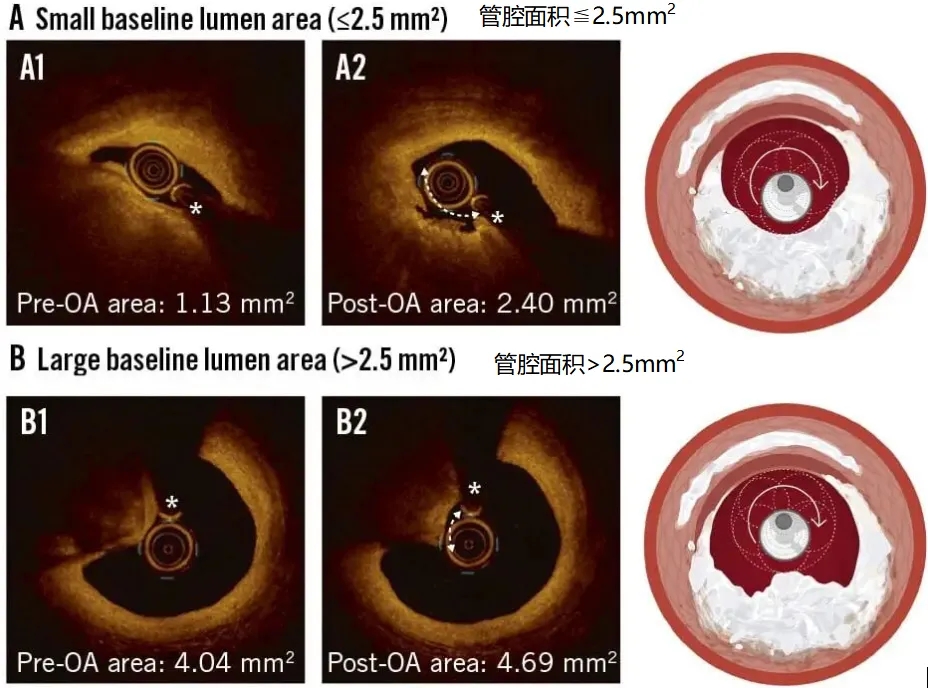
图11.管腔面积和轨道旋磨。
④血管内冲击波碎石术:当前首选技术之一,通过声压波选择性断裂钙化,不受导丝偏倚或管腔大小限制。可同时处理CN及邻近板状钙化,实现整体钙化修饰。Disrupt CAD研究显示其用于含CN的严重钙化病变安全有效。约1/3非碎裂型CN仍不可变形,可能导致支架偏心扩张。
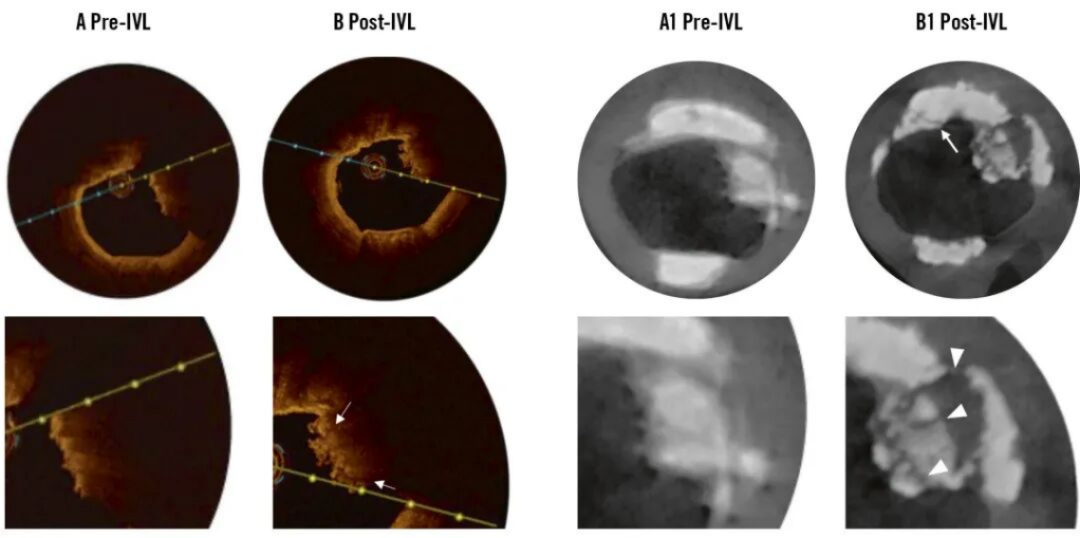
图12.血管内冲击波碎石术前后对比。
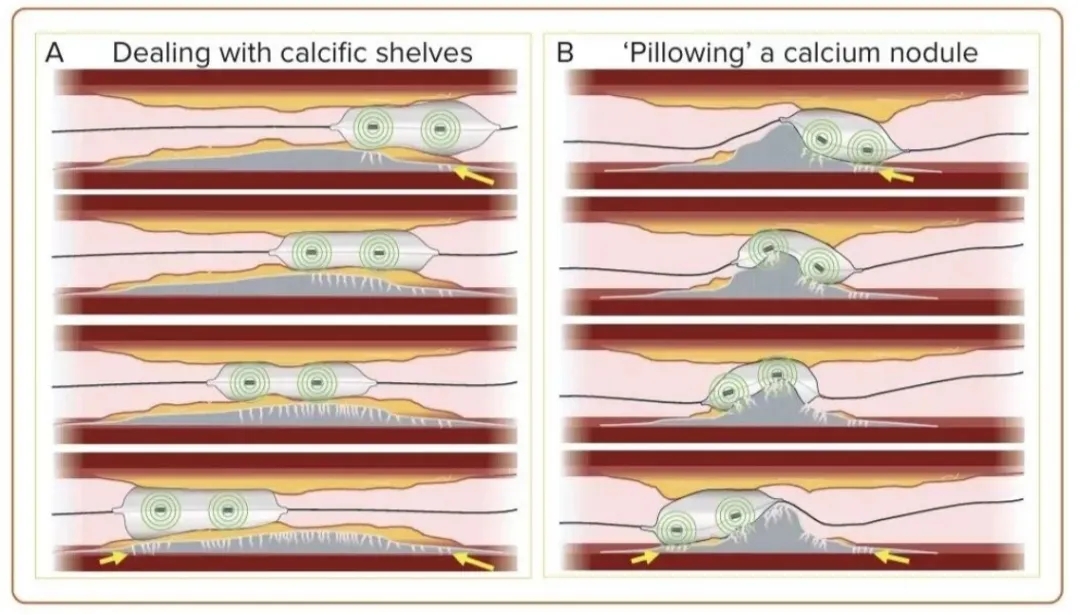
图13.血管内冲击波碎石术对钙化病变的枕头效应。A.处理钙化层:用碎石球囊逐渐增压回撤,在厚薄交界区容易发生钙化结节碎裂;B.钙化结节的枕头效应:在钙化结节处低压扩张,产生枕头样效应,对钙化结节的基底层厚薄区产生最大碎裂效应。
⑤联合策略:理论上有协同作用,先用旋磨/OA去除部分CN体积,再用IVL进行广泛钙化断裂,尚需临床研究验证其优势。
推荐治疗流程
①术前评估:造影怀疑钙化结节→ 使用OCT或HD-IVUS明确诊断并分型。
②初始处理:使用1:1 NC/专用球囊进行高压预扩张,评估可变形性。
③决策路径:若球囊充分扩张→ 可继续支架植入。若球囊未充分扩张(提示不可变形)→ 启用高级斑块修饰技术(震波球囊IVL为首选,或根据情况选择旋切或旋磨OA/RA)。
④支架植入后:建议用OCT评估支架贴壁、膨胀及有无钙化结节再突出。
未来方向
冠状动脉CTA有望提前评估CN形态、密度及脂质残留,预测可变形性。多模态融合成像,如OCT-NIRS、IVUS-NIRS,用于检测CN周围残余脂质成分。药物涂层球囊(DCB)的探索,理论优势是避免支架相关并发症(断裂、再突出),挑战是CN本身易发生弹性回缩和再生,需充分预处理后方可考虑。新型器械开发可更精准的钙化修饰工具。
钙化结节(CN)是PCI中高风险的特殊病变,需引起高度重视。爆发型CN虽易压缩但远期再狭窄率高;非爆发型CN部分不可压缩,影响支架贴壁腔内影像(OCT/IVUS)是识别和分型的关键,指导个体化治疗。IVL已成为主流预处理手段,但部分病例仍需联合策略。未来需更多研究优化治疗路径,改善CN患者的长期预后。
参考文献
[1] Riley RF, Patel MP, Abbott JD, et al. SCAI Expert Consensus Statement on the Management of Calcified Coronary Lesions. J Soc Cardiovasc Angiogr Interv. 2024;3(2):101259. Published 2024 Jan 31. doi:10.1016/j.jscai.2023.101259
[2] Ali ZA, Spratt JC, Finn AV, Maehara A, Shin D. Identification and treatment of calcified nodules in percutaneous coronary intervention. EuroIntervention. 2025;21(23):e1424 -e1433. Published 2025 Dec 1. doi:10.4244/EIJ-D-25-00296
[3] Galougahi KK, Shin D, Dakroub A, et al. Distinct Challenges of Eruptive and Non-Eruptive Calcified Nodules in Percutaneous Coronary Intervention. Curr Cardiol Rep. 2024;26(7):757-765. doi:10.1007/s11886-024-02075-w
· END ·
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系

发表留言
暂无留言
输入您的留言参与专家互动