低危患者经导管与外科主动脉瓣置换术的7年随访比较
经导管主动脉瓣置换术(TAVR)已越来越多地被用作手术治疗严重症状性主动脉瓣狭窄患者的替代方案。随机试验表明,在低、中、高手术风险患者中,TAVR在长达5年的随访期内优于或与外科主动脉瓣置换术相似。如前所述,主动脉瓣经导管瓣膜置入术(PARTNER)3试验显示,在较年轻的低危患者中,TAVR术后1年、2年和5年的死亡、卒中或再住院发生率(主要复合终点)低于或与手术治疗无差异。主动脉瓣植入术后晚期生物瓣膜失效仍是终身患者护理决策中的重要考虑因素。在此,我们描述了PARTNER 3试验的7年临床和超声心动图结果。
研究内容
共有1000例患者在71个临床中心接受随机分组;503例患者被分配接受经股动脉TAVR治疗,497例患者被分配接受外科手术治疗。实际治疗人群包括TAVR组496例患者和手术组454例患者;分别有495例和453例患者接受了预定的瓣膜。植入瓣膜尺寸和外科瓣膜类型的信息此前已发表。。患者的平均年龄为73岁,69.3%为男性,平均STS-PROM评分为1.9%。主要终点可在89.6%的患者中于7年时进行评估(TAVR组为92.7%,手术组为86.1%);在随访最初几年中,手术组出现较多患者退出试验的情况。通过对生存状态的全面追踪,在137例失访或退出试验的患者中确定了84例的生存状态(TAVR组28例,手术组56例)。因此,TAVR组496例患者中有471例(95.0%)确定了生存状态,手术组454例患者中有426例(93.8%)确定了生存状态。
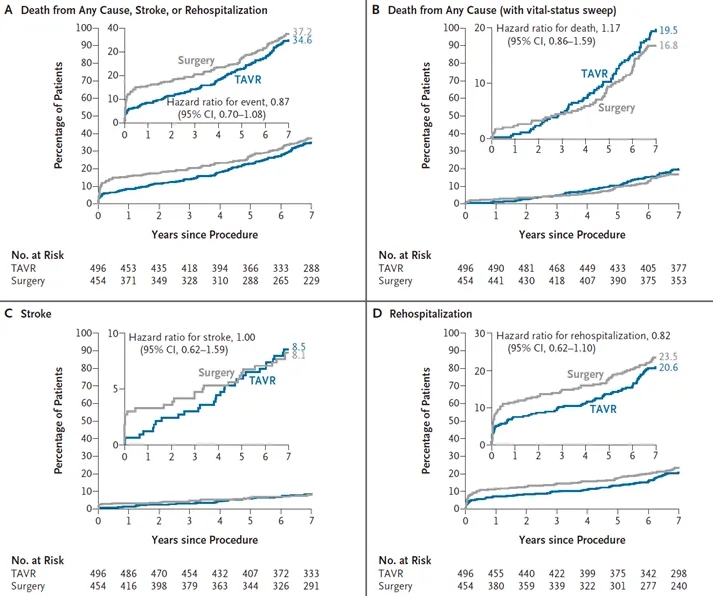
图1. 第一主要终点及其组成部分的Kaplan-Meier曲线
图A显示全因死亡、卒中或与手术、瓣膜或心力衰竭相关的再住院(第一复合主要终点)的Kaplan-Meier估计值;这些数据不包括生存状态全面追踪获得的数据。图B、C和D显示该终点各组成部分的估计值。根据统计分析计划,对复合主要终点的预设分析采用Wald检验计算经导管主动脉瓣置换术(TAVR)与外科手术之间Kaplan-Meier估计值的差异(差异,-2.61%;95% CI,-8.95%至3.74%)。为提供最完整的随访数据,单独对死亡的分析包括生存状态全面追踪获得的数据。其他细节见补充附录表S3。由于死亡组成部分存在随时间风险非比例性的证据,同时评估了比值比,结果为1.20(95% CI,0.86至1.67)。每幅图的插图显示y轴放大后的相同数据。所有分析均在实际治疗人群中进行,包括接受随机分组并开始接受索引手术的患者。
从基线至7年期间,TAVR组496例患者中有165例(Kaplan-Meier估计值34.6%)、手术组454例患者中有156例(Kaplan-Meier估计值37.2%)发生了死亡、卒中或与手术、瓣膜或心力衰竭相关的再住院(第一主要终点)(差异,-2.6个百分点;95%置信区间[CI],-9.0至3.7;风险比,0.87;95% CI,0.70至1.08)(图1A和表1)。TAVR组和手术组第一主要终点各组成部分的7年Kaplan-Meier估计值分别为:全因死亡(包括生存状态全面追踪数据),19.5%和16.8%;卒中,8.5%和8.1%;再住院,20.6%和23.5%(图1B、1C、1D;表1)。表S4和图S4A、S4B提供了心血管死亡和非心血管死亡的详细信息。
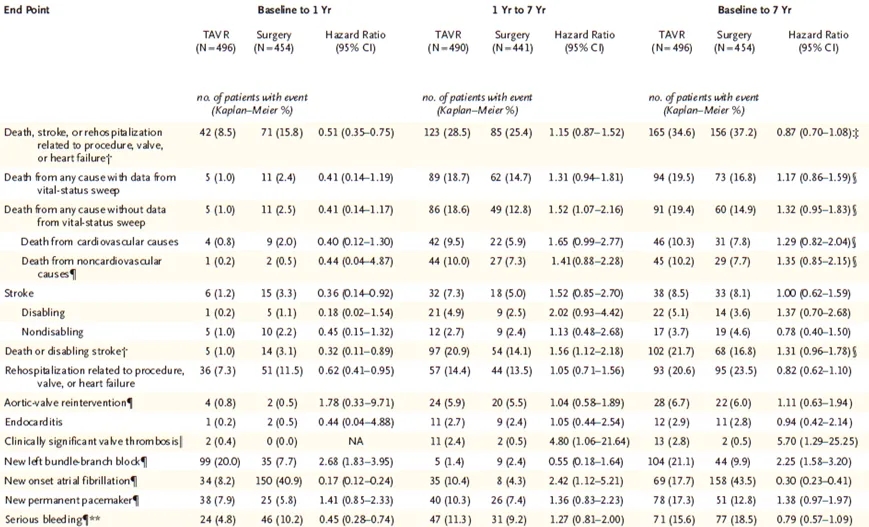
表1.关键临床终点
第一主要终点的结果在所有主要亚组中似乎保持一致(图S5)。在第1至7年的第一主要终点标志性分析中(计算时排除随访第一年的数据),TAVR组和手术组的Kaplan-Meier估计值分别为28.5%和25.4%(死亡、卒中或再住院的风险比,1.15;95% CI,0.87至1.52)(表1)。对第一主要终点7年内限制性平均无事件生存时间和限制性平均总生存时间的分析显示,TAVR较手术多134天无事件生存时间(95% CI,22至247)(图2A),但总生存时间少15天(95% CI,-78至48)(图2B)。第二主要终点的胜率比为1.04(95% CI,0.84至1.30)。
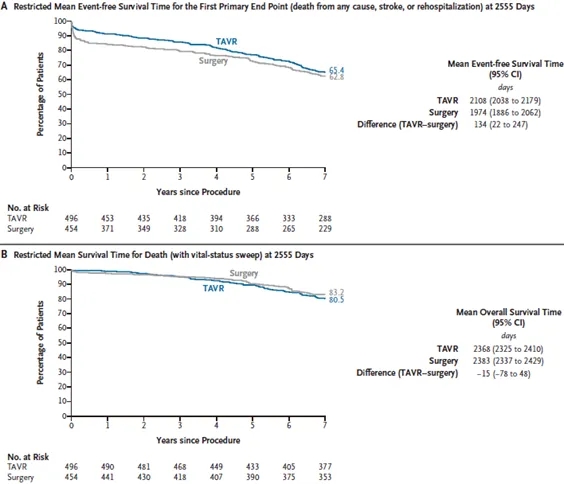
图2. 第一主要终点和全因死亡的限制性平均无事件生存时间
图A显示第一主要终点的限制性平均无事件生存时间,该终点为全因死亡、卒中或与手术、瓣膜或心力衰竭相关的再住院的复合终点;这些数据不包括生存状态全面追踪获得的数据。图B显示全因死亡的限制性平均生存时间,包括生存状态全面追踪获得的数据。两项分析中,无事件天数的定义均依据Gregson等人的方法。
从基线至7年,TAVR组和手术组患者主动脉瓣再次干预、心内膜炎、心肌梗死、严重出血和血运重建事件的Kaplan-Meier估计百分比似乎相似(表1)。新发房颤发生于TAVR组17.7%的患者和手术组43.5%的患者,新发永久性起搏器植入率分别为17.3%和12.8%(表1)。临床有意义的瓣膜血栓形成发生于TAVR组13例患者(2.8%)和手术组2例患者(0.5%)(表1)。在TAVR组13例瓣膜血栓形成患者中,10例存在2期或3期血流动力学瓣膜恶化,其中7例经抗凝治疗后缓解。无瓣膜血栓形成患者死亡。表S8和S10显示了5至7年期间死亡、卒中、心肌梗死、血运重建或新发房颤的患者数量。
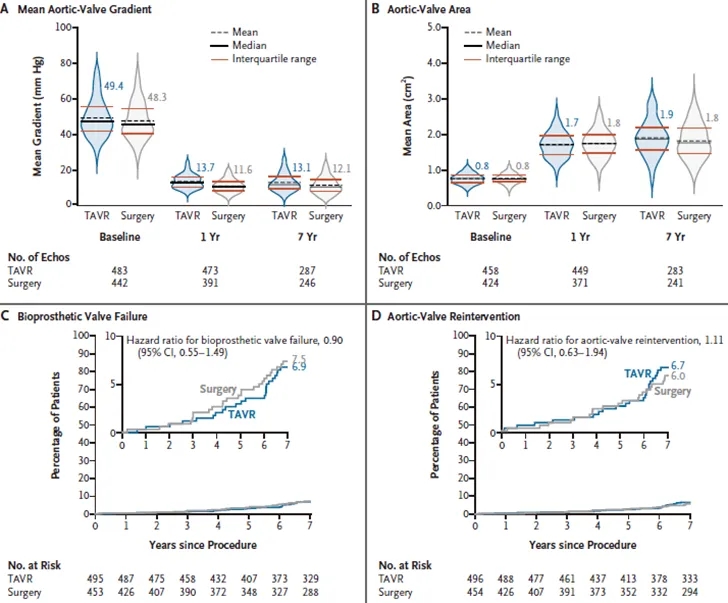
图3. 瓣膜血流动力学和耐久性
图A和图B分别显示核心实验室超声心动图评估的平均主动脉瓣跨瓣压差和平均主动脉瓣口面积。分析在瓣膜植入人群中进行,包括接受预定瓣膜的患者。瓣膜取出或接受瓣中瓣手术的患者数据在再次干预后删失。图C显示按照瓣膜学术研究联盟3(VARC-3)标准裁定的生物瓣膜失效累积发生率;生物瓣膜失效的风险比采用Fine-Gray方法估计,分析在瓣膜植入人群中进行。图D显示各中心报告的主动脉瓣再次干预的Kaplan-Meier估计值;分析在实际治疗人群中进行。图C和图D的插图显示y轴放大后的相同数据。
7年时,TAVR组平均主动脉瓣跨瓣压差为13.1±8.5 mm Hg,手术组为12.1±6.3 mm Hg;平均主动脉瓣口面积分别为1.9±0.6 cm²和1.8±0.5 cm²(图3A和3B)。配对平均压差和主动脉瓣口面积分析见图S12C和S12D。TAVR组17.7%的患者和手术组2.0%的患者存在轻度、中度或重度瓣周主动脉瓣反流。在TAVR组中,术后30天无或微量瓣周主动脉瓣反流的患者与术后30天轻度瓣周反流的患者7年死亡率相似(分别为18.7%和20.7%;风险比,0.89;95% CI,0.57至1.38)。
生物瓣膜失效的累积发生率在TAVR组为6.9%,手术组为7.5%(图3C)。TAVR组和手术组生物瓣膜失效各组成部分的结果分别为:不可逆3期血流动力学瓣膜恶化,1.7%和2.8%;瓣膜再次干预,4.7%和4.3%;瓣膜相关死亡,0.4%和0.5%(表1)。总体而言,手术组6.0%的患者和TAVR组6.7%的患者发生了主动脉瓣再次干预(风险比,1.11;95% CI,0.63至1.94)(图3D)。两组2期或3期结构性瓣膜恶化的发生率似乎相似。7年时,TAVR组73.4%的患者和手术组74.8%的患者存活且无生物瓣膜失效。
7年时,TAVR组72.9%的患者和手术组75.9%的患者存活且纽约心脏协会(NYHA)心功能分级为I级或II级。两组7年时的疾病特异性健康状况似乎相似,TAVR组患者平均KCCQ-OS评分为84.9,手术组为86.2。7年时,TAVR组395例患者中有233例(59.0%)、手术组332例患者中有210例(63.3%)存活且KCCQ-OS评分大于75;两组分别有65.5%和66.6%的患者存活且KCCQ-OS评分大于60,且较基线下降不超过10分。
在低危的严重症状性主动脉瓣狭窄患者中,接受TAVR与接受外科手术的患者在7年时涉及死亡、卒中和再住院的两个主要复合终点方面未观察到显著差异。
参考文献:
1.Leon MB, Mack MJ, Pibarot P, et al. Transcatheter or Surgical Aortic-Valve Replacement in Low-Risk Patients at 7 Years. N Engl J Med. 2026;394(8):773-783. doi:10.1056/NEJMoa2509766
· END ·
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系

发表留言
暂无留言
输入您的留言参与专家互动