文献分享 | 新型PannaWire导丝用于无辐射经皮介入房间隔缺损封堵术的随机对照试验
在先天性心脏病介入治疗中,单纯超声引导下的ASD封堵术虽具有无辐射、成本低等优势,但受限于传统导丝显影不足与稳定性欠佳等影响,直接制约了初级术者的操作效率与成功率。《Circulation: Cardiovascular Interventions》发表的一项多中心随机对照研究表明,PannaWire导丝可在显著提升超声下可视性的同时兼顾通过性与安全性。研究结果显示,初级医生使用该导丝手术成功率高达100%,并显著缩短进入左心房时间、降低心律失常及误导风险,提示其有助于优化学习曲线并推动无辐射介入技术的基层推广。

文章链接:
https://doi.org/10.1161/CIRCINTERVENTIONS.120.009281
摘要
背景
超声引导下的经皮介入手术已被证实可靠且具有优势。然而,对于初级医生而言,其学习曲线较为困难。本研究旨在评估一种新型导丝(PannaWire导丝)在单纯经胸超声心动图引导下经皮房间隔缺损封堵术中的安全性和有效性。
方法
Pannawire导丝适用于超声引导手术,梭形头端收放可调,满足探查与支撑不同需求。本研究开展了一项多中心随机对照试验,以评估PannaWire导丝与传统导丝在手术经验不足100例的初级医生使用时的安全性和有效性。主要结局指标为手术成功率。次要结局指标包括:主要不良事件发生率、手术时间、进入左心房所需时间、心律失常发作次数、误入三尖瓣次数以及外周血管并发症发生率。
结果
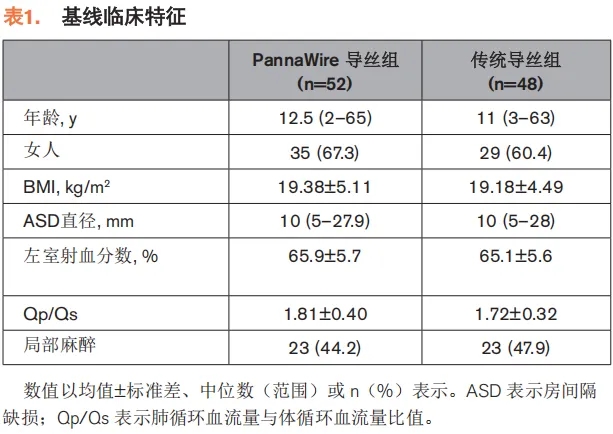
在2018年7月至2019年9月期间,来自3个中心的100例房间隔缺损患者被随机分配至PannaWire导丝组(n=52)或传统导丝组(n=48)。两组患者的基线临床特征分布相似。PannaWire导丝组的手术成功率(主要结局指标)为100%,而传统导丝组为68.75%(P<0.001)。两组均未发生主要不良事件。PannaWire导丝组在手术时间(P=0.004)、进入左心房所需时间(P<0.001)、心律失常发作次数(P<0.001)以及误入三尖瓣次数(P=0.005)方面均显著优于传统导丝组。
结论
PannaWire导丝安全有效,可降低单纯经胸超声心动图引导下经皮房间隔缺损封堵术的学习曲线。
1 引言
房间隔缺损(ASD)是一种常见的先天性心脏病,可通过外科手术或经导管封堵术进行治疗[1]。传统上,经皮房间隔缺损封堵术是在透视引导下进行的[2-4]。近年来,有报道称超声心动图引导经皮ASD封堵术安全可靠[5,6]。无辐射经皮介入(PAN)手术减少了对医疗设备的依赖,降低了医疗成本,并避免了透视和造影剂造成的医源性损伤。然而,由于超声成像与透视成像的成像机制不同,这项新技术的学习曲线较为困难。在透视下,三维心脏被投影到二维平面上,可以随时定位导丝和导管的头端。相比之下,超声心动图采用逐层平面扫描的方式,使得定位和调整导丝及导管头端的方向以通过ASD变得困难。超声伪影也可能对经验较少的术者产生误导。
PannaWire导丝是一种新型导丝,旨在改进无辐射经皮介入技术(PAN)手术。在本研究中,我们开展了一项多中心随机对照试验,以评估初级医生使用PannaWire导丝进行无辐射经皮介入房间隔缺损封堵术的安全性和有效性。
已知信息
-
超声心动图下引导经皮房间隔缺损封堵术已被证实安全且具有优势。
-
但对于初级医生而言,纯超声引导经皮介入手术的学习曲线较为困难。
本研究的新发现
-
PannaWire导丝可显著提高经胸超声心动图引导下经皮房间隔缺损封堵术的手术成功率,并降低学习曲线,从而有助于推广纯超声引导手术,惠及更多偏远地区的患者。
2 方法
研究设计
这项关于超声引导介入手术使用新型导丝的前瞻性、多中心、随机试验在三个中心进行(中国北京阜外医院;中国乌鲁木齐新疆维吾尔自治区人民医院;以及中国郑州河南省人民医院)。
患者
2018年7月至2019年9月期间,对3个中心所有因房间隔缺损就诊的患者进行入组筛选。符合条件的患者需满足以下标准(心脏参数由经胸超声心动图测定):年龄≥2岁;ASD直径≥5mm;中央型ASD伴右心容量负荷增加;缺损边缘与冠状静脉窦、上腔静脉及下腔静脉的距离均≥5mm;与房室瓣的距离≥7mm;房间隔直径>封堵器左房侧直径。
具备以下任一条件的患者被排除本研究:原发孔型或静脉窦型ASD;心内膜炎或出血性疾病;目标区域血栓或穿刺部位静脉血栓;因重度肺动脉高压导致的右向左分流;与ASD无关的重度心肌炎或瓣膜疾病;左心房或左心耳血栓;部分性或完全性肺静脉异位连接;筛选时或筛选前1个月内存在感染性疾病;部分性或完全性肺静脉异位引流。
肺循环血流量与体循环血流量比值的计算
肺循环血流量与体循环血流量比值(Qp/Qs)的计算基于经胸超声心动图,具体步骤如下[7]:测量右心室流出道和左心室流出道的收缩期速度时间积分,以及肺动脉和左心室流出道区域的最大收缩期内径;基于直径假定流出道区域为圆形,计算其面积;然后将流出道面积乘以速度时间积分,获得每搏输出量;最后,用右心室每搏输出量除以左心室每搏输出量,得出肺循环血流量与体循环血流量比值。
PannaWire导丝设计
如图1所示,PannaWire导丝的头端呈梭形,由镍钛合金制成,可收入至5F或6F导管内。该导丝头端因其独特的梭形形状及较宽的直径(图2)而易于在超声下被识别。选择直径大于ASD直径的导丝,可防止导丝及输送系统滑回右心房。此外,镍钛合金网在遇到阻力时可通过形变来避免组织损伤。

图1. PannaWire导丝
A、导丝整体外观,示梭形头端。B、导丝体部由柔性转向段和加硬支撑段组成。C–E、导丝可收入至MPA2导管内。F、导丝位于输送鞘管内。G、导丝头端不能被收入扩张器内。H和I、导丝头端可收回至鞘管内。MPA2为多功能导管。
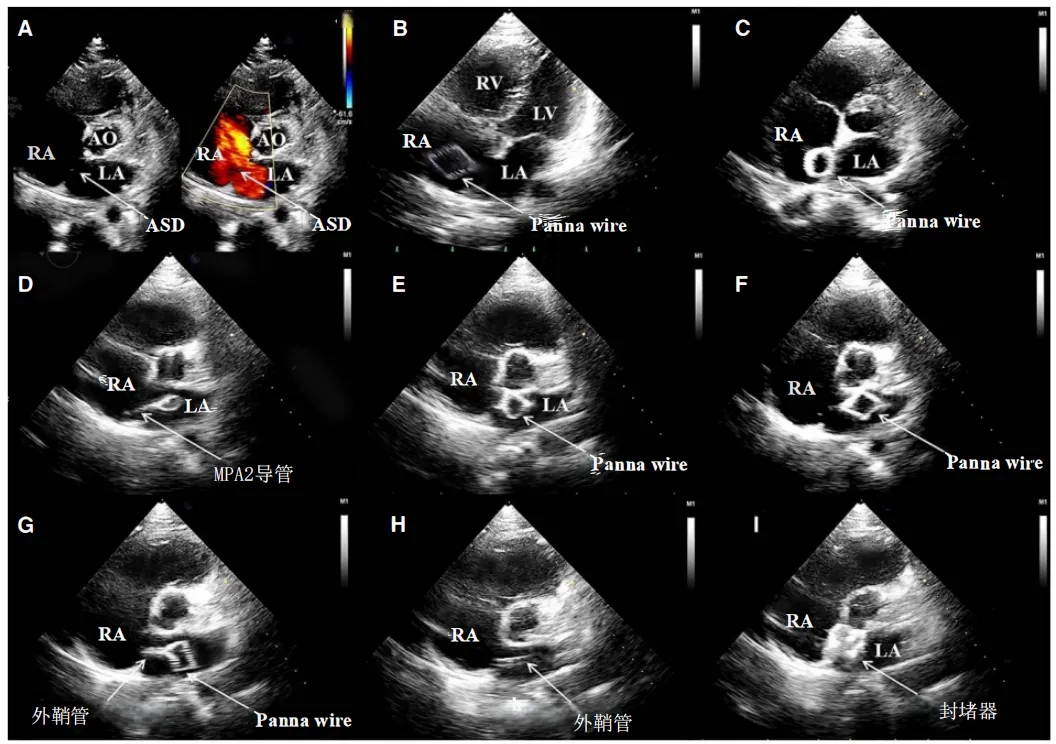
图2. 使用PannaWire导丝的经胸超声心动图引导手术
A、主动脉短轴切面显示房间隔缺损。B、PannaWire导丝在右心房内推进。导丝头端易于被经胸超声心动图识别,而MPA2导管几乎不可见。若无增大的头端,导丝将难以被探测到。C、尝试通过ASD时,将PannaWire导丝部分收回至MPA2导管内,头端尺寸变小。D、PannaWire导丝与MPA2导管一同通过ASD并进入左心房。E、展开导丝头端,其在左心房内清晰可见、易于定位。F、PannaWire导丝保持在左心房内,输送鞘管沿导丝插入。梭形头端无法被拉入扩张器内(L型),从而防止输送鞘管插入过深而刺穿左心房。G、推进鞘管,将PannaWire导丝部分收回至鞘管内,头端尺寸变小。H、梭形头端消失并被回收入鞘管内,输送鞘管定位于左心房中部,从而防止鞘管插入过深或滑回右心房。I、释放封堵器。AO:主动脉;LV:左心室;MPA2:多功能导管;RV:右心室。
手术操作
符合条件的患者按1:1的比例随机分配,接受单纯经胸超声心动图引导下的经皮房间隔缺损封堵术,分别使用PannaWire导丝或传统导丝。随机分组由计算机生成,分组分配隐藏于不透明密封信封中。患者对随机分组分配设盲。要求医生能够独立完成超声引导下的经皮介入手术,且手术经验在>20例至<100例之间。
所有患者术前均接受经胸超声心动图重新评估ASD情况。在局部或全身麻醉后,穿刺右侧股静脉并置入鞘管。测量穿刺点至右胸骨旁第三肋间的距离,作为导管插入的工作长度。选择头端直径比ASD直径大4mm的PannaWire导丝。将PannaWire导丝装载至多功能(MPA2)导管中,然后在剑突下切面和四腔心切面引导下,经股静脉穿刺鞘管将导管送入右心房。导管插入体内的深度不宜超过工作长度。固定PannaWire导丝,同时回撤导管,直至导丝头端露出导管。梭形头端的设计使其在经胸超声心动图下右心房内显影清晰。在超声引导下,调整MPA2导管方向朝向ASD,然后将PannaWire导丝部分回撤至MPA2导管内,使梭形头端变小,从而使其能够通过ASD。将导管穿过缺损,在左心房内完全展开PannaWire导丝头端。保持导丝在左心房内,同时回撤MPA2导管和股静脉穿刺鞘管。然后根据封堵器直径选择8F至14F的输送鞘管,并沿PannaWire导丝将其送入左心房。梭形头端的设计使其不会被拉入扩张器内,从而防止输送鞘管插入过深而刺穿左心房。固定PannaWire导丝和扩张器,同时向前推送鞘管,直至梭形头端消失并被收入鞘管内,这有助于将输送鞘管定位至左心房中部并保持其位置。
传统导丝组的手术步骤与既往研究详述的步骤相同[6]。在传统导丝组中,在剑突下引导下,将MPA2导管和导丝一起经下腔静脉送入右心房。导丝保持在导管内,以增强超声回声并便于引导。在四腔心切面和胸骨旁短轴切面引导下,将导管调整方向朝向并通过ASD后,将导丝从导管内推出并保持在左心房内。导丝取出后,沿输送鞘管植入封堵器。封堵器直径比ASD直径大6至8mm。评估封堵器位置、对邻近心脏结构的潜在影响及残余分流后,释放封堵器并再次进行评估。考虑到患者安全,如果导丝无法成功通过ASD,或导丝取出后输送鞘管滑回右心房,则手术转为透视引导下的常规手术。若发生心脏穿孔、心包填塞或封堵器脱落等严重并发症,则立即进行开胸手术。
结局指标
手术成功率作为主要评价指标。手术成功定义为满足以下标准:导丝能够成功通过ASD进入左心房;输送鞘管能够在导丝引导下成功进入左心房,且在导丝撤出后不回落入右心房;导丝能够成功从患者体内撤出。
次要结局指标包括:主要不良事件发生率;手术时间;进入左心房所需时间;心律失常发作次数;误入三尖瓣次数;以及外周血管并发症。主要不良事件定义为术后1个月内发生的与器械或手术相关的任何并发症,包括但不限于:死亡;急诊手术;需行心包穿刺或手术处理的严重心包填塞;心脏穿孔;出血;以及与手术相关的卒中。手术时间定义为从穿刺至输送鞘管成功撤出的时间。进入左心房所需时间定义为从导丝进入股静脉至成功进入左心房的时间。心律失常发作次数定义为术中房性期前收缩、室上性心动过速、室性期前收缩、室性心动过速及房室传导阻滞发生的总次数。所有患者在门诊进行随访。术后1个月进行胸部X线检查、心电图及经胸超声心动图检查。术后发生的主要不良事件及外周血管并发症,以及术后1个月随访时进行的胸部X线检查、心电图及经胸超声心动图检查结果,均由各中心的两名经验丰富的心脏科医生进行盲法评估。
数据分析
根据我们既往的调研,在手术经验不超过100例的医生操作下,传统导丝在非透视手术中的手术成功率低于70%。在动物实验中[8],新型导丝的手术成功率为93%~100%。我们假设传统导丝组的手术成功率为70%,PannaWire导丝组的手术成功率为93%。据此,共需82例患者(每组41例)以提供80%的把握度检测两组间23%的差异,双侧α为0.05。假设10%的参与者将退出试验,我们估计共纳入100例患者(每组50例)将会是合适的。
我们按照意向性分析原则对所有结局进行分析。连续变量以均值±标准差、中位数(范围)或中位数(IQR)表示。分类变量以百分比表示。手术成功率、主要不良事件发生率及外周血管并发症发生率采用Fisher精确检验进行比较。手术时间、进入左心房所需时间及误入三尖瓣次数采用Wilcoxon秩和检验进行比较。心律失常发作次数采用t检验进行比较。统计分析使用SAS软件9.4版(SAS Institute,Inc,Cary,NC)进行。以P值<0.05为差异具有统计学意义。
3 结局
2018年7月至2019年9月,共有100例符合条件的患者被随机分配至PannaWire导丝组(n=52)或传统导丝组(n=48)(图3)。患者中位年龄为12岁(范围:2–65岁),女性占64%(n=64)。ASD中位直径为10mm(范围:5–28mm)。平均Qp/Qs为1.77±0.37。临床特征见表1。
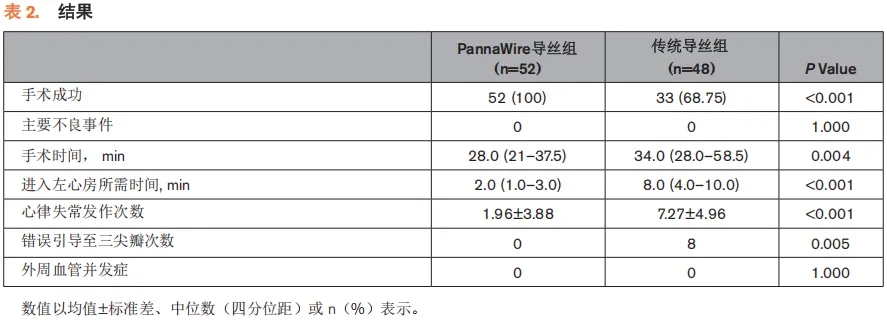
主要结局与次要结局指标总结于表2。主要评价指标——手术成功率,在PannaWire导丝组为100%(n=52),在传统导丝组为68.75%(n=33)(P<0.001)。在传统导丝组中,有2例(4.17%)患者因导丝被超声伪影误导、未能成功通过ASD进入左心房,导致输送系统无法沿导丝到达左心房;另有13例(27.08%)患者在导丝撤出后输送鞘管滑回右心房。上述共15例(31.25%)患者未能完成超声引导下手术,均在透视引导下成功植入封堵器。两组所有导丝均成功撤出。
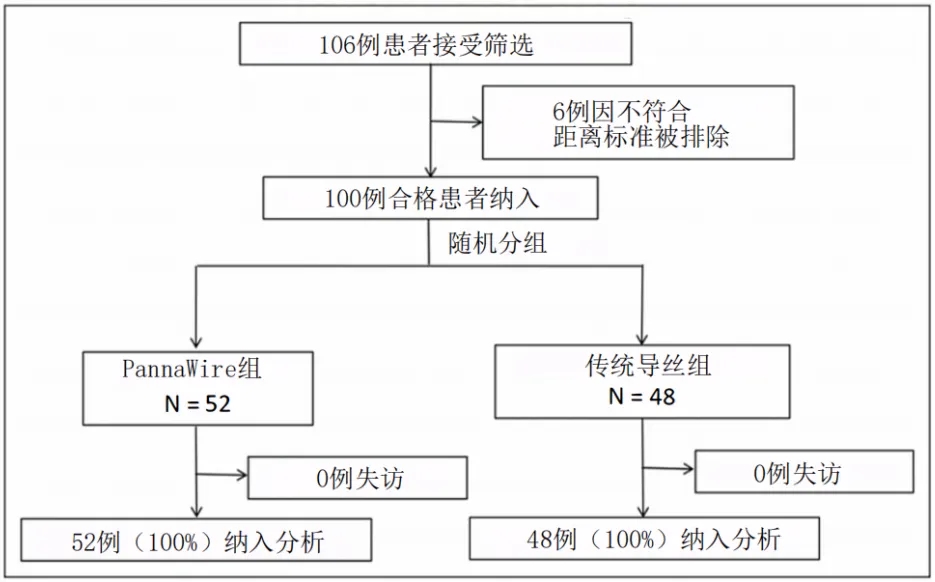
图3. 研究流程图
该流程图展示了本研究的患者招募、随机分组、手术操作、随访及分析过程。距离标准指缺损边缘与冠状静脉窦、上腔静脉及下腔静脉的距离均≥5mm,且与房室瓣的距离≥7mm。
两组均未发生主要不良事件。两组手术时间存在显著差异:PannaWire导丝组中位手术时间为28min(IQR:21–37.5),传统导丝组中位手术时间为34min(IQR:28–58.5)(P=0.004)。此外,使用PannaWire导丝进入左心房所需的时间短于传统导丝(中位时间2min[IQR:1–3]vs.8min[IQR:4–10],P<0.001)。心律失常发作次数在PannaWire导丝组为1.96±3.88次,在传统导丝组为7.27±4.96次(P<0.001)。PannaWire导丝组未发生导丝误入三尖瓣的事件,而传统导丝组有7例患者共发生8次错误引导事件(P=0.005)。
所有患者均完成了术后1个月的随访,未发生封堵器脱落或外周血管并发症。
4 讨论
尽管经皮手术具有微创、术后恢复优于外科手术等优势[2,3],但术中必须使用透视,这可能对患者和医生均产生不良影响[9-11]。此外,透视手术所需的高昂医疗设备也给欠发达地区带来了巨大的经济负担。无辐射经皮介入手术的开展旨在利用超声技术,惠及更多患者[5,6,12,13]。由于具有显著优势,这项新技术的应用数量持续上升,尤其是在发展中国家。然而,由于所有现有导丝均为透视引导手术而设计,并非针对超声引导手术,因此对于初级医生而言,学习曲线颇具挑战性。为此,我们设计了一款新型导丝,以改进超声引导下的手术操作。
PannaWire导丝由钢丝制成的导丝主体部和高度弹性的镍钛合金丝编织而成的梭形头端组成。与直头导丝相比,PannaWire导丝的可变头端尺寸易于被超声探测到,从而便于导丝和导管通过ASD。选择比ASD直径大4mm的PannaWire导丝头端宽度,可显著降低导丝滑回右心房的发生率。此外,导丝头端不能被回拉入扩张器内(L型),使得心脏穿孔几乎不可能发生。PannaWire导丝头端具有良好的弹性和柔软度,在遇到阻力时可发生形变,从而避免对心房壁造成损伤。
本文所描述和研究的梭形导丝是首个为促进超声引导手术而设计的新型导丝。共有15名符合条件的初级医生参与了我们的研究。与传统导丝相比,他们使用PannaWire导丝的手术时间和进入左心房所需时间均显著缩短。此外,在PannaWire导丝组中,所有导丝均成功通过ASD,且无一例输送鞘管滑入右心房。考虑到参与研究的医生仅具有有限的经胸超声心动图引导手术经验,且对PannaWire导丝并不熟悉,这些结果表明该导丝适合初级医生使用,并能够降低学习曲线。此外,在使用PannaWire导丝的手术中,心律失常发作次数更少,误入三尖瓣的发生率也更低,这反映出在经胸超声心动图引导下PannaWire导丝更易于被识别,且其头端接触心房壁和三尖瓣的频率更低。
PannaWire导丝的问世将促进无辐射经皮介入手术(例如动脉导管未闭封堵术)的更广泛应用,并使得为更多偏远地区的患者提供更好的治疗成为可能。
5 局限性
本研究关于PannaWire导丝的初步试验结果令人满意,但仍需在更多中心及更多医生的操作下进行验证。例如,本研究排除了在超声引导手术方面经验丰富的医生——这类医生数量仍然有限,且他们使用传统导丝的手术成功率相对较高。
6 结论
新型PannaWire导丝安全、有效,能够降低单纯经胸超声心动图引导下经皮房间隔缺损封堵术的学习曲线。
参考文献
1. Butera G, Biondi-Zoccai G, Sangiorgi G, Abella R, Giamberti A, Bussadori C, Sheiban I, Saliba Z, Santoro T, Pelissero G, et al. Percutaneous versus sur- gical closure of secundum atrial septal defects: a systematic review and meta-analysis of currently available clinical evidence. EuroIntervention. 2011;7:377–385. doi: 10.4244/EIJV7I3A63
2. Du ZD, Hijazi ZM, Kleinman CS, Silverman NH, Larntz K; Amplatzer Investigators. Comparison between transcatheter and surgical closure of secundum atrial septal defect in children and adults: results of a multi- center nonrandomized trial. J Am Coll Cardiol. 2002;39:1836–1844. doi: 10.1016/s0735-1097(02)01862-4
3. Moore J, Hegde S, El-Said H, Beekman R, 3rd, Benson L, Bergersen L, Holzer R, Jenkins K, Ringel R, Rome J, et al; ACC IMPACT Steering Com- mittee. Transcatheter device closure of atrial septal defects: a safety review. JACC Cardiovasc Interv. 2013;6:433–442. doi: 10.1016/j.jcin.2013.02.005
4. Kang IS, Kim SY, Jang KY, Lee HJ, Park SW, Jun TG, Park PW, Youn SW, Min JY. Transcatheter closure of atrial septal defect. Heart. 2001;31:576.
5. Pan XB, Pang KJ, Hu SS, Ouyang WB, Zhang FW, Zhang DW, Guo GL, Ge Y, Li SJ. [Safety and efficacy of percutaneous transcatheter closure of atrial septal defect under transesophageal echocardiography guidance in children]. Zhonghua Xin Xue Guan Bing Za Zhi. 2013;41:744–746.
6. Pan XB, Ou-Yang WB, Pang KJ, Zhang FW, Wang SZ, Liu Y, Zhang DW, Guo GL, Tian PS, Hu SS. Percutaneous closure of atrial septal defects under transthoracic echocardiography guidance without fluoroscopy or intubation in children. J Interv Cardiol. 2015;28:390–395. doi: 10.1111/joic.12214
7. Silvestry FE, Cohen MS, Armsby LB, Burkule NJ, Fleishman CE, Hijazi ZM, Lang RM, Rome JJ, Wang Y; American Society of Echocardiography; Soci- ety for Cardiac Angiography and Interventions. Guidelines for the echocar- diographic assessment of atrial septal defect and patent foramen ovale: from the American Society of Echocardiography and Society for Cardiac Angiography and Interventions. J Am Soc Echocardiogr. 2015;28:910–958. doi: 10.1016/j.echo.2015.05.015
8. Liu Y, Guo GL, Zhang FW, Wen B, Ou-Yang WB, Xie YQ, Pan XB. A novel wire is effective for echo-guiding percutaneous atrial septal defect closure: a preclini- cal study. J Healthc Eng. 2018;2018:5784567. doi: 10.1155/2018/5784567
9. Andreassi MG, Piccaluga E, Guagliumi G, Del Greco M, Gaita F, Picano E. Occupational health risks in cardiac catheterization labora- tory workers. Circ Cardiovasc Interv. 2016;9:e003273. doi: 10.1161/ CIRCINTERVENTIONS.115.003273
10. Hill KD, Frush DP, Han BK, Abbott BG, Armstrong AK, DeKemp RA, Glatz AC, Greenberg SB, Herbert AS, Justino H, et al; Image Gently Alliance. Radiation safety in children with congenital and acquired heart disease: a scientific position statement on multimodality dose optimization from the image gently alliance. JACC Cardiovasc Imaging. 2017;10:797–818. doi: 10.1016/j.jcmg.2017.04.003
11. Maioli M, Toso A, Leoncini M, Gallopin M, Musilli N, Bellandi F. Persistent renal damage after contrast-induced acute kidney injury: incidence, evo- lution, risk factors, and prognosis. Circulation. 2012;125:3099–3107. doi: 10.1161/CIRCULATIONAHA.111.085290
12. Liu Y, Guo GL, Wen B, Wang S, Ou-Yang WB, Xie Y, Pan XB. Feasibility and effectiveness of percutaneous balloon mitral valvuloplasty under echo- cardiographic guidance only. Echocardiography. 2018;35:1507–1511. doi: 10.1111/echo.14055
13. Wang SZ, Ou-Yang WB, Hu SS, Pang KJ, Liu Y, Zhang FW, Zhang DW, Pan XB. First-in-human percutaneous balloon pulmonary valvuloplasty under echocardiographic guidance only. Congenit Heart Dis. 2016;11:716– 720. doi: 10.1111/chd.12380

扫码下载文献PDF原文
· END ·
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系

发表留言
暂无留言
输入您的留言参与专家互动