病例分享 | 一例主动脉夹层病例诊治
主动脉夹层被称为人体内的“炸弹”,是一类相对少见但极其危重的疾病。发病急,死亡率高,如不能及时准确诊治,患者发病48小时内病死率以每小时1%的速度增长,1周时病死率可达70%,3个月可达90%。因此,提高对主动脉夹层的诊疗水平,是心血管内科医生必不可少的临床技能。
病史摘要
患者男性,87岁,主因“突发胸痛1小时”以“胸痛待查”收住院。患者于2018年7月13日晚饭后突发胸部疼痛,呈撕裂样,无背部放射痛,无意识丧失,无大汗、心悸、胸闷、四肢发冷、头晕、恶心、呕吐等症状,服用硝酸甘油后症状无好转,遂来急诊就诊。
既往史:否认糖尿病、冠心病病史。高血压病史23年余,血压最高150/90mmHg,长期口服氨氯地平、缬沙坦治疗,平时血压控制在110/60mmHg左右。升主动脉瘤样扩张病史8年余。高脂血症病史7年,长期服用辛伐他汀,血脂控制可。室性期前收缩病史14年余,5~6次/min。有青霉素过敏史。否认吸烟、饮酒史。母亲死于肺癌,父亲死于脑血管病。
入院时查体
体温36.5℃,脉搏72次/min,呼吸18次/min,血压135/78mmHg,脉氧饱和度99%。
神志清楚,双侧颈动脉未闻及血管杂音。双肺呼吸音清,未闻及干、湿啰音。心前区无隆起,未触及震颤,心界不大,心率72次/min,律不齐,可闻及期前收缩,各瓣膜听诊区未闻及病理性杂音,无心包摩擦音。腹部平软,无压痛及反跳痛,肝、脾肋下未触及。
辅助检查
1.心肌酶
正常范围。
2.凝血常规
血浆D-二聚体测定>20μg/ml。
3.ECG
窦性心动过速,心率100次/min,室性期前收缩。
4.肺CT平扫
降主动脉瘤样扩张,直径较前有所增加,可见内膜移位,不除外主动脉夹层(图1)。
5.腹部超声
未见异常。
6.心脏超声
左室射血分数58%。左室前壁室壁运动减弱,增厚(水肿)、回声略增强,升主动脉内径明显增宽(长约7.5cm范围内未见明确夹层征象,胸骨上凹等切面因患者躁动无法操作),左室后壁心包腔见宽约0.3cm的无回声暗区,余各房、室腔及大血管结构、大小未见明显异常。
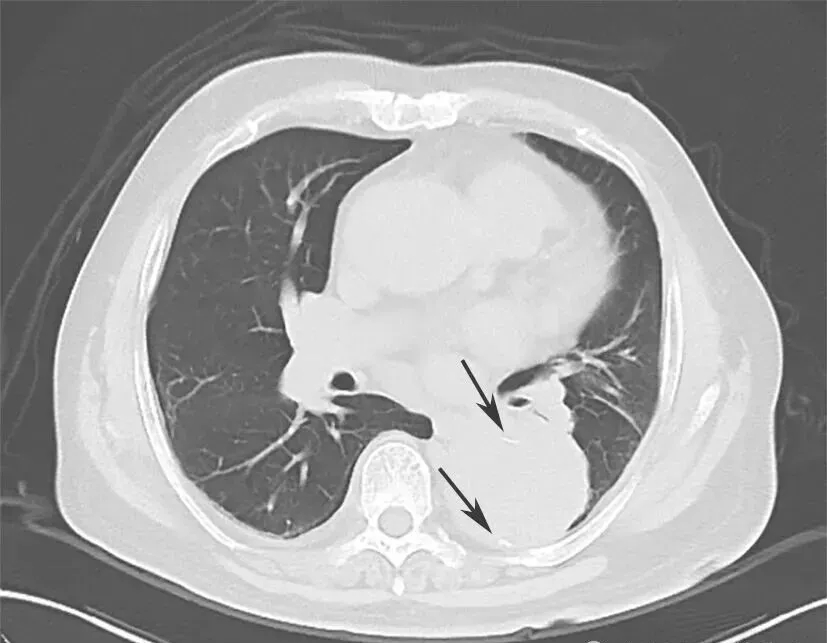
图1 肺部CT平扫(箭头处钙化点内移)
入院诊断
1.胸痛待查,主动脉夹层?急性冠脉综合征?
2.高血压,1级、极高危。
3.心律失常,频发多源室性期前收缩。
4.高脂血症。
诊断思路及首要问题
该患者的首要问题是明确诊断,急性冠脉综合征、主动脉夹层、肺动脉血栓栓塞症常以急症胸痛就医。这些疾病发病急、变化快,若不在短时间内给予明确诊断和恰当治疗,患者将面临猝死的危险。
1.本例患者以胸痛为首发症状来诊,凝血常规提示D-二聚体显著升高,但患者脉氧饱和度持续波动于99%左右,心电图未见SⅠQⅢTⅢ及其他右室负荷过重的表现,考虑不支持急性肺栓塞,但仍不能完全除外。
2.患者持续胸痛,间断加重,含服硝酸甘油未见缓解,否认既往冠心病病史,心电图提示频发室性期前收缩,未见明显ST-T段改变。动态监测心肌酶未见明显升高。急性冠脉综合征诊断依据不足,但仍需监测心电图及心肌酶变化。
3.患者既往存在升主动脉瘤样扩张病史多年,此次复查肺CT显示升主动脉直径较前有所扩大。症状上呈撕裂样疼痛,加之D-二聚体显著升高,考虑患者主动脉夹层的诊断可能性大。
诊治过程
入院后紧急行血管螺旋CT扫描+三维重建,以明确主动脉病变。血管螺旋CT扫描+三维重建如图2所示。降主动脉至腹主动脉夹层动脉瘤并壁间血肿形成(累及主动脉弓至肾动脉开口平面)。升主动脉管径约4.9cm。主动脉弓与降主动脉弥漫管腔增粗,周围可见弥漫壁间血肿形成,向下延伸至肾动脉平面。主动脉弓上三大分支开口与显影良好。主动脉弓外径为5.4cm,内径约3.8cm。降主动脉外径为7.5cm,内径为4.8cm。气管隆嵴下平面降主动脉左前壁局限性钙化上方有一个溃疡,溃疡内有少量对比剂充盈。胸主动脉下段向右侧明显迂曲。腹主动脉与肾动脉平面上方可见内膜片与真假腔形成,假腔内有少量造影剂充填。腹腔干动脉和肠系膜上动脉开口未见受累。右肾动脉开口部分受累,左肾动脉开口未见受累。腹主动脉下段、双侧髂内外动脉血管形态良好。双侧胸腔中等量积(血)液(图3箭头处)。
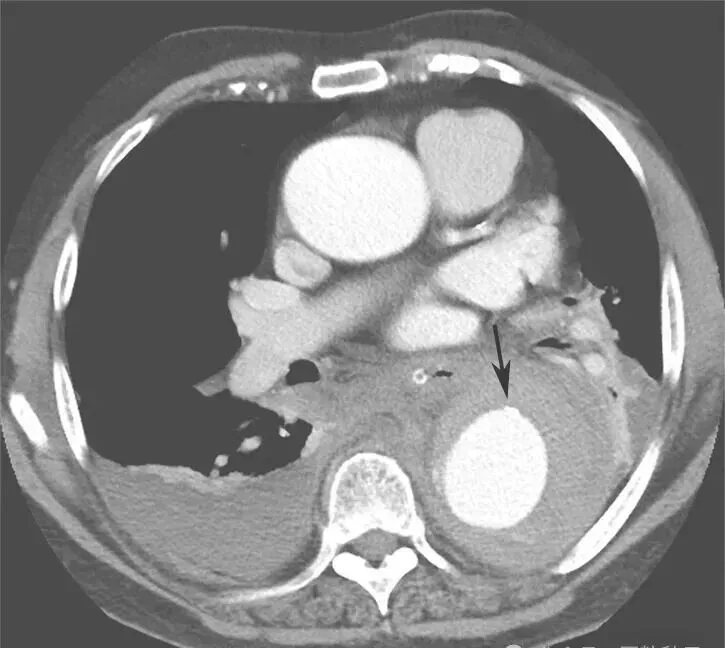
图2 主动脉CT螺旋扫描+三维重建
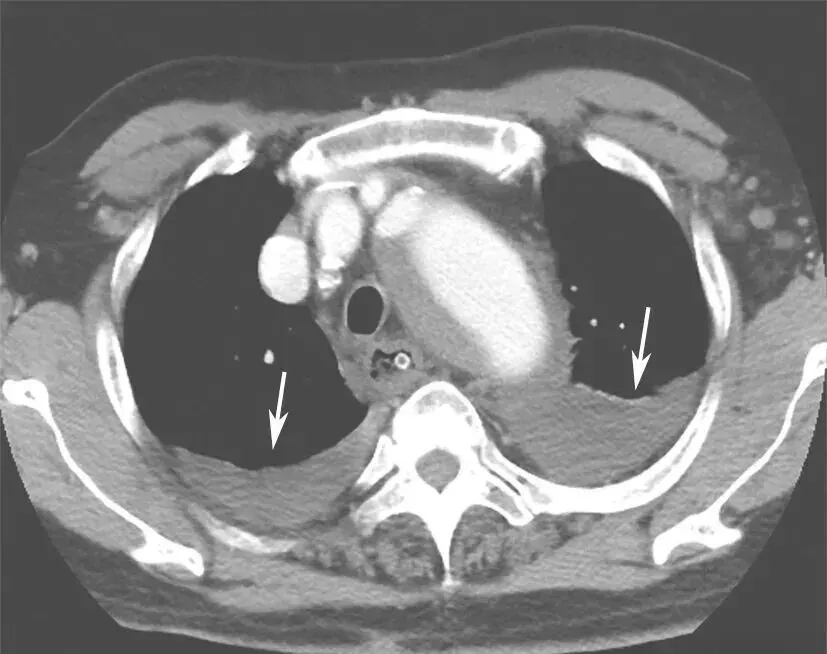
图3 双侧胸腔积(血)液
诊断明确,经血管外科会诊,考虑手术指征明确,完善术前检查后,在全身麻醉下行胸主动脉瘤腔内修复术(thoracic endovascular aneurysm repair,TEVAR),术中植入2枚GORE-TAG支架型血管,覆盖左锁骨下动脉开口至降主动脉折弯处,造影证实瘤体封闭良好。术中行左侧胸腔穿刺引流术。术后给予镇静、抗感染、营养支持等治疗。收缩压维持在100~140mmHg,术后第2天行右侧胸腔穿刺引流术。双侧胸腔共计引流血性积液1830ml。
最后诊断
1.主动脉夹层,动脉瘤腔内修复术后。
2.高血压,1级、极高危。
3.心律失常,频发多源室性期前收缩。
4.高脂血症。
临床结局
术后第20天15:20患者出现点头样呼吸,面色苍白,口唇发绀,听诊双肺呼吸音低,以左肺明显。2分钟后心搏骤停,给予持续胸外按压并反复给予药物复苏无效,15:50宣布临床死亡。抢救期间行胸腔超声探查示左侧大量胸腔积液,右侧少量;超声心动图显示,未见心包积液。死亡原因为主动脉夹层动脉瘤破裂。
诊治心得
患者的首发症状为胸痛,首先要围绕胸痛进行鉴别诊断。急性胸痛的临床表现各异,病情千变万化,危险性存在较大差异。急性心血管源性胸痛包括急性冠脉综合征、急性主动脉综合征和肺栓塞,称为胸痛三联征,是引发急性胸痛严重且危及生命的重要原因,需要临床医生选择快速、恰当且损伤较小的影像学检查手段,尽早识别这三种情况。
对于急性胸痛的患者,2010年AHA指南中提出疑诊主动脉夹层(aortic dissection,AD)的高危易感因素、胸痛特征和体征。IRAD研究基于上述高危因素提出AD危险评分,根据患者符合危险因素分类(高危易感因素、高危疼痛特征及高危体征)的类别数计0~3分(0分为低危,1分为中危,≥2分为高危);该评分≥1分,诊断AD的敏感度达95.7%。因此,对存在上述高危病史、症状及体征的初诊患者,应考虑AD可能并安排合理的辅助检查以明确诊断。基于患者入院时病史询问、体格检查对疾病确诊极为重要。本例患者既往有升主动脉瘤样扩张及高血压病史多年,因突发胸痛入院,AD危险评分≥2分,为AD高危,且门诊胸部CT平扫可见降主动脉瘤样扩张,直径较前有所增加,可见内膜移位,高度怀疑主动脉夹层。
随着64层螺旋CT出现后,使冠状动脉、肺动脉及主动脉血管同时成像成为可能,即一站式多层螺旋CT检查。多排螺旋CT具有无创、快速等优势,并且具有丰富的图像后处理软件,是急性胸痛三联征的病因筛查及确诊的有效手段,具有卓越的临床应用价值。该检查技术就是扩大胸部扫描范围,调整扫描参数和对比剂注射量及注射速度,同时得到主动脉、冠状动脉及肺动脉影像信息,影像医师应用工作站进行图像后处理,可以运用曲面重建(curved planar reconstruction,CPR)、最大密度投影(maximum intensity projection,MIP)、多平面重建(multi-planar reconstruction,MPR)、容积再现(volume rendering,VR)等对冠状动脉、肺动脉、主动脉及肺部进行观察。胸痛三联征一站式扫描技术的重点就是为急诊医师提供短时、高效、可靠的诊断信息,对降低患者并发症、病死率十分关键。《中国胸痛中心认证标准》(第5版)规定:胸痛中心应具备多排螺旋CT增强扫描的条件,并能开展急诊主动脉、肺动脉CTA检查,从启动CT室到接受患者进行检查的时间在30分钟以内。恰当运用多层螺旋CT检测不仅可以明确危及生命的胸部动脉疾病原因,指导治疗,还可以实现非常高的潜在的成本效益。主动脉夹层在影像学上典型的表现如图4。
如果在某一层面看到管腔中的低密度线影不连续,或是对比剂将两个管腔沟通,就可以判定夹层破口的位置(图5)。
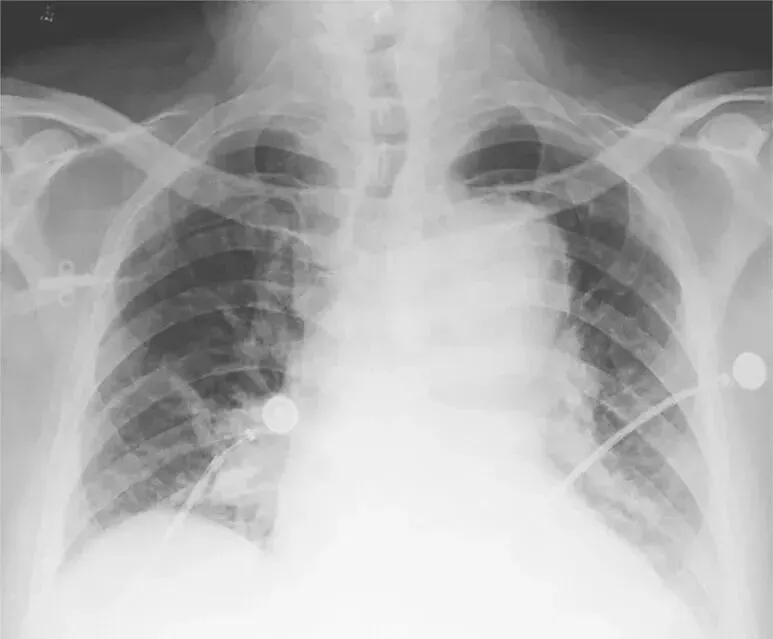
图4 主动脉夹层导致纵隔影增宽
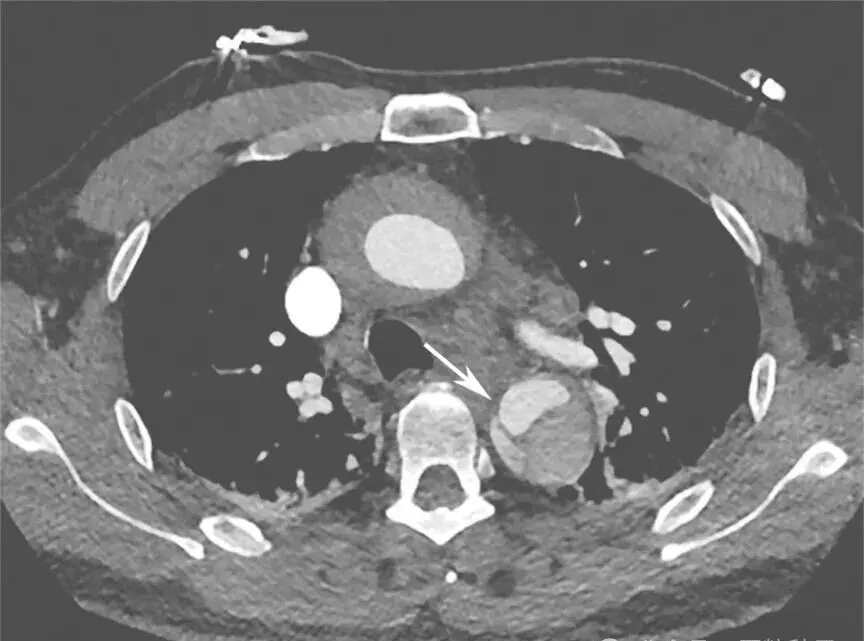
图5 主动脉夹层破口位置
本例患者在第一时间完善了血管增强CT及三维重建,主动脉夹层动脉瘤的诊断明确,为及时行主动脉瘤腔内修复术争取了时间。
根据血管螺旋CT扫描+三维重建结果,本例患者确诊为Stanford B3型主动脉夹层(急性期)。影响急性AD自然病程和预后的主要因素有病变的分型、病变范围和程度、有无并发症及血流动力学变化。患者死亡的主要原因是主动脉破裂、急性心脏压塞、急性心肌梗死、卒中、腹腔脏器缺血、肢体缺血等。急性Stanford B型AD发病2周内的病死率为6.4%,药物治疗的5年生存率约为60%。
AD初步治疗的原则是有效镇痛、控制心率和血压,减轻主动脉剪应力,降低主动脉破裂的风险,进一步治疗方案应根据AD的类型、合并症、疾病进展等因素综合考虑。对于Stanford A型AD患者,一经发现均应积极手术治疗。国内外对于急性Stanford A型AD应进行紧急外科手术治疗已经达成共识。长期的随访结果表明,Stanford A型夹层外科手术的效果明显优于内科保守治疗。而药物治疗是Stanford B型AD的基本治疗方式。一般而言,Stanford B型AD患者急性期药物保守治疗的病死率较低,部分患者可获得长期良好的预后。Stanford B型AD手术治疗的方法主要有腔内修复术(thoracic endovascular aneurysm repair,TEVAR)、开放性手术和Hybrid手术治疗等。孙立忠等根据孙氏细化分型提出Stanford B型AD手术治疗策略:①B1S型建议首选TEVAR,亚急性期(发病1~2周)是介入治疗的最佳时机;②B1C型建议行直视支架象鼻植入术或Hybrid手术;③B3型建议行全胸腹主动脉替换术。然而,由于Stanford B型AD患者的病情复杂多变,目前其最佳治疗方案依然存在争议。具体治疗方案需根据患者的具体病情和医疗机构的技术水平,选择最安全和最适合的治疗策略。本例患者在全麻下行胸主动脉瘤腔内修复术(TEVAR),术中植入2枚GORE-TAG支架型血管,覆盖左锁骨下动脉开口至降主动脉折弯处,造影证实瘤体封闭良好。术后经过控制血压、抗感染、营养支持等治疗,病情逐渐恢复。
胸主动脉腔内修复术(thoracic endovascular aortic repair,TEVAR)的主要目的是封闭原发破口,扩张真腔,改善远端脏器、肢体血供,促进假腔血栓化和主动脉重塑。TEVAR适用于锚定区充足(>1.5cm)、非遗传性结缔组织疾病性Stanford B型AD患者。国内荟萃分析结果表明,TEVAR治疗Stanford B型AD的手术成功率为97.66%~99.20%,术后早期患者的死亡比例低(术后30天死亡占2.2%~3.55%),近期疗效良好。IRAD研究表明,与药物治疗相比,TEVAR可提高急性Stanford B型AD患者5年生存率。2014年ESC指南推荐,对于复杂性Stanford B型AD首选腔内治疗;若合并内脏缺血、肢体缺血、疼痛无法控制、主动脉瘤变等严重并发症,需要急诊积极治疗。中国Stanford B型AD患者的平均发病年龄远低于欧美国家,预期寿命长。因此,专家委员会推荐,非复杂性Stanford B型AD患者在最佳药物治疗的基础上首选TEVAR作为进一步治疗措施;另外,TEVAR术中应根据患者病情选择合适类型的覆膜支架,以减小支架远端降主动脉过度扩张或新发破口形成风险。逆行性Stanford A型AD是Stanford B型AD行TEVAR术后最严重的并发症,其发生率为1.4%~10.0%,可能与主动脉壁病变(如合并结缔组织病、急性期主动脉壁水肿等)、术中操作不当、覆膜支架选择不当等因素有关,可发生于术中、术后或随访期,其中约有25%的患者没有症状,仅在复查CTA时发现。该并发症显著增加了患者住院死亡及并发症发生率,一经发现,应按Stanford A型AD治疗原则进行处理。患者在术后20天突发呼吸、心搏骤停,抢救无效死亡,死亡原因考虑为主动脉夹层动脉瘤破裂。该患者临终前病情变化突然,抢救期间行胸腔超声探查示左侧大量胸腔积液,可能为主动脉夹层动脉瘤破裂导致的血性胸腔积液,因患者家属不同意进行尸检,无法获得死亡的直接原因,推测与患者主动脉夹层撕裂范围大、主动脉壁水肿恢复延缓有关。
无论是采取药物保守治疗、腔内修复术或外科手术等治疗方法,AD患者均需要长期乃至终身进行规律的随访。即使手术康复出院的患者也有可能发生新发夹层、脏器缺血、动脉瘤形成或破裂等并发症。规律的随访有助于定期监测残余夹层的动态变化及主动脉重塑情况、评估脏器功能以及发现影响AD预后的危险因素(如难以控制的高血压、持续或突发疼痛、动脉瘤压迫症状等),为调整治疗药物或再次手术干预提供依据,改善患者远期预后。
综上所述,主动脉夹层是一种严重的心血管急、危、重症,起病急,进展快,非常凶险,病死率极高。应早期识别、尽早诊断以把握先机,采用合适的治疗方法及时救治,加强病情监测,提高患者生存率及生活质量。
急性心血管源性胸痛包括急性冠脉综合征、急性主动脉综合征和肺栓塞,称为胸痛三联征,是引发急性胸痛严重且危及生命的重要原因。
多排螺旋CT具有无创、快速等优势,并且具有丰富的图像后处理软件,是急性胸痛三联征的病因筛查及确诊的有效手段,具有卓越的临床应用价值。
主动脉夹层临床表现复杂多变、病情进展迅速,熟练掌握主动脉夹层的诊断及治疗流程,加强病情监测,降低死亡率。
-END-
专业的心血管医生学术交流平台


版权及免责声明:
本网站所发表内容知识产权归属医谱平台、主办方以及原作者等相关权利人,未经许可,禁止进行复制、传播、展示、镜像、转载、摘编等。经授权使用,须注明来源,否则将追究其法律责任。有关作品内容、版权和其他问题请与本网联系

发表留言
暂无留言
输入您的留言参与专家互动